网址:http://m.1010jiajiao.com/timu_id_455280[举报]
CH3—CH3→CH2=CH2+H2;有关化学键的键能如下。
化学键 C-H C=C C-C H-H
键能(kJ/mol) 414.4 615.3 347.4 435.3
试计算该反应的反应热?
查看习题详情和答案>>为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
⑴实验测得,1 g甲醇在氧气中充分燃烧生成二氧化碳和液态水释放出22.7kJ的热量,试写出甲醇燃烧的热化学方程式。
⑵由气态基态原子形成 1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
已知,CH3―CH3→CH2=CH2+H2;有关化学键的键能如下。
化学键 C-H C=C C-C H-H
键能(kJ/mol) 414.4 615.3 347.4 435.3
试计算该反应的反应热(在答题纸中写出计算过程)。
⑶依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行理论推算。
试依据下列热化学方程式,计算反应2C(s)+2H2(g)+O2(g) ![]() CH3COOH(l)的焓变(在答题纸中写出计算过程)。
CH3COOH(l)的焓变(在答题纸中写出计算过程)。
①CH3COOH(l)+2O2(g) ![]() 2CO2(g)+2H2O(l);△H1=-870.3kJ?mol-1
2CO2(g)+2H2O(l);△H1=-870.3kJ?mol-1
②C(s)+O2(g) ![]() CO2(g);△H2=-393.5kJ?mol-1
CO2(g);△H2=-393.5kJ?mol-1
③H2(g)+1/2O2(g) ![]() H2O(l);△H3=-285.8kJ?mol-1
H2O(l);△H3=-285.8kJ?mol-1
CH3―CH3→CH2=CH2+H2;有关化学键的键能如下。
化学键 C-H C=C C-C H-H
键能(kJ/mol) 414.4 615.3 347.4 435.3
试计算该反应的反应热
查看习题详情和答案>>(1)试计算该有机物的分子式.
(2)红外光谱测定,A分子结构中含有苯环和羟基.在常温下A可与浓溴水反应,1mol A最多可与2molBr2作用(只考虑主要产物),据此确定该有机物可能的结构简式.
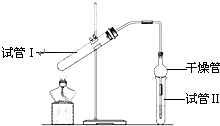 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用图的装置制备乙酸乙酯.
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用图的装置制备乙酸乙酯.(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:
(2)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验.实验开始先用酒精灯
微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中 试剂 |
有机层的 厚度/cm |
| A | 2mL乙醇、1mL乙酸、 1mL18mol?L-1 浓硫酸 |
饱和Na2CO3 溶液 |
3.0 |
| B | 2mL乙醇、1mL乙酸 | 0.1 | |
| C | 2mL乙醇、1mL乙酸、 3mL 2mol?L-1H2SO4 |
0.6 | |
| D | 2mL乙醇、1mL乙酸、盐酸 | 0.6 |
②分析实验
(3)若现有乙酸90g,乙醇138g发生酯化反应得到80g乙酸乙酯,试计算该反应的产率为