摘要:(三)情感.态度.价值观目标 1.从铁铜在国民经济发展中举足轻重的作用引入.以激发学生热爱社会主义祖国.献身科学的热情. 2.通过问题讨论的过程.使学生能主动与他人进行交流.清楚表达自己的观点.培养学生善于合作的精神.
网址:http://m.1010jiajiao.com/timu_id_4452814[举报]
(2013?淮南一模)已知Fe(NO3)2受热分解产物为金属氧化物、NO2和O2,请完成表格内容并回答相关问题:
(1)对固体产物中Fe化合价的猜想
猜想一:只显+2价;猜想二:只显+3价;猜想三:
(2)若猜想二成立,题干完成下表加以验证.供选试剂有:0.01mol/L酸性高锰酸钾溶液、0.1mol/LH2SO4溶液、3%H2O2溶液,0.1mol/LKSCN溶液、蒸馏水.(仪器自添)
经验证,猜想二正确,请写出Fe(NO3)2热分解的化学方程式
(3)某同学将带火星的木条伸入该分解反应参数的气体中,木条复燃,由此他得出“NO2能支持燃烧的结论”.请你判断该结论是否正确?并说明理由.
查看习题详情和答案>>
(1)对固体产物中Fe化合价的猜想
猜想一:只显+2价;猜想二:只显+3价;猜想三:
既有+2价又有+3价
既有+2价又有+3价
(2)若猜想二成立,题干完成下表加以验证.供选试剂有:0.01mol/L酸性高锰酸钾溶液、0.1mol/LH2SO4溶液、3%H2O2溶液,0.1mol/LKSCN溶液、蒸馏水.(仪器自添)
| 实验操作 | 现象 | 目的或结论 |
| 步骤1:取适量上述热分解后的固体于试管中,加入0.1mol/L | 溶解固体产物 | |
| 步骤2: | 溶液中含有Fe3+ | |
| 步骤3: | 溶液中不含有Fe 2+ |
4Fe(NO3)2
2Fe2O3+8NO2↑+O2↑
| ||
4Fe(NO3)2
2Fe2O3+8NO2↑+O2↑
;
| ||
(3)某同学将带火星的木条伸入该分解反应参数的气体中,木条复燃,由此他得出“NO2能支持燃烧的结论”.请你判断该结论是否正确?并说明理由.
(2013?达州模拟)有A、B、C、D、E五种短周期元素,其中A元素和B元素的原子都有一个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4;E元素的基态原子核外有六种运动状态的电子.请回答下列问题:
(1)A元素的简单离子基态时的电子排布式为

(2)CB3分子的空间构型是
(3)由D、E、C三元素可形成共价化合物(DEC)2(分子中各原子均达8电子稳定结构),每个分子中含
(4)E的一种低价氧化物与充入二氧化碳的空气和熔融碳酸钾可构成燃料电池.则该燃料电池的负极反应为
(5)1.2gE的单质在标准状况下的1.68L氧气中燃烧,至反应物耗尽,放出X KJ热量.则1molE与O2反应生成E的低价氧化物时的热化学方程式为
查看习题详情和答案>>
(1)A元素的简单离子基态时的电子排布式为
1s22s22p6
1s22s22p6
R是由C元素与氢元素两种元素形成的18电子分子,R的电子式为

(2)CB3分子的空间构型是
三角锥型
三角锥型
,其中心原子的杂化类型是sp3
sp3
(3)由D、E、C三元素可形成共价化合物(DEC)2(分子中各原子均达8电子稳定结构),每个分子中含
5
5
个δ键.(4)E的一种低价氧化物与充入二氧化碳的空气和熔融碳酸钾可构成燃料电池.则该燃料电池的负极反应为
CO+CO32--2e-=2CO2
CO+CO32--2e-=2CO2
正极反应为O2+2CO2+4e-=2CO32-
O2+2CO2+4e-=2CO32-
(5)1.2gE的单质在标准状况下的1.68L氧气中燃烧,至反应物耗尽,放出X KJ热量.则1molE与O2反应生成E的低价氧化物时的热化学方程式为
C(s)+
O2(g)=CO(g)△H=-(20X-Y)kJ/mol
| 1 |
| 2 |
C(s)+
O2(g)=CO(g)△H=-(20X-Y)kJ/mol
(已知:E的燃烧热为Y KJ/mol)| 1 |
| 2 |
多种物质的转化关系如下图所示(部分反应物或产物已略去,反应条件未列出):
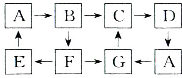
已知:①A、B、C、D、G含有同种元素,且它们的状态与颜色如下表所示:
②E是通常情况下密度最小的气体;B与AgNO3溶液反应生成不溶于稀硝酸的白色沉淀;一种气体氧化物M通入B溶液中可被氧化为F,F是含有三种元素的共价化合物,F与A反应生成E和G.
请回答下列问题:
(1)写出下列物质的化学式.
D: ;
E: .
(2)写出下列反应的离子方程式:
①B+M→F: ;
②A+F→E+G: .
(3)下列氧化物中能与G溶液反应直接生成C固体的是 (填字母).
a.Na2O2
b.SO2
c.CO2
d.BaO2.
查看习题详情和答案>>

已知:①A、B、C、D、G含有同种元素,且它们的状态与颜色如下表所示:
| 物质 | A单质 | B溶液 | C固体 | D固体 | G溶液 |
| 颜色 | 银白色 | 黄色 | 红褐色 | 红棕色 | 浅绿色 |
请回答下列问题:
(1)写出下列物质的化学式.
D:
E:
(2)写出下列反应的离子方程式:
①B+M→F:
②A+F→E+G:
(3)下列氧化物中能与G溶液反应直接生成C固体的是
a.Na2O2
b.SO2
c.CO2
d.BaO2.
有A、B、C、D、E五种短周期元素,其中A元素和B元素的原子都有一个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4;E元素的基态原子核外有六种运动状态的电子。请回答下列问题:
(1)A元素的简单离子基态时的电子排布式为 R是由C元素与氢元素两种元素形成的18电子分子,R的电子式为
(2)CB3分子的空间构型是 ,其中心原子的杂化类型是
(3)由D、E、C三元素可形成共价化合物(DEC)2(分子中各原子均达8电子稳定结构),每个分子中含 个δ键。
(4)E的一种低价氧化物与充入二氧化碳的空气和熔融碳酸钾可构成燃料电池。则该燃料电池的负极反应为 正极反应为
(5)1.2gE的单质在标准状况下的1.68L氧气中燃烧,至反应物耗尽,放出X KJ热量。则1molE与O2反应生成E的低价氧化物时的热化学方程式为 (已知:E的燃烧热为Y KJ/mol)
查看习题详情和答案>>
有A、B、C、D、E五种短周期元素,其中A元素和B元素的原子都有一个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4;E元素的基态原子核外有六种运动状态的电子.请回答下列问题:
(1)A元素的简单离子基态时的电子排布式为______R是由C元素与氢元素两种元素形成的18电子分子,R的电子式为______
(2)CB3分子的空间构型是______,其中心原子的杂化类型是______
(3)由D、E、C三元素可形成共价化合物(DEC)2(分子中各原子均达8电子稳定结构),每个分子中含______个δ键.
(4)E的一种低价氧化物与充入二氧化碳的空气和熔融碳酸钾可构成燃料电池.则该燃料电池的负极反应为______ 正极反应为______
(5)1.2gE的单质在标准状况下的1.68L氧气中燃烧,至反应物耗尽,放出X KJ热量.则1molE与O2反应生成E的低价氧化物时的热化学方程式为______ (已知:E的燃烧热为Y KJ/mol)
查看习题详情和答案>>
(1)A元素的简单离子基态时的电子排布式为______R是由C元素与氢元素两种元素形成的18电子分子,R的电子式为______
(2)CB3分子的空间构型是______,其中心原子的杂化类型是______
(3)由D、E、C三元素可形成共价化合物(DEC)2(分子中各原子均达8电子稳定结构),每个分子中含______个δ键.
(4)E的一种低价氧化物与充入二氧化碳的空气和熔融碳酸钾可构成燃料电池.则该燃料电池的负极反应为______ 正极反应为______
(5)1.2gE的单质在标准状况下的1.68L氧气中燃烧,至反应物耗尽,放出X KJ热量.则1molE与O2反应生成E的低价氧化物时的热化学方程式为______ (已知:E的燃烧热为Y KJ/mol)