摘要:16.(1) (2) , . (3) , .(4) 17 (1) .(2) . . .(3) . . 19(1)① ③ (2) (3) 泉州七中09届高三年上学期第三次月考化学试卷答案(考试时间:12月13日下午9:50---11:20) 满分 100 命卷人:林志鹏 复核人:肖 衡
网址:http://m.1010jiajiao.com/timu_id_444859[举报]
下列说法正确的组合是( )
(1)放热反应不需要加热就能反应,吸热反应不加热就不能反应
(2)物质发生化学变化都伴有能量的变化
(3)伴有能量变化的物质变化都是化学变化
(4)吸热反应和放热反应都有可能自发进行
(5)Na转化为Na+时,吸收的能量就是该过程的反应热
(6)水蒸气变为液态水时放出的能量就是该变化的反应热.
(1)放热反应不需要加热就能反应,吸热反应不加热就不能反应
(2)物质发生化学变化都伴有能量的变化
(3)伴有能量变化的物质变化都是化学变化
(4)吸热反应和放热反应都有可能自发进行
(5)Na转化为Na+时,吸收的能量就是该过程的反应热
(6)水蒸气变为液态水时放出的能量就是该变化的反应热.
| A、(1)(2) | B、(3)(5) | C、(2)(6) | D、(2)(4) |
对有机物 的下列说法中都不正确的是( )
的下列说法中都不正确的是( )
(1)常温下,能与NaHCO3溶液反应放出CO2
(2)能发生碱性水解反应,1摩该有机物完全反应消耗掉8摩NaOH
(3)与稀H2SO4共热,生成2种有机物
(4)该有机物的分子式为C14H12O9.
 的下列说法中都不正确的是( )
的下列说法中都不正确的是( )(1)常温下,能与NaHCO3溶液反应放出CO2
(2)能发生碱性水解反应,1摩该有机物完全反应消耗掉8摩NaOH
(3)与稀H2SO4共热,生成2种有机物
(4)该有机物的分子式为C14H12O9.
| A、(1)(2) | B、(3)(4) | C、(1)(3) | D、(2)(4) |
某研究小组模拟工业无隔膜电解法处理电镀含氰废水,进行以下有关实验,回答下列问题.
(1)实验I 制取次氯酸钠溶液,用石墨作电极电解饱和氯化钠溶液制取次氯酸钠溶液,生成次氯酸钠的离子方程式为 .
实验Ⅱ测定含氰废水处理百分率,利用如图所示装置进行实验:将CN-的浓度为0.2000mol?L-1的含氰废水100mL与l00mL NaClO溶液(过量)置于装置②锥形瓶中充分反应,打开分液漏斗活塞,滴入100ml,稀H2SO4,关闭活塞.
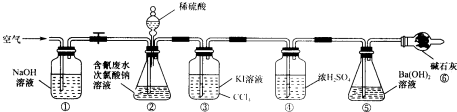
已知装置②中发生的主要反应依次为:
CN-+ClO-═CNO+Cl-
2CNO-+2H++3ClO-═N2↑+2CO2↑+3Cl-+H2O
(2)装置③的作用是 ,装置⑥的作用是 .
(3)反应结束后,缓缓通入空气的目的是 .
(4)为计算该实验中含氰废水被处理的百分率,需要测定 的质量.
(5)上述实验完成后,为了回收装置③中的CCl4需要的操作是 .
(6)若要研究装置②中所加稀硫酸的最佳浓度,请填写该装置进行实验的记录表.要求:①在进行理论判断后,将理论浓度作为第一组实验数据;②记录表要体现实验过程中的不变量、自变量、因变量.
查看习题详情和答案>>
(1)实验I 制取次氯酸钠溶液,用石墨作电极电解饱和氯化钠溶液制取次氯酸钠溶液,生成次氯酸钠的离子方程式为
实验Ⅱ测定含氰废水处理百分率,利用如图所示装置进行实验:将CN-的浓度为0.2000mol?L-1的含氰废水100mL与l00mL NaClO溶液(过量)置于装置②锥形瓶中充分反应,打开分液漏斗活塞,滴入100ml,稀H2SO4,关闭活塞.

已知装置②中发生的主要反应依次为:
CN-+ClO-═CNO+Cl-
2CNO-+2H++3ClO-═N2↑+2CO2↑+3Cl-+H2O
(2)装置③的作用是
(3)反应结束后,缓缓通入空气的目的是
(4)为计算该实验中含氰废水被处理的百分率,需要测定
(5)上述实验完成后,为了回收装置③中的CCl4需要的操作是
(6)若要研究装置②中所加稀硫酸的最佳浓度,请填写该装置进行实验的记录表.要求:①在进行理论判断后,将理论浓度作为第一组实验数据;②记录表要体现实验过程中的不变量、自变量、因变量.
| 实验 | c(H2SO4)mol.L-1 | V(H2SO4)mL | V(NaClO)mL | 含氯废水的体积mL |
| 1 | 100 | 100 | ||
| 2 | 0.0500 | 100 | 100 | |
| 3 | 0.2000 | 100 | 100 |
(8分)
I已知2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ/mol
2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ/mol
(1)氢气的燃烧热△H= kJ/mol
(2)燃烧2gH2生成水蒸气,放出的热量为 kJ。
Ⅱ把煤作为燃料可通过下列两种途径获得热量:
途径1:直接燃烧
C(s)+O2(g)=CO2(g) △H=E1 ①
途径2:先制成水煤气,再燃烧水煤气
C(s)+H2O(g)=CO(g)+H2(g) △H=E2 ②
H2(g)+1/2 O2(g)=H2O(g) △H=E3 ③
CO(g)+1/2 O2(g)=CO2(g) △H=E4 ④
请回答:
(1)上述四个热化学方程式中哪个反应△H >0? (填序号)
(2)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是
(填选项字母)。
A.途径1比途径2多 B.途径1比途径2少 C.途径1与途径2在理论上相同
(3)根据能量守恒定律,E1、E2、E3、E4之间的关系为 .
查看习题详情和答案>>
