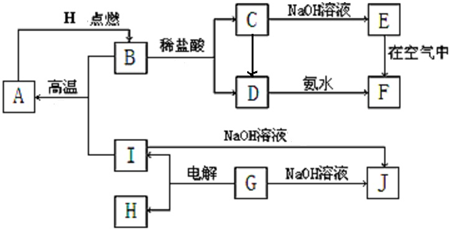
摘要:19.如图所示.A-I分别表示中学化学中常见的一种物质.它们之间的相互关系如下:A为坚硬难熔的主族元素的氧化物.D为紫红色固体单质且常温下能与浓HNO3反应生成H和红棕色气体.B为黑色固体.
网址:http://m.1010jiajiao.com/timu_id_444856[举报]
A~I分别表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素.I单质与NaOH溶液反应产生可燃性气体.
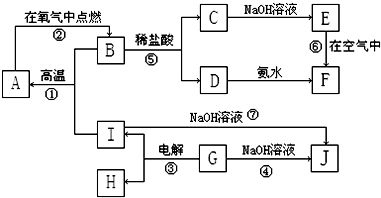
请填写下列空白:
(1)I、G、J三种物质中所含同一种元素在周期表中位置
(2)写出反应⑥的化学方程式
(3)写出反应⑦的化学方程式
(4)若28g A单质在足量的氧气中灼烧,反应放出的热量为Q kJ(Q>0),写出这个反应的热化学方程式:
(5)反应⑦中若有18g I参与反应,则转移电子数为
查看习题详情和答案>>

请填写下列空白:
(1)I、G、J三种物质中所含同一种元素在周期表中位置
第3周期、第IIIA族
第3周期、第IIIA族
;(周期和族)(2)写出反应⑥的化学方程式
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
;(3)写出反应⑦的化学方程式
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
;(4)若28g A单质在足量的氧气中灼烧,反应放出的热量为Q kJ(Q>0),写出这个反应的热化学方程式:
3Fe(s)+2O2(g)=Fe3O4(s);△H=-6QkJ?mol-1
3Fe(s)+2O2(g)=Fe3O4(s);△H=-6QkJ?mol-1
;(5)反应⑦中若有18g I参与反应,则转移电子数为
2
2
NA.A~I分别表示中学化学中常见的一种物质,它们之间相互关系如图所示:已知G在生产中可作为一种耐火材料,F是红褐色难溶于水的沉淀,A、B、C、D、E、F六种物质中均含同一种元素,其中I+B→A+G属于置换反应.(部分反应物、生成物没有列出).

请填写下列空白:
(1)如何检验D中阳离子:
(2)写出反应②的化学方程式:
写出反应⑦的离子方程式:
(3)E在空气中变成F的实验现象是
(4)写出反应⑥的化学方程式并用单线桥标出电子转移的方向和数目:
 计算该反应中若转移2mol电子,需要标况下的O2
计算该反应中若转移2mol电子,需要标况下的O2
查看习题详情和答案>>

请填写下列空白:
(1)如何检验D中阳离子:
取一定量的D溶液于试管中,滴加适量的KSCN溶液,若溶液出现血红色,则说明含Fe3+
取一定量的D溶液于试管中,滴加适量的KSCN溶液,若溶液出现血红色,则说明含Fe3+
(2)写出反应②的化学方程式:
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
| ||
写出反应⑦的离子方程式:
Al2O3+2OH-═2AlO2-+H2O
Al2O3+2OH-═2AlO2-+H2O
(3)E在空气中变成F的实验现象是
白色沉淀迅速变为灰绿色最后变为红褐色
白色沉淀迅速变为灰绿色最后变为红褐色
(4)写出反应⑥的化学方程式并用单线桥标出电子转移的方向和数目:


11.2
11.2
L. A~I分别表示中学化学中常见的一种物质,它们之间相互转化关系如图所示(部分反应物、生成物没有列出),且已知A、B、C、D、E、F六种物质中均含同一种元素,A、I是两种常见的金属单质.H在常温下是一种常见的非金属气态单质.
A~I分别表示中学化学中常见的一种物质,它们之间相互转化关系如图所示(部分反应物、生成物没有列出),且已知A、B、C、D、E、F六种物质中均含同一种元素,A、I是两种常见的金属单质.H在常温下是一种常见的非金属气态单质.请填写下列空白:
(1)写出C、G物质的化学式.
C
FeCl2
FeCl2
G
Al2O3
Al2O3
(2)写出反应①、⑥的化学方程式和反应④的离子方程式.
反应①:
3Fe3O4+8AL
9Fe+4Al2O3
| ||
3Fe3O4+8AL
9Fe+4Al2O3
| ||
该反应通常叫做
铝热
铝热
反应.反应⑥:
4Fe(OH)2+2H2O+O2=4Fe(OH)3
4Fe(OH)2+2H2O+O2=4Fe(OH)3
反应④:
2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
.