摘要:8.若ω1ω2分别表示浓度为amol·L-和bmol·L-硫酸的质量分数.且知2a=b.则下列推断正确的是 ( ) A.2ω1=ω2 B.ω1=2ω2 C.ω2>2ω1 D.ω1<ω2<2ω1
网址:http://m.1010jiajiao.com/timu_id_4441909[举报]
某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹).

请按要求填空:
(1)实验室利用B装置可制取的气体有
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.
①若在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由
②请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱(分别指出甲、乙、丙中盛放的试剂、实验现象及结论)
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得并进行NO2有关实验.
①B中发生反应的化学方程式为
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹
查看习题详情和答案>>

请按要求填空:
(1)实验室利用B装置可制取的气体有
H2、CO2、NO2、NOC2H2H2S等(答两个即可)
H2、CO2、NO2、NOC2H2H2S等(答两个即可)
(填化学式,写出两种即可).(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.
①若在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验 序号 |
实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气 泡产生 |
氯气与水反应的产物具有酸性 |
实验Ⅰ结论合理,实验Ⅱ结论不合理;制取的氯气中含有HCl气体,HCl溶于水后能与碳酸氢钠粉末反应产生气泡
实验Ⅰ结论合理,实验Ⅱ结论不合理;制取的氯气中含有HCl气体,HCl溶于水后能与碳酸氢钠粉末反应产生气泡
.②请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱(分别指出甲、乙、丙中盛放的试剂、实验现象及结论)
在甲、乙、丙中分别装入浓盐酸、二氧化锰、溴化钠溶液;烧瓶中有黄绿色气体生成,试管中溶液由无色变为橙色,可证明氯气的氧化性强于溴,则Br-的还原性强于Cl-
在甲、乙、丙中分别装入浓盐酸、二氧化锰、溴化钠溶液;烧瓶中有黄绿色气体生成,试管中溶液由无色变为橙色,可证明氯气的氧化性强于溴,则Br-的还原性强于Cl-
.(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得并进行NO2有关实验.
①B中发生反应的化学方程式为
Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O
.②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹
a、b
a、b
,再打开止水夹c
c
,使烧杯中的水进入试管丁的操作是双手紧握(或微热)试管丁,使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流入试管丁中
双手紧握(或微热)试管丁,使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流入试管丁中
.某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c表示止水夹).
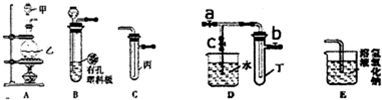
请按要求填空:
(1)如何检查B装置的气密性
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.
①若在丙中加入适量水,即可制得氯水.将所得氯水分成两份,进行I、II两个实验,实验操作、现象结论如下:
请你评价实验I、II的结论是否合理?若不合理,请说明理由.
②请利用上述装置设计一个简单的实验,验证C厂和B广的还原性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.
①B中发生反应的化学方程式为
②欲用D装置验证NO2与水的反应(此时c处于关闭状态),其操作步骤为:先关闭止水夹
③试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满水,则所得溶液中溶质的物质的量浓度是
查看习题详情和答案>>

请按要求填空:
(1)如何检查B装置的气密性
用止水夹夹住橡皮管,向长颈漏斗中加水,若试管中液面不再改变,则装置的气密性良好.
用止水夹夹住橡皮管,向长颈漏斗中加水,若试管中液面不再改变,则装置的气密性良好.
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.
①若在丙中加入适量水,即可制得氯水.将所得氯水分成两份,进行I、II两个实验,实验操作、现象结论如下:
| 实验 序号 |
实验操作 | 现象 | 结论 |
| I | 将氯水滴入品红溶液 | 溶液褪色 | Cl2与水反应的产物有漂白性 |
| II | 氯水中加入NaHCO3粉末 | 有无色气泡产生 | Cl2与水反应的产物具有较强的酸性 |
实验Ⅰ结论合理,实验Ⅱ结论不合理,因为制取的氯气中含有氯化氢气体,氯化氢溶于水后能与碳酸氢钠粉末反应产生气泡;
实验Ⅰ结论合理,实验Ⅱ结论不合理,因为制取的氯气中含有氯化氢气体,氯化氢溶于水后能与碳酸氢钠粉末反应产生气泡;
②请利用上述装置设计一个简单的实验,验证C厂和B广的还原性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)
在甲、乙、丙中分别装入浓盐酸、二氧化锰、溴化钠溶液,烧瓶中有黄绿色气体生成,试管中溶液由无色变为橙色,证明氯气的氧化性强于溴,则证明Br-的还原性强于Cl-.
在甲、乙、丙中分别装入浓盐酸、二氧化锰、溴化钠溶液,烧瓶中有黄绿色气体生成,试管中溶液由无色变为橙色,证明氯气的氧化性强于溴,则证明Br-的还原性强于Cl-.
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验.
①B中发生反应的化学方程式为
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
②欲用D装置验证NO2与水的反应(此时c处于关闭状态),其操作步骤为:先关闭止水夹
ab
ab
再打开止水夹c
c
,使烧杯中的水进入试管丁的操作是双手紧握试管丁使试管中气体逸出,二氧化氮与水接触后即可引发烧杯中的水倒流于试管丁.
双手紧握试管丁使试管中气体逸出,二氧化氮与水接触后即可引发烧杯中的水倒流于试管丁.
.③试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满水,则所得溶液中溶质的物质的量浓度是
0.045mol/L
0.045mol/L
(气体按标准状况计算).已知 NH3和 Cl2在常温下可快速反应生成氮气:2NH3+3Cl2→N2+6HCl.当 Cl2和 NH3 比例不同时,产物有差异.
(1)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 Cl2和 NH3的最佳比例为 .该反应可用于检验化工生产中氯气是否泄漏.如氯气有少量泄漏,用氨气检验时有明显现象,此过程中发生反应的Cl2和NH3的体积比范围为 .
(2)体积为1.12L,质量为3.335g的Cl2和N2的混合气体通过浓氨水后,体积变为0.672L(其中Cl2体积分数为50%)(气体体积均为标准状况下测定).则原混合气体中N2的体积为 mL.
(3)根据第(2)题数据,计算被氧化的NH3的质量.下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
(4)有Cl2和N2的混合气体,其中N2的体积分数为x,将1L该混合气体与1L氨气混合,讨论x取不同范围的数值时,所得气体体积y与x的关系式(所有气体体积均在相同状况下测定).
查看习题详情和答案>>
(1)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 Cl2和 NH3的最佳比例为
(2)体积为1.12L,质量为3.335g的Cl2和N2的混合气体通过浓氨水后,体积变为0.672L(其中Cl2体积分数为50%)(气体体积均为标准状况下测定).则原混合气体中N2的体积为
(3)根据第(2)题数据,计算被氧化的NH3的质量.下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
| 学生编号 | 所列第一步算式 | 未知数X表示的意义 | ||||
| 甲 |
|
|||||
| 乙 |
|
下表是短周期中部分元素的原子半径及主要化合价.
请回答:
(1)X在元素周期表中的位置是 ;
(2)V、W、Z三种元素的离子具有相同的电子层结构,三者的离子半径由大到小的顺序(用离子符号表示)是 ;并用离子方程式表示出Z离子可作净水剂的原因 ;
(3)M的单质能跟V的最高价氧化物水化物的热浓溶液发生氧化还原反应,生成两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式 ;
(4)W、X、Y分别与U均可形成10电子共价化合物,晶体类型均为 ,其中,属于非极性分子的是(写化学式) ,若将其作为燃料,以熔融的K2CO3为电解质,空气作为氧化剂,并选择适当的惰性电极,组成原电池.写出该电池工作时的负极反应式 .
查看习题详情和答案>>
| 元素代号 | U | V | W | X | Y | Z | M |
| 原子半径/nm | 0.037 | 0.157 | 0.074 | 0.075 | 0.077 | 0.143 | 0.102 |
| 主要化合价 | +1 | +1 | -2 | -3,+5 | +2,+4 | +3 | -2,+6 |
(1)X在元素周期表中的位置是
(2)V、W、Z三种元素的离子具有相同的电子层结构,三者的离子半径由大到小的顺序(用离子符号表示)是
(3)M的单质能跟V的最高价氧化物水化物的热浓溶液发生氧化还原反应,生成两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式
(4)W、X、Y分别与U均可形成10电子共价化合物,晶体类型均为
 (2011?江山市模拟)第28届夏季奥运会在北京成功举办,向世界人民展示了中国人的风采和北京的魅力.奥运五环象征着五大洲的团结以及全世界运动员以公正、坦率的比赛和友好的精神.“北京欢迎您”不仅是北京奥运会的主题歌也是吉祥物的“名字”也正好是五个环相一致(如图所示).
(2011?江山市模拟)第28届夏季奥运会在北京成功举办,向世界人民展示了中国人的风采和北京的魅力.奥运五环象征着五大洲的团结以及全世界运动员以公正、坦率的比赛和友好的精神.“北京欢迎您”不仅是北京奥运会的主题歌也是吉祥物的“名字”也正好是五个环相一致(如图所示).若奥运五环中的每一个环代表一种有机物,分别为A、B、C、D、E.已知:
a、它们都是芳香族化合物,均含有一个苯环且碳骨架完全相同,苯环上仅有一个侧链.
b、五个圆环之间相互套接处①和②、③和④、⑤和⑥、⑦和⑧分别表示两种有机物含有一种相同的官能团.
c、A分子中仅含有碳、氢两种元素,相对分子质量小于120,分子中的所有碳原子在同一平面内.
d、B和C能发生银镜反应,C、D、E能发生酯反应,C和D互为同分异构体,C经一步反应可转化为B,D经一步反应可以转化为E.
e、多个羟基连在同一个碳原子,则该有机物不能稳定存在,碳碳双键、叁键碳原子上一般不再连有羟基.
(1)A的结构简式为




(2)D转化为E的条件为
浓硫酸、加热
浓硫酸、加热
,该反应类型为消去反应
消去反应
.(3)写出下列转化的化学方程式:
B发生的银镜反应


C与足量的E反应
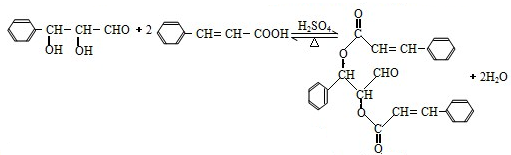

D在一定条件下生成高聚物的反应
 或
或
 或
或