摘要:7SO2Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
网址:http://m.1010jiajiao.com/timu_id_442507[举报]
 图是制取、洗涤并测量生成气体体积的装置示意图.利用上述装置进行下表所列实验,能达到试验目的是( ) 图是制取、洗涤并测量生成气体体积的装置示意图.利用上述装置进行下表所列实验,能达到试验目的是( )
|
查看习题详情和答案>>
 (2010?大连二模)有一化学样品Na2SO3,可能含有NaCl、Na2SO4、KNO3、K2CO2、K2SO4中的一种或几种杂质,某实验小组利用图提供的装置确定该样品的成分及Na2SO3的质量分数.称此样品6.30g,加入6.0mol?L-1的硫酸至过量,产生无色气体560mL(标准状况),向逸出气体后的溶液中加入稍过量的BaCl2溶液,得到白色沉淀9.32g,透过蓝色钻玻璃观察,滤液的焰色反应无紫色.请回答下列问题:
(2010?大连二模)有一化学样品Na2SO3,可能含有NaCl、Na2SO4、KNO3、K2CO2、K2SO4中的一种或几种杂质,某实验小组利用图提供的装置确定该样品的成分及Na2SO3的质量分数.称此样品6.30g,加入6.0mol?L-1的硫酸至过量,产生无色气体560mL(标准状况),向逸出气体后的溶液中加入稍过量的BaCl2溶液,得到白色沉淀9.32g,透过蓝色钻玻璃观察,滤液的焰色反应无紫色.请回答下列问题:(1)乙图溶液X是
浓H2SO4
浓H2SO4
,甲图煤油的作用是防止SO2与水接触
防止SO2与水接触
.(2)若实验中加入硫酸溶液的体积为5.00mL,则样品中Na2SO3的质量分数是
50%
50%
,写出有关离子方程式SO32-+2H+=SO2↑+H2O、Ba2++SO42-=BaSO4↓
SO32-+2H+=SO2↑+H2O、Ba2++SO42-=BaSO4↓
.(3)结合已提供的实验仪器,设计实验(实验仪器自选)如何正确测出气体的体积,简述操作步骤:
反应装置冷至室温后,再上下移动量筒,使量筒与甲瓶内液面保持水平,然后读取体积
反应装置冷至室温后,再上下移动量筒,使量筒与甲瓶内液面保持水平,然后读取体积
.(4)说明一定含有硫酸钠的依据:
产生沉淀的物质的量为0.04mol,而加入的硫酸物质的量为0.03mol,所以必有硫酸钠
产生沉淀的物质的量为0.04mol,而加入的硫酸物质的量为0.03mol,所以必有硫酸钠
.在Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑,反应中,
(1)
(2)用双线桥标出该反应电子转移的方向和数目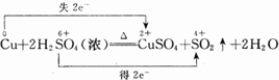
 .
.
Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑
(3)若有3.2g的Cu参与反应,则被还原的H2SO4的质量为多少?
查看习题详情和答案>>
| ||
(1)
Cu
Cu
元素被氧化,浓H2SO4
浓H2SO4
是氧化剂.(2)用双线桥标出该反应电子转移的方向和数目


Cu+2H2SO4(浓)
| ||
(3)若有3.2g的Cu参与反应,则被还原的H2SO4的质量为多少?
4.9g
4.9g
.某些金属氧化物跟熔融烧碱反应可以生成盐,根据下面化学反应框架图填空.

(1)单质F是
(2)写出由E生成G的离子方程式(或化学方程式)
(3)溶液I中所含金属离子是
(4)由C→E+F若改为浓酸,则不能选用的浓酸是(写分子式)
(5)写出由H生成I的离子方程式
查看习题详情和答案>>

(1)单质F是
H2
H2
,(2)写出由E生成G的离子方程式(或化学方程式)
Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+、4Fe(OH)2+O2+2H2O=4Fe(OH)3↓
Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+、4Fe(OH)2+O2+2H2O=4Fe(OH)3↓
.(3)溶液I中所含金属离子是
Na+、Al3+
Na+、Al3+
.(4)由C→E+F若改为浓酸,则不能选用的浓酸是(写分子式)
浓HNO3、浓H2SO4
浓HNO3、浓H2SO4
.(5)写出由H生成I的离子方程式
[Al(OH)4]-+4H+=Al3++4H2O
[Al(OH)4]-+4H+=Al3++4H2O
.如图所示为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置.其中E瓶中放有干燥红色布条;F中为铜网,F右端出气管口附近放在脱脂棉.

试回答:
(1)A中所放试剂为
(2)C中试剂是
(3)E中现象是
(4)H中试剂为
(5)整套装置中有两处用酒精灯加热,两处酒精灯点燃的先后顺序是
查看习题详情和答案>>

试回答:
(1)A中所放试剂为
浓盐酸
浓盐酸
,B中所放试剂为MnO2
MnO2
,二者反应的化学方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
,此反应的氧化剂是
| ||
MnO2
MnO2
.(2)C中试剂是
饱和NaCl溶液
饱和NaCl溶液
,其作用是除去Cl2中的HCl
除去Cl2中的HCl
.D中试剂是浓H2SO4
浓H2SO4
,其作用是除去Cl2中的水蒸气
除去Cl2中的水蒸气
.(3)E中现象是
黄绿色气体充满试剂瓶,红布不褪色
黄绿色气体充满试剂瓶,红布不褪色
.F中现象是产生大量棕色烟
产生大量棕色烟
.反应的化学方程式为Cu+Cl2
CuCl2
| ||
Cu+Cl2
CuCl2
.F管中脱脂棉的作用是
| ||
防止生成的氯化铜颗粒堵塞导管
防止生成的氯化铜颗粒堵塞导管
.(4)H中试剂为
NaOH溶液
NaOH溶液
,反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O
Cl2+2NaOH=NaCl+NaClO+H2O
.(5)整套装置中有两处用酒精灯加热,两处酒精灯点燃的先后顺序是
先点燃B处酒精灯,待黄绿色气体充满F后,再点燃F处酒精灯
先点燃B处酒精灯,待黄绿色气体充满F后,再点燃F处酒精灯
.