摘要:分析:(1)本题是用计算推理方法确定混合烃的组成.1L碳原子数为n的烷烃或烯烃充分燃烧均得到nL CO2.由题意推断.该混合烃只能由碳原子数大于3.6的烷烃和碳原子数小于3.6的烯烃或炔烃组成.它们可能有四种组合.根据每种组合中烷烃和不饱和烃的碳原子数及燃烧后生成CO2的体积可能有四种组合.根据每种组合中烷烃和不饱和烃的碳原子数及燃烧后生成CO2的体积可确定A和B的体积比.例如:若A为C4H10.B为C2H4.设1升混合气中含C4H10为x L.含C2H4为(1-x)L.它们充分燃烧后分别得到4x升CO2和2(1-x)L CO2.根据1升混合气燃烧后得到3.6LCO2.可得4x+2(1-x)=3.6
网址:http://m.1010jiajiao.com/timu_id_442438[举报]
(10分)通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。如图是用燃烧的方法确定有机物分子式的常用装置。

试回答下列问题:
(1)产生的氧气按从左到右流向,所选装置各导管的连接顺序是_____________ 。
(2)C装置中浓硫酸的作用是_______________。
(3)燃烧管中CuO的作用是_______________。[来源:]
(4)若准确称取0.48 g样品,经充分燃烧,A管质量增加1.32 g,B管质量增加1.08 g,则该有机物是否含氧元素 ? ______填(有、无)该有机物的分子式为_______
查看习题详情和答案>>
(10分)通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。如图是用燃烧的方法确定有机物分子式的常用装置。
试回答下列问题:
(1)产生的氧气按从左到右流向,所选装置各导管的连接顺序是_____________ 。
(2)C装置中浓硫酸的作用是_______________。
(3)燃烧管中CuO的作用是_______________。
(4)若准确称取0.48 g样品,经充分燃烧,A管质量增加1.32 g,B管质量增加1.08 g,则该有机物是否含氧元素 ? ______填(有、无)该有机物的分子式为_______
查看习题详情和答案>>
(1)现用物质的量浓度为a mol/L的标准盐酸去测定V mL NaOH溶液的物质的量浓度,请填写下列空白:
酸式滴定管用蒸馏水洗净后,还应该进行的操作是
;若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度会
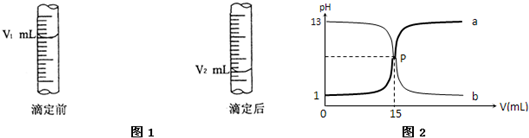
(2)图2是盐酸与氢氧化钠的滴定曲线a和b,试认真分析后填空:
曲线a是用
查看习题详情和答案>>
酸式滴定管用蒸馏水洗净后,还应该进行的操作是
用标准盐酸润洗2-3次
用标准盐酸润洗2-3次
;图1是酸式滴定管中液面在滴定前后的读数,则c (NaOH)=| a(V2-V1) |
| V |
| a(V2-V1) |
| V |
偏高
偏高
(偏高、偏低).(2)图2是盐酸与氢氧化钠的滴定曲线a和b,试认真分析后填空:
曲线a是用
NaOH
NaOH
溶液滴定HCl
HCl
溶液;曲线b是用HCl
HCl
溶液滴定NaOH
NaOH
溶液;盐酸的物质的量浓度为0.1
0.1
mol/L.
Ⅰ.下列有关实验操作中,合理的是
A.用托盘天平称取11.70g食盐
B.用量筒量取12.36mL盐酸
C.用酸式滴定管量取21.20mL 0.10mol/L H2SO4溶液
D.用200mL容量瓶配制500mL 0.1mol/L NaCl溶液
E.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较
Ⅱ.现用物质的量浓度为a mol/L的标准盐酸去测定V mL NaOH溶液的物质的量浓度,请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,还应该进行的操作是
(2)图1是酸式滴定管中液面在滴定前后的读数:c (NaOH)=
mol/L.

(3)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度
III.如图2是盐酸与氢氧化钠的滴定曲线a和b,试认真分析后填空:
曲线a是用
查看习题详情和答案>>
C
C
(填序号).A.用托盘天平称取11.70g食盐
B.用量筒量取12.36mL盐酸
C.用酸式滴定管量取21.20mL 0.10mol/L H2SO4溶液
D.用200mL容量瓶配制500mL 0.1mol/L NaCl溶液
E.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较
Ⅱ.现用物质的量浓度为a mol/L的标准盐酸去测定V mL NaOH溶液的物质的量浓度,请填写下列空白:
(1)酸式滴定管用蒸馏水洗净后,还应该进行的操作是
用标准盐酸润洗2-3次
用标准盐酸润洗2-3次
.(2)图1是酸式滴定管中液面在滴定前后的读数:c (NaOH)=
| a(V2-V1) |
| V |
| a(V2-V1) |
| V |

(3)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的NaOH物质的量浓度
偏大
偏大
.(选“偏大”“偏小”“不变”)III.如图2是盐酸与氢氧化钠的滴定曲线a和b,试认真分析后填空:
曲线a是用
NaOH
NaOH
溶液滴定HCl
HCl
溶液;曲线b是用HCl
HCl
溶液滴定NaOH
NaOH
溶液;P点的坐标为(15,7)
(15,7)
;盐酸的物质的量浓度为0.1
0.1
mol/L.
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置先进行了有关实验:
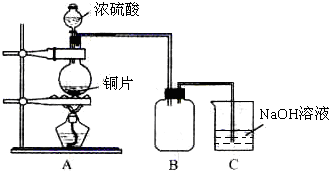
(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整.
(2)实验中他们取6.4g 铜片和12mL 18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①写出铜跟浓硫酸反应的化学方程式: ;
②有一定量的余酸但未能使铜片完全溶解,你认为其中原因是 ;
(3)为定量测定余酸的物质的量浓度,该小组学生进行了如下设计:
先测定铜与浓硫酸反应产生的SO2的量,再计算余酸的物质的量浓度.他们认为测定二氧化硫的量的方法有多种,你认为下列实验方案中可行的是 (填写编号).
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量氯化钡溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(已折算成标准状况)
D.将装置A产生的气体缓缓通入足量氢氧化钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
E.将装置A产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
请你对不可行的方案中选出一例进行分析: [要求标明不可行的方案序号、说出不可行的理由及造成的误差(偏高或偏低)].
(4)请你再设计一种其他可行的实验方案,来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算) .
查看习题详情和答案>>

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整.
(2)实验中他们取6.4g 铜片和12mL 18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①写出铜跟浓硫酸反应的化学方程式:
②有一定量的余酸但未能使铜片完全溶解,你认为其中原因是
(3)为定量测定余酸的物质的量浓度,该小组学生进行了如下设计:
先测定铜与浓硫酸反应产生的SO2的量,再计算余酸的物质的量浓度.他们认为测定二氧化硫的量的方法有多种,你认为下列实验方案中可行的是
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将装置A产生的气体缓缓通入足量用稀硫酸酸化的高锰酸钾溶液,再加入足量氯化钡溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(已折算成标准状况)
D.将装置A产生的气体缓缓通入足量氢氧化钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
E.将装置A产生的气体缓缓通入足量硝酸酸化的硝酸钡溶液,反应完全后,过滤、洗涤、干燥、称量沉淀
请你对不可行的方案中选出一例进行分析:
(4)请你再设计一种其他可行的实验方案,来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算)