摘要:5.腐蚀的常见类型 (1)析氢腐蚀 在酸性条件下.正极发生2H++2e-=H2↑反应. (2)吸氧腐蚀 在极弱酸或中性条件下.正极发生2H2O+O2+4e-=4OH-反应.若负极金属不与电解质溶液发生直接的反应.则形成吸氧腐蚀的原电池反应.如生铁浸入食盐水中.会形成许多微小的原电池.
网址:http://m.1010jiajiao.com/timu_id_441894[举报]
在工业上,氯气是一种重要的化工原料;在实验室中,氯气和氯水是重要的化学试剂。
(1)资料显示,漂白粉在酸性(如硫酸)条件下可发生反应并生成氯气,有关反应的化学方程式为 Ca(ClO)2+CaCl2+2H2SO4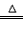 2CaSO4+2Cl2↑+2H2O。某学习小组利用此反应原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此反应原理设计如图所示装置制取氯气并探究其性质。
(1)资料显示,漂白粉在酸性(如硫酸)条件下可发生反应并生成氯气,有关反应的化学方程式为 Ca(ClO)2+CaCl2+2H2SO4
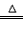 2CaSO4+2Cl2↑+2H2O。某学习小组利用此反应原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此反应原理设计如图所示装置制取氯气并探究其性质。 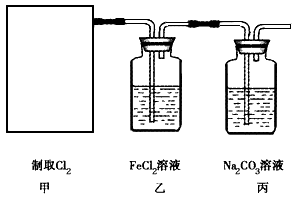
①在该实验中,甲部分的装置是__(填字母序号)。
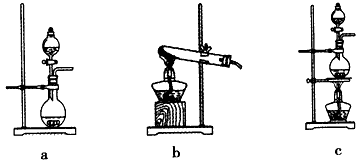
②证明乙装置中FeCl2与Cl2发生了氧化还原反应的方法是___。
③丙装置中通入少量的Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强 于次氯酸,则丙中发生反应的化学方程式是___。
④该实验存在一个明显的缺陷,改进的方法是___
(2)某同学设计了一个实验方案以证明新制氯水中含有次氯酸。他所用的试剂如下:新制氯水、 0.5 mol.L-1的CaCl2溶液、品红溶液、CaCO3粉末,请你协助他完成实验方案。
步骤一:取5 mL 0.5 mol.L-1的CaCl2溶液于试管中,滴入3滴品红溶液,振荡,溶液不褪色。
步骤二:取5 mL新制氯水于试管中,___。
步骤三:____。 说明新制氯水中存在次氯酸的实验现象是___。设计步骤一的理由是___。
查看习题详情和答案>>
③丙装置中通入少量的Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强 于次氯酸,则丙中发生反应的化学方程式是___。
④该实验存在一个明显的缺陷,改进的方法是___
(2)某同学设计了一个实验方案以证明新制氯水中含有次氯酸。他所用的试剂如下:新制氯水、 0.5 mol.L-1的CaCl2溶液、品红溶液、CaCO3粉末,请你协助他完成实验方案。
步骤一:取5 mL 0.5 mol.L-1的CaCl2溶液于试管中,滴入3滴品红溶液,振荡,溶液不褪色。
步骤二:取5 mL新制氯水于试管中,___。
步骤三:____。 说明新制氯水中存在次氯酸的实验现象是___。设计步骤一的理由是___。
(1)钢含碳量为
(2)电化学腐蚀是造成钢铁腐蚀的主要原因,它包括
查看习题详情和答案>>
0.03%~2%
0.03%~2%
;油脂在体内水解后的产物是高级脂肪酸与甘油
高级脂肪酸与甘油
.检验糖尿病患者的尿液可以选用的化学试剂是新制的Cu(OH)2
新制的Cu(OH)2
,产生的现象为产生红色沉淀
产生红色沉淀
.淀粉和纤维素是重要的多糖,它们在催化剂的作用下都能发生水解反应,反应的最终产物都是葡萄糖
葡萄糖
.(2)电化学腐蚀是造成钢铁腐蚀的主要原因,它包括
析氢
析氢
腐蚀和吸氧
吸氧
腐蚀.

