摘要:2.外内:(1)浓度:浓度越大.单位体积内活化分子数 .有效碰撞的几率 .发生化学反应的速率 ,因此.化学反应速率与浓度有密切的关系.浓度越大.化学反应速率越快.增大反应物的浓度.正反应速率加快.(2)温度:温度越高.一方面活化分子百分数 .另一方面含有较高能量的分子间的碰撞频率 .两个方面都使分子间有效碰撞的几率 .反应速率 .(3)压强:对于有气体参与的化学反应.通过改变容器体积而使压强变化的情况:压强增大.相当于浓度 .反应速率 .(反应物和生成物的浓度都增大.正逆反应速率都增大.相反.亦然).(4)催化剂:使用正催化剂.反应所需的活化能 .活化分子百分数 .有效碰撞的几率 .化学反应速率 (对于可逆的反应使用催化剂可以同等程度地改变正逆反应速率).试题枚举
网址:http://m.1010jiajiao.com/timu_id_441773[举报]
 以下是某实验小组用CO2和NaOH溶液做喷泉实验的装置和测得的一组数据
以下是某实验小组用CO2和NaOH溶液做喷泉实验的装置和测得的一组数据| NaOH浓度(mol/L) | 0 | 0.4 | 0.5 | 0.8 | 1.0 | 1.4 | 1.6 | 1.8 |
| 现象 | 不能 形成 |
一段 液柱 |
形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 |
| 时间 | 6min | 1min | 35s | 10s | 6s | 6s | ||
| 烧瓶中水的体积(mL) | 7 | 41 | 71 | 125 | 240 | 240 |
C
C
A.CO2在水中的溶解度小,不宜用水直接吸收CO2来做喷泉实验
B.在一定的浓度范围内氢氧化钠溶液的浓度越大越易形成喷泉
C.NaOH浓度为1.6mol/L时,CO2还没有全部分被吸收
D.当氢氧化钠溶液的物质的量浓度为1.0mol/L时所得溶液不可能有氢氧化钠,烧瓶也没有充满.
以下是某实验小组用CO2和NaOH溶液做喷泉实验的装置和测得的一组数据
已知:烧瓶最大容量为250mL,每次实验充分摇动烧瓶,只有NaOH浓度不同,其它条件和操作方式相同.结合喷泉实验原理及你所学的知识,判断下列说法中不正确的是______
A.CO2在水中的溶解度小,不宜用水直接吸收CO2来做喷泉实验
B.在一定的浓度范围内氢氧化钠溶液的浓度越大越易形成喷泉
C.NaOH浓度为1.6mol/L时,CO2还没有全部分被吸收
D.当氢氧化钠溶液的物质的量浓度为1.0mol/L时所得溶液不可能有氢氧化钠,烧瓶也没有充满.
查看习题详情和答案>>
| NaOH浓度(mol/L) | 0 | 0.4 | 0.5 | 0.8 | 1.0 | 1.4 | 1.6 | 1.8 |
| 现象 | 不能 形成 |
一段 液柱 |
形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 |
| 时间 | 6min | 1min | 35s | 10s | 6s | 6s | ||
| 烧瓶中水的体积(mL) | 7 | 41 | 71 | 125 | 240 | 240 |
A.CO2在水中的溶解度小,不宜用水直接吸收CO2来做喷泉实验
B.在一定的浓度范围内氢氧化钠溶液的浓度越大越易形成喷泉
C.NaOH浓度为1.6mol/L时,CO2还没有全部分被吸收
D.当氢氧化钠溶液的物质的量浓度为1.0mol/L时所得溶液不可能有氢氧化钠,烧瓶也没有充满.

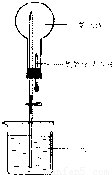
以下是某实验小组用CO2和NaOH溶液做喷泉实验的装置和测得的一组数据
已知:烧瓶最大容量为250mL,每次实验充分摇动烧瓶,只有NaOH浓度不同,其它条件和操作方式相同.结合喷泉实验原理及你所学的知识,判断下列说法中不正确的是______
A.CO2在水中的溶解度小,不宜用水直接吸收CO2来做喷泉实验
B.在一定的浓度范围内氢氧化钠溶液的浓度越大越易形成喷泉
C.NaOH浓度为1.6mol/L时,CO2还没有全部分被吸收
D.当氢氧化钠溶液的物质的量浓度为1.0mol/L时所得溶液不可能有氢氧化钠,烧瓶也没有充满.
 查看习题详情和答案>>
查看习题详情和答案>>
| NaOH浓度(mol/L) | 0.4 | 0.5 | 0.8 | 1.0 | 1.4 | 1.6 | 1.8 | |
| 现象 | 不能 形成 | 一段 液柱 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 |
| 时间 | 6min | 1min | 35s | 10s | 6s | 6s | ||
| 烧瓶中水的体积(mL) | 7 | 41 | 71 | 125 | 240 | 240 |
A.CO2在水中的溶解度小,不宜用水直接吸收CO2来做喷泉实验
B.在一定的浓度范围内氢氧化钠溶液的浓度越大越易形成喷泉
C.NaOH浓度为1.6mol/L时,CO2还没有全部分被吸收
D.当氢氧化钠溶液的物质的量浓度为1.0mol/L时所得溶液不可能有氢氧化钠,烧瓶也没有充满.
 查看习题详情和答案>>
查看习题详情和答案>>
 以下是某实验小组用CO2和NaOH溶液做喷泉实验的装置和测得的一组数据
以下是某实验小组用CO2和NaOH溶液做喷泉实验的装置和测得的一组数据
| NaOH浓度(mol/L) | 0 | 0.4 | 0.5 | 0.8 | 1.0 | 1.4 | 1.6 | 1.8 |
| 现象 | 不能 形成 | 一段 液柱 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 | 形成喷泉 |
| 时间 | 6min | 1min | 35s | 10s | 6s | 6s | ||
| 烧瓶中水的体积(mL) | 7 | 41 | 71 | 125 | 240 | 240 |
A.CO2在水中的溶解度小,不宜用水直接吸收CO2来做喷泉实验
B.在一定的浓度范围内氢氧化钠溶液的浓度越大越易形成喷泉
C.NaOH浓度为1.6mol/L时,CO2还没有全部分被吸收
D.当氢氧化钠溶液的物质的量浓度为1.0mol/L时所得溶液不可能有氢氧化钠,烧瓶也没有充满. 查看习题详情和答案>>
控制变量法是研究化学变化量的重要思想方法.请仔细观察下表中50mL稀盐酸和1g碳酸钙反应的实验数据:
(1)该反应属于
(2)实验5、6表明
(3)根据实验1、3、5可以得出条件对反应速率的影响规律是
(4)从本实验数据中分析,影响化学反应速率的因素还有
查看习题详情和答案>>
| 实验 序号 |
碳酸钙 状态 |
c(HCl)/ mol?l-1 |
溶液温度/℃ | 碳酸钙消失 时间/s | |
| 反应前 | 反应后 | ||||
| 1 | 块状 | 0.5 | 20 | 39 | 400 |
| 2 | 粉末 | 0.5 | 20 | 40 | 60 |
| 3 | 块状 | 0.6 | 20 | 41 | 280 |
| 4 | 粉末 | 0.8 | 20 | 40 | 30 |
| 5 | 块状 | 1.0 | 20 | 40 | 120 |
| 6 | 块状 | 1.0 | 30 | 50 | 40 |
放热
放热
反应(填“吸热”或“放热”),该反应的离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑
CaCO3+2H+=Ca2++H2O+CO2↑
(2)实验5、6表明
温度
温度
对反应速率的影响,说明温度越高
温度越高
,反应速率越快.(3)根据实验1、3、5可以得出条件对反应速率的影响规律是
反应物浓度越大,反应速率越大
反应物浓度越大,反应速率越大
.(4)从本实验数据中分析,影响化学反应速率的因素还有
反应物的接触面积
反应物的接触面积
,能表明这一规律的实验序号是1和2
1和2
.