网址:http://m.1010jiajiao.com/timu_id_441616[举报]
1-5、CCABB 6-10、BCAD、BC 11-15、AC、DCCD 16-20、ADDDD 21、D
22【答案】(14分)
(1)Cu、O
(2)b、c
(3)2Fe3++2I-=2Fe2++I2 S2O82-+2Fe2+=2SO42-+2Fe3+(离子方程式不配平不扣分)
(4)a:稀硫酸、KMnO4溶液
b:稀硫酸浸取炉渣所得溶液能使KMnO4溶液褪色
23【答案】(14分)
(1)①铁屑 ②稀硫酸 ③稀硝酸 ④氢氧化钠 ⑤氢氧化钠
(2)Fe+2H+=Fe2++H2↑ 2Fe3++Fe=3Fe2+
Cu2++Fe=Cu+Fe2+ 2Au3++3Fe=2Au+3Fe2+
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(3)Fe2O3 用作红色涂料 用作制造铜盐的原料
24【答案】(11分)(1)Cu2S (2)Cu2O,Cu2S (3)形成酸雨,会对植物和建筑物造成严重损害 硫酸 硫酸铵 电解池中,粗铜作阳极,精铜作阴极,电解质为硫酸铜溶液。阳极上发生氧化反应,Cu失去电子,使Cu单质变为Cu2+进入溶液中Cu-2e- === Cu2+;阴极上发生还原反应,Cu2+得到电子在阴极上析出Cu单质,Cu2++2e- === Cu,从而达到精制Cu的目的 (5)A D
25【答案】(8分)(1)Cu + H2O2 + H2SO4 == CuSO4 + 2H2O
(2)4Fe2+ + O2 + 4H+ == 4Fe3+ + 2H2O 2Fe3+ + 2I― == 2Fe2+ + I2
(3)10KOH + 3Cl2 + 2Fe(OH)3 == 2K2FeO4 + 6KCl + 8H2O
26【答案】(10分)(1)B 目的是除去空气中的水蒸气,避免反应④发生;D 目的是除去空气中的CO2,避免反应③发生;F 目的是除去空气中的O2,避免反应①发生。
(2)j→h→g→d→c→k→l(或l→k)→a→b(或b→a)
(3)制得的氮化镁将不纯 因为A装置没有排完空气前就加热会让空气中的氧气、CO2、水蒸气等与镁反应
(4)将产物取少量置于试管中,加入适量水,将润湿的红色石蕊试纸置于试管口,如果能够看到润湿的红色石蕊试纸变蓝,则说明产物是氮化镁
27【答案】(11分)(1)3、4、5、6 Fe-2e-=Fe2+(或2Fe-4e-=2Fe2+) O2+4e-+2H2O=4OH-(2)湿度、温度、O2的浓度、电解质存在 (3)电镀、发蓝等表面覆盖层,牺牲阳极的阴极保护法等(其他合理答案也给分)
28【答案】(1)2Fe3++Cu = 2Fe2++Cu2+。 (2)装置图:
 ;正极反应:Fe3++e- = Fe2+(或2Fe3++2e- = 2Fe2+);负极反应:Cu-2e- = Cu2+。 (3)①通入足量氯气将Fe2+氧化成Fe3+;②加入CuO调节溶液的pH至3.2~4.7;③过滤[除去Fe(OH)3]。 (4)CuO+H2SO4 = CuSO4+H2O、 CuSO4+Fe = FeSO4+Cu;不锈钢表面有紫红色物质生成。
;正极反应:Fe3++e- = Fe2+(或2Fe3++2e- = 2Fe2+);负极反应:Cu-2e- = Cu2+。 (3)①通入足量氯气将Fe2+氧化成Fe3+;②加入CuO调节溶液的pH至3.2~4.7;③过滤[除去Fe(OH)3]。 (4)CuO+H2SO4 = CuSO4+H2O、 CuSO4+Fe = FeSO4+Cu;不锈钢表面有紫红色物质生成。
29【答案】(1)2Al+6H+ = 2Al3++3H2↑或2Al+3Cu2+ = 2Al3++3Cu;
2Cu+O2+H2O+CO2 = Cu2(OH)2CO3。
(2)白色沉淀生成,后沉淀逐渐溶解至消失。
Al3++3OH- = Al(OH)3↓,
Al(OH)3+OH- = AlO2- +2H2O。
(3)①3MnO2+4Al 3Mn+2Al2O3。
3Mn+2Al2O3。
②MnO2+H2O2+2H+ = Mn2++O2↑+2H2O。
 (2011?黄山模拟)如图是各种不同密度的硝酸与铁反应(相同温度)时主要还原产物的分布图.请认真读图分析,回答有关问题.
(2011?黄山模拟)如图是各种不同密度的硝酸与铁反应(相同温度)时主要还原产物的分布图.请认真读图分析,回答有关问题.(1)下列叙述中正确的是(填序号)
A.图中横坐标是硝酸的密度,硝酸的密度越大,其浓度越大
B.当还原剂和温度相同时,不同浓度的硝酸被还原的产物不是单一的,只是在某浓度时,以某种产物为主而已
C.硝酸的浓度越大,还原产物中N元素低化合价产物越多
D.当硝酸密度大于1.3g?cm-3时,还原产物主要为NO、NO2
(2)当硝酸溶液的密度为1.36g?cm-3时,下列化学方程式中,能较准确表达Fe与过量硝酸反应的是(填序号)
A.2Fe+10HNO3═2Fe(NO3)3+NO↑+3NO2↑+5H2O
B.4Fe+18HNO3═4Fe(NO3)3+3NO↑+3NO2↑+9H2O
C.3Fe+12HNO3═2Fe(NO3)3+Fe(NO3)2+2NO↑+2NO2↑+3H2O
(3)密度为1.26g?cm-3,质量分数为50.0%的硝酸,其物质的量浓度是
(4)限用下列仪器、药品验证由铁和过量1.36g?cm-3硝酸反应产生的气体中含有NO(不考虑N2O4).设计一个合理而简单的实验方案(仪器可选择使用,N2的用量可自由控制,加热装置和固定装置省略).

第1步:反应并收集生成的气体:
①实验中气体发生装置应选择
②装置的连接顺序是(填各装置接口的序号):[
③检查装置气密性后,开始反应.待E中充满红棕色气体,停止实验.
第2步:验证E中有NO.
④取下试管E,倒立在F中,轻轻摇动试管,
确认生成的气体中有NO的现象是
火柴是人们常用的生活用品,某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S等物质,设计了以下系列实验,并回答下列各题。
Ⅰ、火柴头中硫元素的实验证明

A B
⑴设计装置A中可观察到 的实验现象,即可证明火柴头上含有S元素。
⑵甲同学认为B装置中除了可选用稀高锰酸钾外还可选用:品红溶液、紫色石蕊溶液、滴有酚酞的NaOH溶液、溴水等,经大家分析后淘汰了紫色石蕊溶液和滴有酚酞的NaOH 溶液。你认为淘汰的原因可能是 。甲同学还认为在A装置中选用浓的高锰酸 钾酸性溶液更好,因为浓度越大反应速率越快,你认为对吗? (先判断再说明 原因)。
Ⅱ、火柴头中含有Cl元素的证明,设计了以下实验流程图:
⑴为验证火柴头中含有Cl元素的实验步骤是:取滤液C……请回答后续实验步骤 是 。
⑵有学生提出检验火柴头上KClO3另一套实验方案:
|
实验中发生的反应是 KClO3 + 3NaNO2 + AgNO3 = AgCl↓+3NaNO3 + KNO3,其中NaNO2 是 。剂,有人提出上述方法中出现白色沉淀并不能充分说明火柴头上 KClO3的存在,其理由是 。
Ⅲ、测定火柴头中KClO3的含量,设计了以下实验流程图:
⑴步骤②的实验操作装置如下图所示,仪器a的名称为 ,装置B的作用是 。
 则当抽滤完毕或中途停止抽滤时,最佳的正确操作是 。
则当抽滤完毕或中途停止抽滤时,最佳的正确操作是 。
⑵得到的沉淀常用95%的酒精洗涤再抽滤,试问用酒精洗涤的原因 。(3)实验测 得火柴头中KClO3的质量分数为 ;未洗涤沉淀,测得KClO3的质量分数将 (填 “偏大”、“偏小”、或“无影响”,下同)。
查看习题详情和答案>>
火柴是人们常用的生活用品,某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S等物质,设计了以下系列实验,并回答下列各题。
Ⅰ、火柴头中硫元素的实验证明
A B
⑴设计装置A中可观察到 的实验现象,即可证明火柴头上含有S元素。
⑵甲同学认为B装置中除了可选用稀高锰酸钾外还可选用:品红溶液、紫色石蕊溶液、滴有酚酞的NaOH溶液、溴水等,经大家分析后淘汰了紫色石蕊溶液和滴有酚酞的NaOH 溶液。你认为淘汰的原因可能是 。甲同学还认为在A装置中选用浓的高锰酸钾酸性溶液更好,因为浓度越大反应速率越快,你认为对吗? (先判断再说明原因)。
Ⅱ、火柴头中含有Cl元素的证明,设计了以下实验流程图:
⑴为验证火柴头中含有Cl元素的实验步骤是:取滤液C……请回答后续实验步骤 是 。
⑵有学生提出检验火柴头上KClO3另一套实验方案:
|
|

⑴步骤②的实验操作装置如下图所示,仪器a的名称为 ,装置B的作用是 。
则当抽滤完毕或中途停止抽滤时,最佳的正确操作是 。
⑵得到的沉淀常用95%的酒精洗涤再抽滤,试问用酒精洗涤的原因 。(3)实验测 得火柴头中KClO3的质量分数为 ;未洗涤沉淀,测得KClO3的质量分数将 (填 “偏大”、“偏小”、或“无影响”,下同)。 查看习题详情和答案>>
火柴是人们常用的生活用品,某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S等物质,设计了以下系列实验,并回答下列各题。
Ⅰ、火柴头中硫元素的实验证明

A B
⑴设计装置A中可观察到 的实验现象,即可证明火柴头上含有S元素。
⑵甲同学认为B装置中除了可选用稀高锰酸钾外还可选用:品红溶液、紫色石蕊溶液、滴有酚酞的NaOH溶液、溴水等,经大家分析后淘汰了紫色石蕊溶液和滴有酚酞的NaOH 溶液。你认为淘汰的原因可能是 。甲同学还认为在A装置中选用浓的高锰酸 钾酸性溶液更好,因为浓度越大反应速率越快,你认为对吗? (先判断再说明 原因)。
Ⅱ、火柴头中含有Cl元素的证明,设计了以下实验流程图:

⑴为验证火柴头中含有Cl元素的实验步骤是:取滤液C……请回答后续实验步骤 是 。
⑵有学生提出检验火柴头上KClO3另一套实验方案:
|
实验中发生的反应是 KClO3 + 3NaNO2 + AgNO3 = AgCl↓+ 3NaNO3 + KNO3,其中NaNO2 是 。剂,有人提出上述方法中出现白色沉淀并不能充分说明火柴头上 KClO3的存在,其理由是 。
Ⅲ、测定火柴头中KClO3的含量,设计了以下实验流程图:

⑴步骤②的实验操作装置如下图所示,仪器a的名称为 ,装置B的作用是 。
 则当抽滤完毕或中途停止抽滤时,最佳的正确操作是
。
则当抽滤完毕或中途停止抽滤时,最佳的正确操作是
。
⑵得到的沉淀常用95%的酒精洗涤再抽滤,试问用酒精洗涤的原因 。(3)实验测 得火柴头中KClO3的质量分数为 ;未洗涤沉淀,测得KClO3的质量分数将 (填 “偏大”、“偏小”、或“无影响”,下同)。
查看习题详情和答案>>
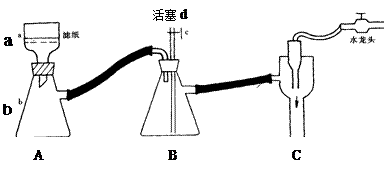
Ⅰ、火柴头中硫元素的实验证明
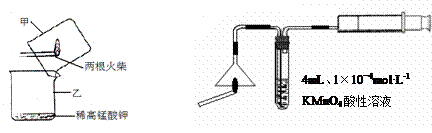
A B
⑴设计装置A中可观察到 的实验现象,即可证明火柴头上含有S元素。
⑵甲同学认为B装置中除了可选用稀高锰酸钾外还可选用:品红溶液、紫色石蕊溶液、滴有酚酞的NaOH溶液、溴水等,经大家分析后淘汰了紫色石蕊溶液和滴有酚酞的NaOH 溶液。你认为淘汰的原因可能是 。甲同学还认为在A装置中选用浓的高锰酸钾酸性溶液更好,因为浓度越大反应速率越快,你认为对吗? (先判断再说明原因)。
Ⅱ、火柴头中含有Cl元素的证明,设计了以下实验流程图:

⑴为验证火柴头中含有Cl元素的实验步骤是:取滤液C……请回答后续实验步骤 是 。
⑵有学生提出检验火柴头上KClO3另一套实验方案:
|
|
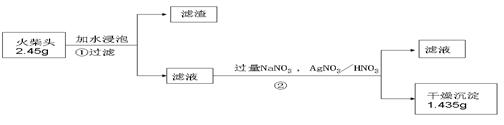
⑴步骤②的实验操作装置如下图所示,仪器a的名称为 ,装置B的作用是 。
则当抽滤完毕或中途停止抽滤时,最佳的正确操作是 。
⑵得到的沉淀常用95%的酒精洗涤再抽滤,试问用酒精洗涤的原因 。(3)实验测 得火柴头中KClO3的质量分数为 ;未洗涤沉淀,测得KClO3的质量分数将 (填 “偏大”、“偏小”、或“无影响”,下同)。


