摘要:(7) 溶质的物质的量浓度(CB)=溶质的物质的量.在单位体积的98%()硫酸中所含溶质――硫酸的质量是不变的.但由(6)中所述可知.其物质的量(n)变成了原来的一半.故物质的量浓度变为原来的0.5倍,(8) 不论作为相对原子质量的标准如何变化.单个CO2分子的质量并未变化.故一定质量的CO2所含的分子个数是不会发生变化的.
网址:http://m.1010jiajiao.com/timu_id_441199[举报]
等体积等物质的量浓度的NaHCO3溶液和Ba(OH)2溶液混合,离子方程式正确的是( )
A.HCO3-+OH-→H2O+C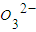
B.2HCO3-+Ba(OH)2→BaCO3↓+2H2O+C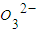
C.HCO3-+Ba2++OH-→H2O+BaCO3↓
D.2HCO3-+Ba2++2OH-→BaCO3↓+2H2O+C
查看习题详情和答案>>
A.HCO3-+OH-→H2O+C
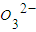
B.2HCO3-+Ba(OH)2→BaCO3↓+2H2O+C
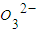
C.HCO3-+Ba2++OH-→H2O+BaCO3↓
D.2HCO3-+Ba2++2OH-→BaCO3↓+2H2O+C

查看习题详情和答案>>
等体积等物质的量浓度的NaHCO3溶液和Ba(OH)2溶液混合,离子方程式正确的是
- A.HCO3-+OH-→H2O+C
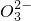
- B.2HCO3-+Ba(OH)2→BaCO3↓+2H2O+C
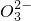
- C.HCO3-+Ba2++OH-→H2O+BaCO3↓
- D.2HCO3-+Ba2++2OH-→BaCO3↓+2H2O+C
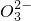
(1)醋酸是一种常见的弱酸,为了证明醋酸是弱电解质,某校研究性学习小组开展了题为“醋酸是弱电解质的实验研究”的探究活动.该校研究性学习小组设计了如下方案:
A.先配制一定量的0.10mol/L CH3COOH溶液,然后测溶液的pH,若pH大于1,则可证明醋酸为弱电解质
B.先测0.10mol/L CH3COOH溶液的pH,然后将其加热至40℃,再测pH,如果pH变小,则可证明醋酸为弱电解质
C.先配制一定量0.01mol/L和0.10mol/L的CH3COOH溶液,分别测它们的pH,若两者的pH相差小于1个单位,则可证明醋酸为弱电解质
D.在常温下,配制一定量的CH3COONa溶液,测其pH,若pH大于7,则可证明醋酸为弱电解质.
你认为上述方案可行的是
(2)一定温度下,有a、盐酸;b、硫酸;c、醋酸三种酸的稀溶液.(用a、b、c、<、=、>号填写)
①当其物质的量浓度相同时,c(H+)由大到小的顺序是
②同体积同物质的量浓度的三种酸,中和同物质的量浓度的NaOH消耗的体积由大到小的顺序是
③当c(H+)相同、体积相同时,分别加入足量锌,相同状况产生的气体体积由大到小的顺序
④将c(H+)相同的三种酸均稀释10倍,pH由大到小的顺序为
(3)某温度(t℃)时,KW=10-13,将此温度下pH=1的硫酸溶液aL与pH=12的氢氧化钡溶液bL混合.
①若所得混合液为中性,则a:b=
②若所得混合液的pH=2,则a:b=
查看习题详情和答案>>
A.先配制一定量的0.10mol/L CH3COOH溶液,然后测溶液的pH,若pH大于1,则可证明醋酸为弱电解质
B.先测0.10mol/L CH3COOH溶液的pH,然后将其加热至40℃,再测pH,如果pH变小,则可证明醋酸为弱电解质
C.先配制一定量0.01mol/L和0.10mol/L的CH3COOH溶液,分别测它们的pH,若两者的pH相差小于1个单位,则可证明醋酸为弱电解质
D.在常温下,配制一定量的CH3COONa溶液,测其pH,若pH大于7,则可证明醋酸为弱电解质.
你认为上述方案可行的是
ABCD
ABCD
.(2)一定温度下,有a、盐酸;b、硫酸;c、醋酸三种酸的稀溶液.(用a、b、c、<、=、>号填写)
①当其物质的量浓度相同时,c(H+)由大到小的顺序是
b>a>c
b>a>c
,②同体积同物质的量浓度的三种酸,中和同物质的量浓度的NaOH消耗的体积由大到小的顺序是
b>a=c
b>a=c
③当c(H+)相同、体积相同时,分别加入足量锌,相同状况产生的气体体积由大到小的顺序
c>a=c
c>a=c
④将c(H+)相同的三种酸均稀释10倍,pH由大到小的顺序为
=b>c
=b>c
(3)某温度(t℃)时,KW=10-13,将此温度下pH=1的硫酸溶液aL与pH=12的氢氧化钡溶液bL混合.
①若所得混合液为中性,则a:b=
1:1
1:1
.②若所得混合液的pH=2,则a:b=
11:9
11:9
.已知B饱和溶液的①溶液质量m1(g);②溶剂质量m2(g);③溶液体积V(mL);④溶质B的溶解度S(g);⑤溶质B的摩尔质量M(g?mol -1);⑥溶液的密度ρ(g?cm-3),从以上条件的组合中列出计算该饱和溶液的物质的量浓度cB的可用条件和相关的计算式(可以增加也可以不满):
查看习题详情和答案>>
| 组合 | 序号 | 计算式/mol?L-1 | ||||
| A | ①②③⑤ ①②③⑤ |
cB=
cB=
| ||||
| B | ②③⑤⑥ ②③⑤⑥ |
cB=
cB=
| ||||
| C | ①②⑤⑥ ①②⑤⑥ |
| ||||
| D | ②③④⑤ ②③④⑤ |
cB=
cB=
| ||||
| E | ①③④⑤ ①③④⑤ |
cB=
cB=
| ||||
| F | 不填 不填 |
不填 不填 |
已知B饱和溶液的①溶液质量m1(g);②溶剂质量m2(g);③溶液体积V(mL);④溶质B的溶解度S(g);⑤溶质B的摩尔质量M;⑥溶液的密度ρ,从以上条件的组合中列出计算该饱和溶液的物质的量浓度cB的可用条件和相关的计算式(可以增加也可以不满):
查看习题详情和答案>>
| 组合 | 序号 | 计算式/mol?L-1 |
| A | ______ | ______ |
| B | ______ | ______ |
| C | ______ | ______ |
| D | ______ | ______ |
| E | ______ | ______ |
| F | ______ | ______ |
查看习题详情和答案>>