网址:http://m.1010jiajiao.com/timu_id_4400097[举报]
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
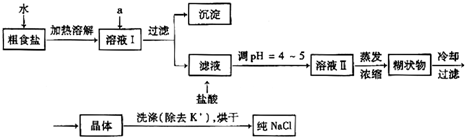
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为
(2)用提纯的NaCl配制500mL4.00mol?L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有
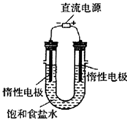
(3)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2
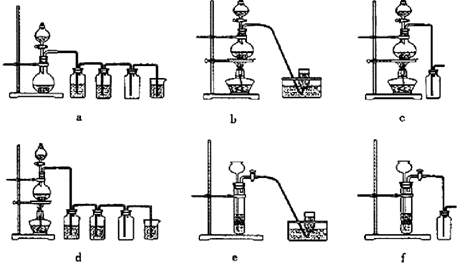
(4)实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4 ZnSO4+H2↑;MnO2+4HCl(浓)
| ||
据此,从下列所给仪器装置中选择制备并收集H2的装置
绿矾晶体(FeSO4·7H2O,M=278g/mol)是治疗缺铁性贫血药品的重要成分。实验室利用硫酸厂的烧渣(主要成分为Fe2O3及少量FeS、SiO2),制备绿矾的过程如下:

试回答:
(1)操作I为 ???????????? (填写操作名称)。
(2)试剂Y与溶液X反应的离子方程式为?????????????????????????????????? 。
(3)操作III的顺序依次为:????????????? 、冷却结晶、过滤、 ????????? 、干燥。
(4)某同学用酸性KMnO4溶液测定绿矾产品中Fe2+含量:
a.称取11.5g绿矾产品,溶解,配制成1000mL溶液;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。①步骤a配制溶液时需要的玻璃仪器除玻璃棒、量筒、烧杯、胶头滴管外,还需???????????????? 。②该同学设计的下列滴定方式,最合理的是?????? (夹持部分略去)(填字母序号)。
③滴定时发生反应的离子方程式为: 。
④判断此滴定实验达到终点的方法是????????????? ;若在滴定终点读取滴定管刻度时,俯视KMnO4溶液液面,其它操作均正确,则使测定结果???????? (填“偏高”“偏低”“无影响”)。
⑤计算上述样品中FeSO4·7H2O的质量分数为???????????????? 。

查看习题详情和答案>>
(14分)绿矾晶体(FeSO4·7H2O,M=278g/mol)是治疗缺铁性贫血药品的重要成分。实验室利用硫酸厂的烧渣(主要成分为Fe2O3及少量FeS、SiO2),制备绿矾的过程如下:

试回答:
(1)操作Ⅰ为 (填写操作名称)。
(2)试剂Y与溶液X反应的离子方程式为 。
(3)操作Ⅲ的顺序依次为: 、冷却结晶、过滤 、 、干燥。
(4)某同学用酸性KMnO4溶液测定绿矾产品中Fe2+含量:
a.称取11.5g绿矾产品,溶解,配制成1000mL溶液;b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①步骤a配制溶液时需要的玻璃仪器除玻璃棒、量筒、烧杯、胶头滴管外,还需
②该同学设计的下列滴定方式,最合理的是 (夹持部分略去)(填字母序号)

③滴定时发生反应的离子方程式为: 。
④判断此滴定实验达到终点的方法是 ;若在滴终点读取滴定管刻度时,俯视KMnO4溶液液面,其它操作均正确,则使测定结果 (填“偏高”“偏低”“无影响”)。
⑤计算上述样品中FeSO4·7H2O的质量分数为
查看习题详情和答案>>
利用某炉渣 (只含Fe2O3、FeO、SiO2、Al2O3)可制备新型净水剂碱式氯化铝[Al2(OH)nCl6-n] 和Fe2O3。工艺流程如下:
①用3.00mol/L的盐酸稀盐酸浸取炉渣,过滤.
②滤液先用H2O2氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3
③将第②步分离出沉淀的滤液通CO2调pH值后,保持温度在90~100℃进行“蒸发浓缩”,可以得到碱式氯化铝[Al2(OH)nCl6-n]
据以上信息回答下列问题:
(1)实验室配制3.00mol/L的盐酸100mL需要36.5%的浓盐酸(密度为1.2g/cm3) _____mL,配制用到的仪器有烧杯、玻璃棒、量筒、胶头滴管、 。
(2)写出H2O2与滤液反应的化学方程式
(3) “蒸发浓缩”需保持温度在90~100℃,可采用的加热方法是
(4)为验证炉渣中含有Fe2O3,做如下实验:
a取适量炉渣于烧杯中,加足量 溶解、静置
b取上层清液少量于试管中,滴加 ,观察现象。选用提供的试剂,
提供的试剂:①稀硝酸 ②稀硫酸 ③氯水 ④KMnO4溶液 ⑤ KSCN溶液
步骤a、b中所加试剂分别为 ;
步骤b中反应的离子方程式:
查看习题详情和答案>>
利用某炉渣(只含Fe2O3、FeO、SiO2、Al2O3)可制备新型净水剂碱式氯化铝[Al2(OH)nCl6-n] 和Fe2O3。工艺流程如下:
①用3.00mol/L的盐酸稀盐酸 浸取炉渣,过滤.
浸取炉渣,过滤.
②滤液先用H2O2氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3
③将第②步分离出沉淀的滤液通CO2调pH值后,保持温度在90~100℃进行“蒸发浓缩”,可以得到碱式氯化铝[Al2(OH)nCl6-n]
据以上信息回 答下列问题:
答下列问题:
(1)实验室配制3.00mol/L的盐酸100mL需要36.5%的浓盐酸(密度为1.2g/cm 3) _____mL,配制用到的仪器有烧杯、玻璃棒、量筒、胶头滴管、 。
3) _____mL,配制用到的仪器有烧杯、玻璃棒、量筒、胶头滴管、 。
(2)写出H2O2与滤液反应的化学方程式
(3) “蒸发浓缩”需保持温度在90~100℃,可采用的加热方法是
(4)为验证炉渣中含有Fe2O3,做如下实验:
a取适量炉渣于烧杯中,加足量 溶解、静置
b取上层清液少量于试管中,滴加 ,观察现象。选用提供的试剂,
提供的试剂:①稀硝酸 ②稀硫酸 ③氯水 ④ KMnO4溶液 ⑤ KSCN溶液
KMnO4溶液 ⑤ KSCN溶液
步骤a、b中所加试剂分别为 ;
步骤b中反应的离子方程式: