摘要:该部分知识点主要体现在阿伏伽德罗常数的计算上.也涉及阿伏伽德罗定律及其推论.其他如一定物质的量浓度的计算.物质的量应用于化学方程式的计算往往穿插于大题之中.复习时要引起重视. [典例精析]1.用NA表示阿伏伽德罗常数的值.下列叙述正确的是: A.25℃时.pH=13的1.0LBa(OH)2溶液中含有的数目为0.2NA B.标准状况下.2.24LCl2与过量的稀NaOH 溶液反应.转移电子总数为0.2NA C.室温下.21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA D.标准状况下.22.4L甲醇中含有的氧原子数为1.0NA [解析]pH=13.则c(OH-)=0.1mol·L-1.n()=0.1mol.则N(OH-)=0.1NA.A错误,Cl2与NaOH 反应时.每摩Cl2转移1mol电子.所以2.24LCl2应转移0.1mol.B错误, 标况下.22.4L甲醇的物质的量远大于1mol.所以D错误, [答案]C21世纪教育网 [考点分析]以阿伏伽德罗常数的计算为背景考查:溶液中微粒数.氧化还原反应中转移的电子数.混合物中原子数.以及气体摩尔体积的应用21世纪教育网
网址:http://m.1010jiajiao.com/timu_id_4394712[举报]
(2013?重庆一模)为测定该补血剂样品[主要成分是硫酸亚铁晶体(FeSO4?7H2O)]中铁元素的含量,某化学兴趣小组设计了两套实验方案:
方案一:用酸性KMnO4溶液滴定测定铁元素的含量
(1)写出滴定反应的离子方程式
(2)下列滴定方式中,最合理的是

(3)实验前,首先要准确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
方案二 将FeSO4转化为Fe2O3,测定质量变化操作流程如下:

(4)步骤②中除用H2O2外还可以使用的物质是
(5)步骤②是否可以省略
(6)步骤④中一系列操作依次是:过滤、洗涤、
(7)假设实验无损耗,则每片补血剂含铁元素的质量
查看习题详情和答案>>
方案一:用酸性KMnO4溶液滴定测定铁元素的含量
(1)写出滴定反应的离子方程式
5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O
5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O
.(2)下列滴定方式中,最合理的是
B
B
(夹持部分略去)(填字母序号).
(3)实验前,首先要准确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
250ml容量瓶
250ml容量瓶
(填仪器名称).方案二 将FeSO4转化为Fe2O3,测定质量变化操作流程如下:

(4)步骤②中除用H2O2外还可以使用的物质是
氯水
氯水
.(5)步骤②是否可以省略
否
否
,理由是Fe2+与碱反应后不能保证Fe2+全部转化为Fe3+,加热不能得到纯净的Fe2O3,故无法准确计算Fe的含量
Fe2+与碱反应后不能保证Fe2+全部转化为Fe3+,加热不能得到纯净的Fe2O3,故无法准确计算Fe的含量
.(6)步骤④中一系列操作依次是:过滤、洗涤、
灼烧
灼烧
、冷却、称量.(7)假设实验无损耗,则每片补血剂含铁元素的质量
0.07a
0.07a
g(用含a的代数式表示).为测定该补血剂样品[主要成分是硫酸亚铁晶体(FeSO4?7H2O)]中铁元素的含量,某化学兴趣小组设计了两套实验方案:
方案一:用酸性KMnO4溶液滴定测定铁元素的含量
(1)写出滴定反应的离子方程式
(2)下列滴定方式中,最合理的是

(3)实验前,首先要准确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
(4)某同学设计以原电池的形式实现Fe2+至Fe3+的转化,电解质溶液为稀硫酸,请写出负极的电极反应式
方案二 将FeSO4转化为Fe2O3,测定质量变化操作流程如下:

(3)步骤②中除用H2O2外还可以使用的物质是
(5)步骤②是否可以省略
(6)步骤④中一系列操作依次是:过滤、洗涤、
(7)假设实验无损耗,则每片补血剂含铁元素的质量
查看习题详情和答案>>
方案一:用酸性KMnO4溶液滴定测定铁元素的含量
(1)写出滴定反应的离子方程式
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
.(2)下列滴定方式中,最合理的是
B
B
(夹持部分略去)(填字母序号).
(3)实验前,首先要准确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
250mL容量瓶
250mL容量瓶
(填仪器名称).(4)某同学设计以原电池的形式实现Fe2+至Fe3+的转化,电解质溶液为稀硫酸,请写出负极的电极反应式
Fe2+-e-═Fe3+
Fe2+-e-═Fe3+
方案二 将FeSO4转化为Fe2O3,测定质量变化操作流程如下:

(3)步骤②中除用H2O2外还可以使用的物质是
氯水
氯水
.(5)步骤②是否可以省略
不能
不能
,理由是Fe2+与碱反应后不能保证Fe2+全部转化为Fe3+,加热不能得到纯净的Fe2O3,故无法准确计算Fe的含量
Fe2+与碱反应后不能保证Fe2+全部转化为Fe3+,加热不能得到纯净的Fe2O3,故无法准确计算Fe的含量
.(6)步骤④中一系列操作依次是:过滤、洗涤、
灼烧
灼烧
、冷却、称量.(7)假设实验无损耗,则每片补血剂含铁元素的质量
0.07a
0.07a
g(用含a的代数式表示). 下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:
下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:①一般认为H2SO4浓度大于60%,就具有一定的强氧化性,越浓氧化性越强,60%以下的H2SO4主要体现的是酸性,基本上不体现强氧化性.
②温度也影响氧化性,如铜放于冷的浓H2SO4中反应不明显,如果加热就可以观察到明显现象.
③98%的浓H2SO4物质的量浓度为18.4mol/L,密度为1.84g?cm-3,根据以上信息回答:?
(1)如图装置,同学甲先向带支管的试管中放入铜粉和3mL水,然后从分液漏斗中加98%的浓H2SO4 0.5mL,加热至沸腾,该试管中液体没有明显变化,试用数据解释原因
H2SO4溶液的质量分数为23%<60%,其氧化性不强,所以无明显现象
H2SO4溶液的质量分数为23%<60%,其氧化性不强,所以无明显现象
(2)乙同学利用所示装置直接从分液漏斗中再加浓H2SO4 10mL与铜片反应.观察到右边试管中溶液褪色,这是因为
生成具有漂白性的二氧化硫
生成具有漂白性的二氧化硫
;若把品红试液换成硝酸酸化的硝酸钡溶液,产生的现象是由白色沉淀生成
由白色沉淀生成
;在左边试管中观察到的现象除了铜粉变黑色外,还有:①
液体呈浅蓝色
液体呈浅蓝色
,原因是溶液中含有Cu2+
溶液中含有Cu2+
②有白色固体在试管底部析出,原因是
98%浓H2SO4有吸水性,生成无水CuSO4
98%浓H2SO4有吸水性,生成无水CuSO4
;(3)丙同学等乙同学实验结束后,取左试管(内有没反应完的铜)倾出上层清液于试管中来检验剩余的硫酸,他可以选择下列哪些试剂
AD
AD
(填写编号).A.锌粉 B.银粉 C.氯化钡溶液 D.碳酸氢钠溶液.
(2013?资阳二模)为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺.己知:V可形成VO2+、VO2+、VO3-等多种离子;部分含钒物质在水中的溶解性如下表所示:
该工艺的主要流程如下:
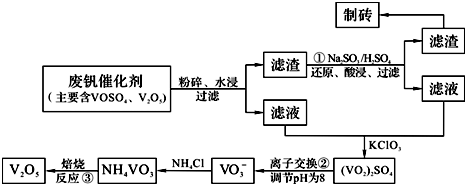
请回答下列问题:
(1)工业上由V2O5冶炼金属钒常用铝热剂法,其反应的化学方程式为
(2)反应①的目的是
(3)若用NaOH溶液调节pH,则转化②的离子方程式为
(4)实验室中实现反应③所需主要仪器除三脚架、泥三角、酒精灯外,必不可少的是
(5)V2O5为硫酸工业接触室中的重要催化剂,其催化反应为2SO2(g)+O2(g)?2SO3(g)△H<0,在容积为2.0L的密闭容器中充入2mol SO2、1mol O2,一定条件下达到平衡,SO3的体积分数为
.
①该条件下反应2SO2(g)+O2(g)?2SO3(g)的平衡常数为
②下列措施能使
增大的是
A.升高温度
B.保持温度和容积不变,再充入2mol He
C.保持温度和容积不变,再充入2mol SO2和1mol O2
D.不用V2O5作催化剂,改用其它更高效催化剂.
查看习题详情和答案>>
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |

请回答下列问题:
(1)工业上由V2O5冶炼金属钒常用铝热剂法,其反应的化学方程式为
3V2O5+10Al
6V+5Al2O3
| ||
3V2O5+10Al
6V+5Al2O3
.
| ||
(2)反应①的目的是
将V2O5转化为可溶的VOSO4
将V2O5转化为可溶的VOSO4
.(3)若用NaOH溶液调节pH,则转化②的离子方程式为
VO2++2OH-=VO3-+H2O
VO2++2OH-=VO3-+H2O
.(4)实验室中实现反应③所需主要仪器除三脚架、泥三角、酒精灯外,必不可少的是
坩埚
坩埚
.(5)V2O5为硫酸工业接触室中的重要催化剂,其催化反应为2SO2(g)+O2(g)?2SO3(g)△H<0,在容积为2.0L的密闭容器中充入2mol SO2、1mol O2,一定条件下达到平衡,SO3的体积分数为
| 6 |
| 7 |
①该条件下反应2SO2(g)+O2(g)?2SO3(g)的平衡常数为
1620
1620
;②下列措施能使
| n(SO3) |
| n(SO2) |
C
C
.A.升高温度
B.保持温度和容积不变,再充入2mol He
C.保持温度和容积不变,再充入2mol SO2和1mol O2
D.不用V2O5作催化剂,改用其它更高效催化剂.
随着材料科学的发展,金属钒被誉为“合金的维生素”.为回收利用含钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺.
己知:V可形成VO2+、VO2+、VO3-等多种离子;部分含钒物质在水中的溶解性如下表所示:
该工艺的主要流程如下:
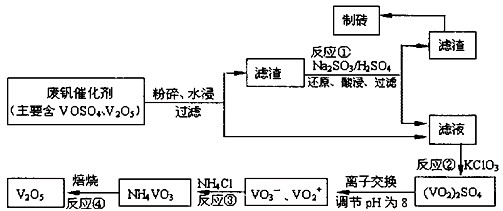
请回答下列问题
(1)工业上常用铝热反应法由V2O5冶炼金属钒,请写出反应的化学方程式 .
(2)反应①的离子方程式是 .
(3)在反应②中,每生成1mol(VO2)2SO4转移电子的数目为 .
(4)在离子交换过程中,发生可逆反应VO2++2OH-?VO3-+H2O.
该反应的化学平衡常数K 的表达式为 .
(5)反应③充分反应后,分离出NH4VO3的实验所需主要玻璃仪器为 ,为保证产品纯度,还应进行的操作名称是 .
查看习题详情和答案>>
己知:V可形成VO2+、VO2+、VO3-等多种离子;部分含钒物质在水中的溶解性如下表所示:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |

请回答下列问题
(1)工业上常用铝热反应法由V2O5冶炼金属钒,请写出反应的化学方程式
(2)反应①的离子方程式是
(3)在反应②中,每生成1mol(VO2)2SO4转移电子的数目为
(4)在离子交换过程中,发生可逆反应VO2++2OH-?VO3-+H2O.
该反应的化学平衡常数K 的表达式为
(5)反应③充分反应后,分离出NH4VO3的实验所需主要玻璃仪器为