网址:http://m.1010jiajiao.com/timu_id_439161[举报]
说明:
1. 本答案供阅卷评分使用,试题的参考解答是用来说明评分标准的,考生如按其他方法或步骤解答,正确的同样给分;有错的,根据错误的性质,参照评分标准中相应的规定评分。
2. 化学专用名词中出现错别字、元素符号有错误,都要参照评分标准扣分。
3. 化学方程式、离子方程式未配平的,都不给分。
4. 计算只有最后答案而无演算过程的,不给分。
第Ⅰ卷(选择题,共50分)
一、选择题(本题包括25小题,每小题2分,共50分。每小题只有一个选项符合题意)
1. A 2. D 3. B 4. A 5. C 6. D 7. C 8. C 9. D 10. D 11. B 12. C 13. B 14. D 15. A 16. D 17. A 18. C 19. A 20. B 21. B 22. D 23. B 24. C 25. A
第Ⅱ卷(非选择题,共50分)
二、(本题包括4小题,共22分)
26.(共4分)3,28,9,1,14(2分) 0.1(2分)
27.(共6分,每空2分)(1)0.01 mol/(L?s) (2)> 乙
 28.(共3分,每空1分)H2-2e-===2H+
H2+2OH--2e-===2H2O
28.(共3分,每空1分)H2-2e-===2H+
H2+2OH--2e-===2H2O
O2+2H2O+4e-===4OH-
29.(共9分,每空1分)(1)AlCl3 Al2O3 Fe
(2)铝热 焊接钢轨,冶炼钒、铬、锰等金属(答出一种即可)
(3)3Fe+4H2O高温====Fe3O4+4H2
(4)① 2Al+2OH-+2H2O===2AlO-2+3H2↑ ② Al3++3AlO-2+6H2O===4Al(OH)3↓
(5)氨水
三、(本题包括2小题,共15分)
30.(共7分)(1)I-、Fe2+、Al3+(3分) HCO-3、NO-3(2分)
(2)4Fe(OH)2+O2+2H2O===4Fe(OH)3(1分)
(3)AlO-2+CO2+2H2O===Al(OH)3↓+HCO-3(1分)
31.(共8分,每空1分)(1)Mg2++2OH-===Mg(OH)2↓(1分)
(2)碱式滴定管、酸式滴定管(1分) (3)酚酞(1分) 酚酞的变色范围最接近中性,滴定终点时,pH为8.2~10,Mg(OH)2不会溶解,不影响测定结果(1分)
(4)偏低(2分) (5)7.5 %(2分)
四、(本题包括2小题,共13分)
32.(共4分)解:n(Cu)==0.09 mol,n(HNO3)=2.0 mol/L×
==
3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O ………………………………(1分)
3 8
=
因为< 所以硝酸过量 ……………………………………(1分)
n(NO)=×n(Cu)=×0.09 mol=0.06 mol ……………………………………(1分)
溶液中n(NO-3)=0.3 mol-0.06 mol=0.24 mol
c(NO-3)==1.6 mol/L ……………………………………………………(1分)
答:溶液中NO-3 的物质的量浓度为1.6 mol/L。
(此题的评分原则是:判断过量2分,算出NO-3 的浓度2分)
 33.(共9分)解:合金溶解于盐酸时所发生的反应有:
33.(共9分)解:合金溶解于盐酸时所发生的反应有:
Mg+2HCl===MgCl2+H2↑,2Al+6HCl===2AlCl3+3H2↑ ………………(1分)
根据图示,加NaOH溶液至130 mL过程中,发生的反应为:
NaOH+HCl===NaCl+H2O MgCl2+2NaOH===Mg(OH)2↓+2NaCl
AlCl3+3NaOH===Al(OH)3↓+3NaCl ………………………………………(1分)
当NaOH溶液由130 mL加至150 mL时,发生的反应为:
Al(OH)3+NaOH===NaAlO2+2H2O …………………………………………(1分)
(1)n(Mg)=n[Mg(OH)2]==0.15 mol ………………………………(1分)
m(Mg)=0.15 mol×
n(Al)=n[Al(OH)3]==0.1 mol ……………………………………(1分)
m(Al)=0.1 mol×
(2)据题意,在加入NaOH溶液130 mL时,溶液中n(Na+)=n(Cl-) …………(1分)
Na+ 全部来自NaOH,Cl- 全部来自盐酸,故n(HCl)=130×10
c(HCl)==6.5 mol/L …………………………………………………(1分)
答:原合金中Al、Mg的质量分别是
(此题的评分原则是:化学方程式或离子方程式共3分,算出铝的质量2分,算出镁的质量2分,算出盐酸的浓度2分。如未写化学方程式或离子方程式,计算结果正确者,镁、铝的质量各3分,盐酸的浓度3分)
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
(1)写出下列物质的化学式:A:
(2)写出下列反应的化学方程式:M→D:
(3)写出下列反应的离子方程式:A→B+C:
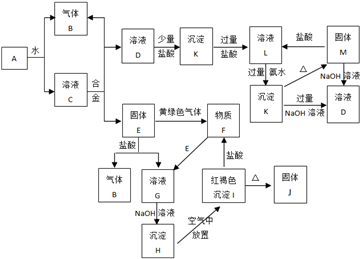

根据上图和实验现象,回答下列问题:(用化学式表示)
(1)A是
(2)写出反应①的化学方程式
(3)写出反应②的离子方程式
Ⅰ:已知31g白磷变为31g红磷释放能量.试回答:
(1)上述变化属于
(2)31g白磷具有的能量_
(3)31g白磷完全燃烧释放的能量_
Ⅱ:A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸
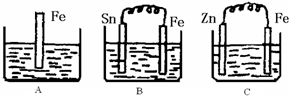
(1)分别写出三个装置中铁片表面发生反应的离子方程式:
A
(2)一段时间后,B中Sn极附近溶液的pH
(3)一段时间后,C中产生了3.36L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度=
(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
Ⅲ:某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
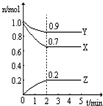
(1)该反应的化学方程式为
 2Z
2Z 2Z
2Z(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时
四种常见元素:A、B、C、D为周期表前四周期元素,原子序数依次递增,它们的性质或结构信息如下表.试根据信息回答有关问题.
| 元素 | A | B | C | D |
| 结构性质 信息 |
基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 | 原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有2对成对的p电子 | 其原子序数比A、B、C三种元素原子的质子数总和还少1,有+1、+2两种常见化合价 |
(2)B元素的氢化物的沸点比同主族相邻元素氢化物沸点
(3)元素F与A相邻且同主族,它们与氧元素的成键情况如下:
| A-O | A=O | F-O | F=O | |
| 键能(KJ/mol) | 360 | 803 | 464 | 640 |
(4)往D元素的硫酸盐溶液中逐滴加入过量B元素的氢化物水溶液,可生成的配合物,该配合物中不含有的化学键是
(5)下列分子结构图中的“
 ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“ ”表示没有形成共价键的最外层电子,短线表示共价键.
”表示没有形成共价键的最外层电子,短线表示共价键.

则在以上分子中,中心原子采用sp3杂化形成化学键的是
(6)已知一种分子B4分子结构如图所示,断裂1molB-B吸收aKJ的热量,生成1molB≡B放出bKJ热量.试计算反应:B4(g)═2B2(g)△H=
