摘要:(2)SO2+C12+2H2O===SO4+2C1+4H,
网址:http://m.1010jiajiao.com/timu_id_438871[举报]
氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用.请回答下列问题:
(1)实验室制取氯气的反应原理为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
①该反应中被还原的元素是
②取一定量的浓盐酸使其与二氧化锰反应,产生的氯气在标准状况下的体积为33.6L,则被氧化的HCl的物质的量为
(2)某同学用下列装置制备并检验Cl2的性质.
下列说法正确的是

a.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
b.Ⅱ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
c.Ⅲ图中:生成蓝色的烟
(3)若氯气罐发生泄漏,当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
a.NaOH b.NaCl c. KOH d. Na2CO3
(4)将SO2和Cl2分别通入装有品红溶液的两个试管中,两溶液的红色均褪去.加热后,有一支试管中的溶液又呈现红色,该试管通入的气体是
查看习题详情和答案>>
(1)实验室制取氯气的反应原理为:MnO2+4HCl(浓)
| ||
①该反应中被还原的元素是
Mn
Mn
,还原剂是HCl
HCl
.②取一定量的浓盐酸使其与二氧化锰反应,产生的氯气在标准状况下的体积为33.6L,则被氧化的HCl的物质的量为
3mol
3mol
,反应中转移电子数为3NA或1.806×1024
3NA或1.806×1024
.(2)某同学用下列装置制备并检验Cl2的性质.
下列说法正确的是
b
b

a.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
b.Ⅱ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
c.Ⅲ图中:生成蓝色的烟
(3)若氯气罐发生泄漏,当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
d
d
.a.NaOH b.NaCl c. KOH d. Na2CO3
(4)将SO2和Cl2分别通入装有品红溶液的两个试管中,两溶液的红色均褪去.加热后,有一支试管中的溶液又呈现红色,该试管通入的气体是
SO2
SO2
.将SO2和Cl2按1:1体积比(同温同压)混合后通入品红溶液中,溶液不褪色.为检验两种气体在溶液中是否发生了氧化还原反应,应向所得溶液加入的试剂是BaCl2
BaCl2
(填化学式).经实验证明,SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是SO2+C12+2H2O=4H++SO42-+2Cl-
SO2+C12+2H2O=4H++SO42-+2Cl-
.(2007?天津)二氯化二硫(S2C12)在工业上用于橡胶的硫化.为在实验室合成S2C12,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2C12粗品.
②有关物质的部分性质如下表:
设计实验装置图如下:

(1)图中气体发生和尾气处理装置不够完善,请你提出改进意见
利用改进后的正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式:
(3)C、D中的试剂分别是
(4)仪器A、B的名称分别是
(5)如果在加热E时温度过高,对实验结果的影响是
(6)S2C12粗品中可能混有的杂质是(填写两种)
查看习题详情和答案>>
①将干燥的氯气在110℃~140℃与硫反应,即可得S2C12粗品.
②有关物质的部分性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 化学性质 | ||||
| S | 112.8 | 444.6 | 略 | ||||
| S2C12 | -77 | 137 | 遇水生成HCl、SO2、S; 300℃以上完全分解; S2C12+C12
|

(1)图中气体发生和尾气处理装置不够完善,请你提出改进意见
用导管将A的上口和B相连(或将A换成恒压滴液漏斗),在G和H之间增加干燥装置
用导管将A的上口和B相连(或将A换成恒压滴液漏斗),在G和H之间增加干燥装置
.利用改进后的正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式:
MnO2+4 H++2 C1-
Mn2++C12↑+2H2O
| ||
MnO2+4 H++2 C1-
Mn2++C12↑+2H2O
;E中反应的化学方程式:
| ||
2 S+C12
S2C12
| ||
2 S+C12
S2C12
.
| ||
(3)C、D中的试剂分别是
饱和食盐水
饱和食盐水
、浓硫酸
浓硫酸
.(4)仪器A、B的名称分别是
分液漏斗
分液漏斗
、蒸馏烧瓶
蒸馏烧瓶
,F的作用是导气、冷凝
导气、冷凝
.(5)如果在加热E时温度过高,对实验结果的影响是
产率降低
产率降低
,在F中可能出现的现象是有固体产生
有固体产生
.(6)S2C12粗品中可能混有的杂质是(填写两种)
SCl2
SCl2
、、C12
、C12
,为了提高S2C12的纯度,关键的操作是控制好温度和控制浓盐酸的滴速不要过快
控制浓盐酸的滴速不要过快
.(1)将SO2和Cl2分别通入装有品红溶液的两个试管中,两溶液的红色均褪去.加热后,有一支试管中的溶液又呈现红色,该试管通入的气体是
(2)将SO2和Cl2按1:1体积比(同温同压)混合后通入品红溶液中,溶液不褪色.为检验两种气体在溶液中是否发生了氧化还原反应,应向所得溶液加入的试剂是
查看习题详情和答案>>
SO2
SO2
,该实验说明的问题是SO2与有色物质结合成的无色物质不稳定
SO2与有色物质结合成的无色物质不稳定
.(2)将SO2和Cl2按1:1体积比(同温同压)混合后通入品红溶液中,溶液不褪色.为检验两种气体在溶液中是否发生了氧化还原反应,应向所得溶液加入的试剂是
氯化钡溶液
氯化钡溶液
(填化学式).经实验证明,SO2和Cl2在溶液中发生了氧化还原反应,且SO2被氧化,该反应的离子方程式是SO2+C12+2H2O=4H++SO42-+2Cl-
SO2+C12+2H2O=4H++SO42-+2Cl-
.(2008?枣庄一模)现有A、B、C、D、F六种短周期元素,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构.
已知:①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的单质以溶于NaOH溶液,向生成的溶液中通入CO2气体有白色沉淀生成;
③C的氢化物分子G是具有10电子微粒,且以发生下列转化:G
P
Q
M+P;
④E和D是同一主族的元素,二者能形成微粒的个数比为1:2和1:3的化合物T和K;
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y.
请回答下列问题:
(1)B元素的名称是
(2)E元素的原子结构示意图是
 .
.
(3)请将A、C的元素符号填在如图所示部分元素周期表的适当位置上.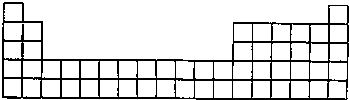
(4)G的电子式为
 .化合物X所含化学键类型有
.化合物X所含化学键类型有
(5)T与F单质的水溶液反应的离子方程式为
查看习题详情和答案>>
已知:①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的单质以溶于NaOH溶液,向生成的溶液中通入CO2气体有白色沉淀生成;
③C的氢化物分子G是具有10电子微粒,且以发生下列转化:G
| D的单质 |
| D的单质 |
| H2O |
④E和D是同一主族的元素,二者能形成微粒的个数比为1:2和1:3的化合物T和K;
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y.
请回答下列问题:
(1)B元素的名称是
钠
钠
;(2)E元素的原子结构示意图是


(3)请将A、C的元素符号填在如图所示部分元素周期表的适当位置上.

(4)G的电子式为


离子键、共价键
离子键、共价键
.(5)T与F单质的水溶液反应的离子方程式为
SO2+C12+2H2O=4H++SO42-+2C1-
SO2+C12+2H2O=4H++SO42-+2C1-
;G与D的单质反应的化学方程式为4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;M与铜反应的化学方程式为
| ||
| △ |
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O或Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O或Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
.W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素,由Y元素组成的单质通常呈淡黄色.
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为
(2)写出X 的最高价氧化物的一种用途
(3)X的硝酸盐水溶液显
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为:
(5)比较Y、Z气态氢化物的稳定性
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是:
查看习题详情和答案>>
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为
Al(OH)3+OH-═AlO2-+2H2O
Al(OH)3+OH-═AlO2-+2H2O
.(2)写出X 的最高价氧化物的一种用途
冶炼铝(或制造耐火材料等)
冶炼铝(或制造耐火材料等)
.(3)X的硝酸盐水溶液显
酸
酸
性,该溶液中各离子浓度由大到小的顺序为:c(NO3-)>c(A13+)>c(H+)>c(OH-)
c(NO3-)>c(A13+)>c(H+)>c(OH-)
.(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为:
SO2+C12+2H2O═H2SO4+2HCl
SO2+C12+2H2O═H2SO4+2HCl
.(5)比较Y、Z气态氢化物的稳定性
HCl
HCl
>H2S
H2S
(用分子式表示).(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是:
S2-
S2-
>Cl-
Cl-
>Na+
Na+
>Al3+
Al3+
.