摘要:21·下列物质中:①NaHC03②NH4C1③CH3COONH4 ④C6H50H⑤C6H5ONa⑥H2N-CH(CH3)-COONa ⑦H2N-CH2-COOH⑧HOOC--CH(CH3)-NH2·HC1其中只能与盐酸反应的是 .只能与NaOH溶液反应的是: .既能与盐酸反应又能与NaOH溶液反应的是 .22.丙氨酸在强酸性溶液中以阳离子存在.在强碱性溶液中.以阴离子形式存在.在pH=6时.以两性离子存在.丙氨酸在水溶液中存在下列关系: CH3-CH-COOH CH3-CH-COO- CH3-CH-COO- NH3+ NH3+ NH2 现在以Pt电极在下列介质中电解丙氨酸的水溶液: (1)在强酸性溶液中.在 极.析出丙氨酸. (2)在强碱性溶液中.在 极.析出丙氨酸. (3)在pH=6时.阳极的电极反应式是 .
网址:http://m.1010jiajiao.com/timu_id_4387732[举报]
维生素C(又名抗坏血酸,分子式为C6H8O6)是动物维持生长、繁殖和保证健康所必需的营养物质,主要用于补充血液中Vc不足,预防Vc缺少症,提高动物免疫力和抗应激能力。小剂量Vc可以预防和治疗坏血病,大剂量Vc可以提高动物在疾病、逆境和生理应激等情况下的抵抗能力。
(1)取a g某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了a g。下列物质中不能满足上述结果的是( )
A.H2 B.HCHO C.C12H22O11 D.维生素C
(2)Vc极不稳定,具有较强的还原性,放置在空气中易被氧化,其含量可通过在弱酸性溶液中用已知浓度的I2溶液进行滴定。该反应的化学方程式如下:
C6H8O6+I2====C6H6O6+2HI
现欲测定某样品中维生素C的含量,具体的步骤及测得的数据如下:取10 mL 6 mol·L-1 CH3COOH,加入100 mL蒸馏水,将溶液加热煮沸后放置冷却。精确称取0.20 g样品,溶解于上述冷却的溶液中。加入1 mL淀粉指示剂,立即用浓度为0.05 mol·L-1的I2溶液进行滴定,直至溶液中的蓝色持续不褪为止,共消耗21.00 mL I2溶液。
①为何加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用?
②计算样品中维生素C的质量分数。
查看习题详情和答案>>光健康、太阳能、绿色节能、零排放等高科技点亮2010上海世博。
(1)世博园区外围设置生态化停车场,有害尾气被纳米光触媒涂料分解为无毒物质,汽车尾气中下列物质中属于由极性键构成的非极性分子为____。
A.CO2 B.NO C.NO2 D.CO
(2)“一轴四馆”中安装了高亮度节能的陶瓷金卤灯,金卤灯中填充物通常包含Na、81Tl、49In、Sc、I等元素的单质及化合物。有关说法正确的是____。
A.第ⅢA元素铊和铟,第一电离能T1大于In
B.元素Sc位于周期表d区
C.钠的熔点低,是因为金属键较弱
D.I2溶于KI溶液,可产生I3-,由价层互斥理论可推知I3-呈直线形
(3)“东方之冠”(中国馆)表面装有7000多块红色铝板,红色铝板为新型氟碳喷涂型材,一种氟碳涂层聚酯(FEP),它的单体为CF3-CF=CF2,该分子中碳原子的杂化方式有____。
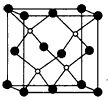
(4)上海城区大规模集中使用“21世纪绿色光源”LED半导体照明,LED晶片采用砷化镓(GaAs)等材料组成。其中As原子在基态时外围电子排布式为:_____。GaAs的晶胞结构如图,晶胞中含镓原子数为____。
(1)世博园区外围设置生态化停车场,有害尾气被纳米光触媒涂料分解为无毒物质,汽车尾气中下列物质中属于由极性键构成的非极性分子为____。
A.CO2 B.NO C.NO2 D.CO
(2)“一轴四馆”中安装了高亮度节能的陶瓷金卤灯,金卤灯中填充物通常包含Na、81Tl、49In、Sc、I等元素的单质及化合物。有关说法正确的是____。
A.第ⅢA元素铊和铟,第一电离能T1大于In
B.元素Sc位于周期表d区
C.钠的熔点低,是因为金属键较弱
D.I2溶于KI溶液,可产生I3-,由价层互斥理论可推知I3-呈直线形
(3)“东方之冠”(中国馆)表面装有7000多块红色铝板,红色铝板为新型氟碳喷涂型材,一种氟碳涂层聚酯(FEP),它的单体为CF3-CF=CF2,该分子中碳原子的杂化方式有____。
(4)上海城区大规模集中使用“21世纪绿色光源”LED半导体照明,LED晶片采用砷化镓(GaAs)等材料组成。其中As原子在基态时外围电子排布式为:_____。GaAs的晶胞结构如图,晶胞中含镓原子数为____。
(5)世博馆广泛采用了冰蓄冷空调。冰蓄冷空调采用液态化合物乙二醇(HOCH2CH2OH)介质,乙二醇沸点高,是由于_______________________。
查看习题详情和答案>>
 A、B、C、D都是中学化学中的常见物质,具有如图所示的转化关系(反应条件,其他反应物及多余产物均已略去):
A、B、C、D都是中学化学中的常见物质,具有如图所示的转化关系(反应条件,其他反应物及多余产物均已略去):(1)若A是一种白色难溶于水的钙盐,由三种元素组成,C是一种参与植物光合作用的气体.按要求写出下列物质化学式或反应式:
B
CaO
CaO
; C+D→A离子方程式:CO2+Ca2++2OH-═CaCO3↓+H2O
CO2+Ca2++2OH-═CaCO3↓+H2O
.(2)若A是一种无色液体,D是一种金属氧化物,其相对分子质量为232,其中金属元素和氧元素的质量比为21:8.按要求写出下列物质化学式或反应式:B
O2
O2
; C+D→A化学方程式:4H2+Fe3O4
4H2O+3Fe
| ||
4H2+Fe3O4
4H2O+3Fe
.
| ||
实验题
(1)某学生的实验报告所列出的下列数据中合理的是
A.用10mL量筒量取7.1mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70mL
E.用浓度分别为0.50mol/L,体积各为50mL盐酸、氢氧化钠溶液测定中和热
(2)用酸式滴定管准确移取25.00mL某未知浓度的盐酸于一洁净的锥形瓶中,然后用0.20mol?L -1的氢氧化钠溶液(指示剂为甲基橙)滴定,滴定结果如下:
①根据以上数据可以计算出盐酸的物质的量浓度为
②判断滴定终点的现象是
③以下操作造成测定结果偏高的原因可能是
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.盛装未知液的锥形瓶用蒸馏水洗后,未用待测液润洗
E.未用标准液润洗碱式滴定管.
查看习题详情和答案>>
(1)某学生的实验报告所列出的下列数据中合理的是
D
D
.A.用10mL量筒量取7.1mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70mL
E.用浓度分别为0.50mol/L,体积各为50mL盐酸、氢氧化钠溶液测定中和热
(2)用酸式滴定管准确移取25.00mL某未知浓度的盐酸于一洁净的锥形瓶中,然后用0.20mol?L -1的氢氧化钠溶液(指示剂为甲基橙)滴定,滴定结果如下:
| NaOH起始读数 | NaOH终点读数 | 第一次 | 0.10mL | 18.40mL | 第二次 | 0.30mL | 18.40mL |
0.1456
0.1456
mol?L-1 (小数点后保留两位有效数字).②判断滴定终点的现象是
无色变粉红色且30s不变色
无色变粉红色且30s不变色
③以下操作造成测定结果偏高的原因可能是
ACE
ACE
(填写序号).A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.盛装未知液的锥形瓶用蒸馏水洗后,未用待测液润洗
E.未用标准液润洗碱式滴定管.
(2013?河池模拟)如图所示物质中,只有X是单质,常温下A和B呈气态,且B是导致酸雨的大气污染物,D是淡黄色固体.B→E和E→Y是工业生产Y中的重要两步反应.
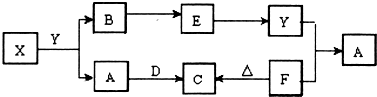
据此回答下列问题:
(1)元素X在元素周期表中位于
(2)物质D的电子式为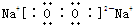
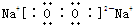 其阴阳离子个数比为
其阴阳离子个数比为
(3)写出X和Y反应的化学方程式
(4)请写出Y和F反应的离子方程式
(5)工业生产中B转化为E使用的设备名称为
查看习题详情和答案>>

据此回答下列问题:
(1)元素X在元素周期表中位于
二
二
周期ⅣA
ⅣA
族.(2)物质D的电子式为
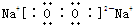
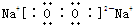
1:2
1:2
.(3)写出X和Y反应的化学方程式
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O
.
| ||
(4)请写出Y和F反应的离子方程式
H++HCO3-=CO2↑+H2O
H++HCO3-=CO2↑+H2O
.(5)工业生产中B转化为E使用的设备名称为
接触室
接触室
,反应的化学方程式为2SO2+O2
2SO3
| ||
| △ |
2SO2+O2
2SO3
.
| ||
| △ |