摘要:D.用NaOH溶液.蒸馏水和红色石蕊试纸检验溶液中是否含有NH4+
网址:http://m.1010jiajiao.com/timu_id_438727[举报]
 某学习小组的学生用标准浓度的氢氧化钠溶液测定未知浓度的盐酸溶液,
某学习小组的学生用标准浓度的氢氧化钠溶液测定未知浓度的盐酸溶液,(1)该学生盛装标准液的仪器和指示剂选用正确的一组是
D
D
.(写编号)| 序号 | 选用指示剂 | 选用滴定管 |
| A | 石蕊 | (乙) |
| B | 甲基橙 | (甲) |
| C | 酚酞 | (甲) |
| D | 酚酞 | (乙) |
e
e
→b
b
→d→c
c
→a
a
→g
g
→f.a.用酸式滴定管取盐酸溶液25.00mL,注入锥形瓶中,加入指示剂.
b.用蒸馏水洗干净滴定管.
c.用待测定的溶液润洗酸式滴定管.
d.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下.
e.检查滴定管是否漏水.
f.另取锥形瓶,再重复操作一次.
g.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度.
(3)若采用(1)选择进行实验,滴定终点为
当滴入最后一滴氢氧化钠溶液后,锥形瓶内最后溶液由无色突变为粉红色,且保持半分钟颜色不发生变化
当滴入最后一滴氢氧化钠溶液后,锥形瓶内最后溶液由无色突变为粉红色,且保持半分钟颜色不发生变化
.(4)已知滴定管中装有浓度为0.1120mol/L的氢氧化钠.逐滴加入到装有盐酸溶液的锥形瓶中.开始时读数及恰好反应时氢氧化钠溶液的读数见表.
实验编号 |
待测盐酸溶液体积(mL) |
滴定开始读数(mL) |
滴定结束读数(mL) |
| ① |
25.00 |
0.00 |
23.80 |
② |
25.00 |
1.00 |
24.78 |
| ③ |
25.00 |
0.22 |
24.04 |
0.1066mol/L
0.1066mol/L
.(5)下面操作会导致待测盐酸的浓度偏大的是
a、d
a、d
(写编号)a.其它操作均正确,滴定终点读数时,仰视滴定管的刻度
b.盛装待测液的锥形瓶用水洗后未用所装待测液润洗
c.盛装待测液的酸式滴定管未用待测液润洗
d.盛装标准液的碱式滴定管未用标准液洗.
下列物质的分离、提纯和鉴别的方法中可行的是(必要时可加热)( )
A.用NaOH溶液,蒸馏水和红色石蕊试纸检验溶液中是否含有![]()
B.用升化法分离碘和氯化铵的混合物
C.以粗铜为阴极,精铜为阳极,CuSO4溶液为电解液,精炼铜
D.用AgNO3溶液和稀盐酸检验溶液中是否含有Cl-
查看习题详情和答案>>下列物质的分离、提纯和鉴别的方法中可行的是(必要时可加热)( )
A.用NaOH溶液,蒸馏水和红色石蕊试纸检验溶液中是否含有![]()
B.用升华法分离碘和氯化铵的混合物
C.以粗铜为阴极,精铜为阳极,CuSO4溶液为电解液,精炼铜
D.用AgNO3溶液和稀盐酸检验溶液中是否含有Cl-
查看习题详情和答案>>下列物质的分离、提纯和鉴别的方法中(必要时可加热),可行的是
- A.以AgNO3溶液和稀盐酸检验溶液中是否含有Cl-
- B.用升华法分离碘和氯化铵的混合物
- C.以粗铜为阴极,精铜为阳极,CuSO4溶液为电解液,精炼铜
- D.用NaOH溶液、蒸馏水和红色石蕊试纸检验溶液中是否含有NH4+
I.(1)指出下列实验用品或仪器(已经洗涤干净)使用时的第一步操作:
①蓝色石蕊试纸(检验气体性质)
②容量瓶
③托盘天平
(2)下列有关化学实验操作中“先”与“后”的说法正确的是
A.用排水法收集气体后,先移出导管,后熄灭酒精灯
B.点燃可燃性气体(如CH4、H2、CO等)时,都要先检验气体纯度,后点燃
C.碱液流到桌子上,先用稀醋酸溶液中和,后用水洗
D.给试管加热时,先均匀加热,后局部加热
II.实验室利用SO2和一定浓度的NaOH溶液反应制备少量NaHSO3.实验装置如图所示:
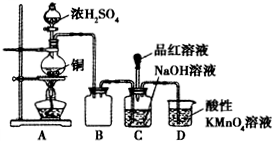
请回答下列问题:
(1)写出圆底烧瓶中发生反应的化学方程式
(2)反应结束后发现烧瓶中还有少量的铜片剩余,有人认为还有一定的硫酸剩余,原因是
(3)装置B的作用是
(4)证明C装置中NaOH溶液全部转化为NaHSO3的实验操作和现象是
查看习题详情和答案>>
①蓝色石蕊试纸(检验气体性质)
用蒸馏水润湿
用蒸馏水润湿
;②容量瓶
检验是否漏水
检验是否漏水
;③托盘天平
游码归零,调节天平平衡
游码归零,调节天平平衡
.(2)下列有关化学实验操作中“先”与“后”的说法正确的是
ABCD
ABCD
(填代号).A.用排水法收集气体后,先移出导管,后熄灭酒精灯
B.点燃可燃性气体(如CH4、H2、CO等)时,都要先检验气体纯度,后点燃
C.碱液流到桌子上,先用稀醋酸溶液中和,后用水洗
D.给试管加热时,先均匀加热,后局部加热
II.实验室利用SO2和一定浓度的NaOH溶液反应制备少量NaHSO3.实验装置如图所示:

请回答下列问题:
(1)写出圆底烧瓶中发生反应的化学方程式
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(2)反应结束后发现烧瓶中还有少量的铜片剩余,有人认为还有一定的硫酸剩余,原因是
随着反应进行,硫酸越来越稀,铜和稀硫酸不反应,所以有硫酸剩余
随着反应进行,硫酸越来越稀,铜和稀硫酸不反应,所以有硫酸剩余
,在不增加硫酸的情况下,要使剩余铜片溶解,可再加入NaNO3、Fe2O3
NaNO3、Fe2O3
固体(填写两种不同类别的物质).(3)装置B的作用是
安全瓶(防止倒吸)
安全瓶(防止倒吸)
,装置D的作用是吸收多余的SO2
吸收多余的SO2
.(4)证明C装置中NaOH溶液全部转化为NaHSO3的实验操作和现象是
把品红溶液滴入C装置反应后的溶液中,若品红溶液褪色,证明NaOH溶液全部转化为NaHSO3
把品红溶液滴入C装置反应后的溶液中,若品红溶液褪色,证明NaOH溶液全部转化为NaHSO3
.