摘要:下列反应硫酸表现氧化性的是A.实验室用浓硫酸干燥氯气.氯化氢等气体 B.将KI与浓硫酸混合.有单质I2产生C.浓硫酸与氧化亚铁反应.会生成硫酸铁 D.用浓硫酸在木制品上“烙 字画
网址:http://m.1010jiajiao.com/timu_id_438351[举报]
实验室利用图④来制乙烯时,常因温度过高而发生副反应.部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑.请用下列编号为①~④的实验装置设计一个实验,以验证上述反应后的混合气中含有二氧化碳、二氧化硫和水蒸气.
(1)装置③中的固体药品为
(2)装置B中的试剂为
A.溴水 B.酸性高锰酸钾溶液 C.NaOH溶液 D.饱和NaHCO3溶液
(3)装置②盛有
(4)用装置的编号表示其连接顺序(按气体产物从左到右的流向) ④→
(5)装置A中的现象是
(6)装置C中的现象是
查看习题详情和答案>>

(1)装置③中的固体药品为
无水硫酸铜
无水硫酸铜
,用以验证的产物是水蒸气
水蒸气
(2)装置B中的试剂为
A
A
(填“A、B、C、D”)A.溴水 B.酸性高锰酸钾溶液 C.NaOH溶液 D.饱和NaHCO3溶液
(3)装置②盛有
澄清石灰水
澄清石灰水
,可以验证CO2
CO2
气体的存在.(4)用装置的编号表示其连接顺序(按气体产物从左到右的流向) ④→
③①②
③①②
;(5)装置A中的现象是
品红褪色
品红褪色
,验证SO2
SO2
;(6)装置C中的现象是
品红不褪色
品红不褪色
说明SO2已被除净.
SO2已被除净.
.实验室可以通过以下三条途径按不同要求制取氮气:
①加热NaNO2(一种致癌物质,有毒)与NH4Cl的混合物浓溶液制取N2;
②将空气通过灼热的活性铜粉制得较纯净的N2;
③加热条件下用NH3还原CuO得纯净的N2和活性铜粉.
如图所示,给出了按上述途径制取N2可供选择的几种实验装置:

请回答下列问题:
(1)按途径①制取N2时,应选用上述装置中的
(2)若只需较纯净的N2,有同学建议把②和③两条途径协同使用,这样做的好处是
(3)按途径③制取N2时,若气流从左到右的顺序所需的上述装置是:A→C→B→D.在A装置中所需要的试剂是
①甲同学:为通过实验现象验证C处有水产生,必须在C装置前后都连接E装置,其中填充的固体药品按前后顺序分别为
②乙同学:实验过程中,发现黑色固体完全变红,质疑此时红色固体可能含Cu2O.通过查阅资料知:Cu2O+2H+=Cu2++Cu+H2O.依据信息,请设计实验证明C处的红色固体中是否含有Cu2O:
③丙同学:实验时充分加热,至C装置硬质玻管质量不再减轻为止.实验完毕后,若实验测得收集的N2体积为aL(已折算为标准状况),硬质玻管质量减轻了bg.则氨分子中氮、氢的原子个数比为(用含a、b的字母的代数式表示)
(此空记3分).
(4)目前工业上用氮气和氢气直接合成氨,氨经一系列反应可制得硝酸.在以上各步反应中,按要求完成化学反应方程式:
①氮元素只发生还原反应
②氮元素既发生氧化反应又发生还原反应:
查看习题详情和答案>>
①加热NaNO2(一种致癌物质,有毒)与NH4Cl的混合物浓溶液制取N2;
②将空气通过灼热的活性铜粉制得较纯净的N2;
③加热条件下用NH3还原CuO得纯净的N2和活性铜粉.
如图所示,给出了按上述途径制取N2可供选择的几种实验装置:

请回答下列问题:
(1)按途径①制取N2时,应选用上述装置中的
F
F
(填装置代码)做发生装置.(2)若只需较纯净的N2,有同学建议把②和③两条途径协同使用,这样做的好处是
铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染)
铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染)
.(3)按途径③制取N2时,若气流从左到右的顺序所需的上述装置是:A→C→B→D.在A装置中所需要的试剂是
浓氨水
浓氨水
和生石灰
生石灰
.(写试剂名称)①甲同学:为通过实验现象验证C处有水产生,必须在C装置前后都连接E装置,其中填充的固体药品按前后顺序分别为
碱石灰(或无水氯化钙)
碱石灰(或无水氯化钙)
、无水硫酸铜
无水硫酸铜
.(写试剂名称)②乙同学:实验过程中,发现黑色固体完全变红,质疑此时红色固体可能含Cu2O.通过查阅资料知:Cu2O+2H+=Cu2++Cu+H2O.依据信息,请设计实验证明C处的红色固体中是否含有Cu2O:
取样加入稀硫酸后溶液呈蓝色,即证明含Cu2O
取样加入稀硫酸后溶液呈蓝色,即证明含Cu2O
③丙同学:实验时充分加热,至C装置硬质玻管质量不再减轻为止.实验完毕后,若实验测得收集的N2体积为aL(已折算为标准状况),硬质玻管质量减轻了bg.则氨分子中氮、氢的原子个数比为(用含a、b的字母的代数式表示)
| 16a |
| 22.4b |
| 16a |
| 22.4b |
(4)目前工业上用氮气和氢气直接合成氨,氨经一系列反应可制得硝酸.在以上各步反应中,按要求完成化学反应方程式:
①氮元素只发生还原反应
N2+3H2
2NH3
| 高温高压 |
| 催化剂 |
N2+3H2
2NH3
、| 高温高压 |
| 催化剂 |
②氮元素既发生氧化反应又发生还原反应:
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
.实验室里可用图1所示装置制取氯酸钾、次氯酸钠和探究氯水的性质. ?
?
图中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液?
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:
图2中符合该晶体溶解度曲线的是
(3)本实验中制取次氯酸钠的离子方程式是
查看习题详情和答案>>
 ?
?图中:①为氯气发生装置;②的试管里盛有15mL 30% KOH溶液,并置于水浴中;③的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过
分液漏斗
分液漏斗
(填写仪器名称)向烧瓶中加入适量的浓盐酸.实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有B
B
(填写下列编号字母)的净化装置.A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液?
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:
碱溶液(或反应物)的浓度不同,反应温度不同?
碱溶液(或反应物)的浓度不同,反应温度不同?
反应完毕经冷却后,②的试管中有大量晶体析出.图2中符合该晶体溶解度曲线的是
M
M
(填写编号字母);冷却后从②的试管中分离出该晶体的方法是过滤
过滤
(填写实验操作名称).(3)本实验中制取次氯酸钠的离子方程式是
Cl2+2OH-═ClO-+Cl-+H2O
Cl2+2OH-═ClO-+Cl-+H2O
,实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | |
| 然后溶液从无色逐渐变为 黄绿 黄绿 色 |
实验室用少量的溴和足量的乙醇制备1,2-二溴乙烷(BrCH2CH2Br).
反应分两步进行:
第一步,乙醇与浓硫酸共热到170℃生成乙烯(CH3CH2OH
CH2=CH2↑+H2O);
第二步,乙烯与溴生成1,2-二溴乙烷(CH2=CH2+Br2→BrCH2CH2Br).
可能存在的副反应有:乙醇在浓硫酸的存在下于l40℃脱水生成乙醚(C2H5-O-C2H5);温度过高,乙醇与浓硫酸反应生成SO2、CO2等酸性气体.
有关数据列表如下:
反应装置如图(略去加热等装置):
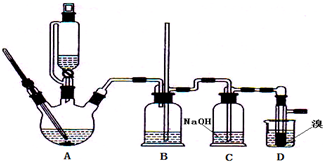
回答下列问题:
(1)熔沸点:乙醇>乙醚.利用物质结构的相关知识解释原因 .
(2)组装好仪器后检查A、B、C装置气密性的操作是 .
(3)如果D中导气管发生堵塞事故,装置B中可能观察到的现象是 .
(4)装置C中可能发生反应的化学方程式是 (写出一个即可).
(5)将1,2-二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在 层(填“上”、“下”);若产物中有少量未反应的Br2,最好用 洗涤除去(填字母).
a.水 b.氢氧化钠溶液 c.乙醇
(6)若产物中有少量副产物乙醚,可采用的除杂方法是 .
(7)反应时装置D的烧杯中应装 (填“a”或“b”),不装另一种的原因是 .
a.冷水 b.冰水. 查看习题详情和答案>>
反应分两步进行:
第一步,乙醇与浓硫酸共热到170℃生成乙烯(CH3CH2OH
| H2SO4(浓) |
| 170℃ |
第二步,乙烯与溴生成1,2-二溴乙烷(CH2=CH2+Br2→BrCH2CH2Br).
可能存在的副反应有:乙醇在浓硫酸的存在下于l40℃脱水生成乙醚(C2H5-O-C2H5);温度过高,乙醇与浓硫酸反应生成SO2、CO2等酸性气体.
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
| 色、态 | 无色液体 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/(g?cm-3) | 0.79 | 2.2 | 0.71 | 3.1 |
| 沸点/℃ | 78.5 | 132 | 34.6 | 59.47 |
| 熔点/℃ | -130 | 9 | -116 | -7.25 |

回答下列问题:
(1)熔沸点:乙醇>乙醚.利用物质结构的相关知识解释原因
(2)组装好仪器后检查A、B、C装置气密性的操作是
(3)如果D中导气管发生堵塞事故,装置B中可能观察到的现象是
(4)装置C中可能发生反应的化学方程式是
(5)将1,2-二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在
a.水 b.氢氧化钠溶液 c.乙醇
(6)若产物中有少量副产物乙醚,可采用的除杂方法是
(7)反应时装置D的烧杯中应装
a.冷水 b.冰水. 查看习题详情和答案>>