网址:http://m.1010jiajiao.com/timu_id_4383078[举报]
 (1)一位同学在做氢气还原氧化铜实验时,发现还原出的红色物质又逐渐变成黑色,可能的错误操作是什么?
(1)一位同学在做氢气还原氧化铜实验时,发现还原出的红色物质又逐渐变成黑色,可能的错误操作是什么?(2)另一位同学收集了一试管氢气,按如图所示用拇指堵住试管口,移近火焰,检验氢气的纯度,结果没有听到任何声音,他认为氢气已经纯净了,对么?请你说明理由.
(3)氢气作为新能源普遍被人们看好.请写出氢气作为新能源的优缺点.(各写一条)
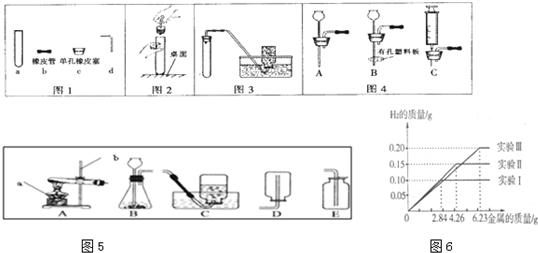
(1)根据图1回答:①写出a的名称
(2)采用图2所示操作可能造成的后果之一是
(3)利用图3装置(夹持装置未画出)能进行的实验是
(4)图3中的气体发生装置虽然简单,操作方便,但无法控制反应速率.请从图4中选取
(5)实验室用图5中A装置制氧气的化学方程式是
| ||
| △ |
| ||
| △ |
| ||
| ||
(6)机动车排放的尾气是空气的重要污染源,其成分之一是NO.某化学兴趣小组的同学在查阅资料后得知:①NO常温下是一种无色、难溶于水的气体,它的密度比空气略大;②NO常温下能与氧气迅速反应,生成红棕色的NO2气体:2NO2+O2═2NO2;③实验室常用铜与稀硝酸反应制取NO:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4X. 根据以上信息完成下列问题:
①物质X的化学式为
②若选择合适的装置来制取并收集NO气体,你选择图5中的发生装置是
③该小组的同学通过查阅资料还得知:a.NO容易和血红蛋白结合而使人中毒;b.NO能抗击侵入人体的微生物,并能阻止癌细胞的繁殖和肿瘤细胞的扩散.综合分析①和②的信息,你得到的启示是
④某化工厂准备生产Cu(NO3)2,以铜和稀硝酸为主要原料设计了两种方案:
方案一:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑十4X;
方案二:2Cu+O2
| ||
(7)某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.23g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制出如图象图6:试回答(计算结果精确到0.1%):
①写出实验中有关的化学方程式:
②实验I中铁参加反应的质量为
③稀硫酸完全参加反应的实验中,反应后溶液中溶质的质量分数是多少.
(1)钢铁属于
(2)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失.在日常生活中,小明发现切过咸菜的菜刀更容易生锈.为了验证该现象,小明做了下列实验:
取两支试管,分别放上一个相同铁钉,在一支试管中加入
(3)为了防止钢铁锈蚀,人们常采用在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法.这些方法都能防止锈蚀的共同原理是
(4)铁螺丝放入足量的稀盐酸中,观察到铁锈逐渐消失,该反应的化学方程式为:
一段时间后,又观察到铁钉表面有气泡产生,写出产生气泡的化学方程式:
长时间反应后,溶液中有黑色颗粒沉淀,该物质是
(5)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如下:

请写出第③步反应的化学方程式:
(6)金属矿物的储量有限,而且不能再生,所以废钢铁要
(7)一同学联想到家里铜制餐具上有一层绿色物质,认为铜在空气中也会生锈.他们上网查阅资料,知道这种绿色物质的化学成分为Cu2(OH)2CO3(铜绿).他们从铜绿组成和空气的成分大胆猜测,铜生锈除了与铁生锈条件相同外,还应该有CO2参加反应.
请写出铜在空气中生成铜绿的化学方程式
(8)将盛有等质量、等质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的铝和铁(提示:铝与盐酸反应生成氯化铝和氢气),待反应停止后,请判断:
若天平仍保持平衡,烧杯中一定没有剩余的物质是
若天平失去平衡,则指针一定偏向
钢铁是重要的金属材料,在生产、生活中有广泛的用途.
(1)钢铁属于______(填“纯净物”或“混合物”).
(2)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失.在日常生活中,小明发现切过咸菜的菜刀更容易生锈.为了验证该现象,小明做了下列实验:
取两支试管,分别放上一个相同铁钉,在一支试管中加入______,在另一支试管中加入等体积的______,一周后小明观察实验现象,得到了与日常生活中相同的结果,他的结论是:水中溶有______.
(3)为了防止钢铁锈蚀,人们常采用在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法.这些方法都能防止锈蚀的共同原理是______.
(4)铁螺丝放入足量的稀盐酸中,观察到铁锈逐渐消失,该反应的化学方程式为:
______;
一段时间后,又观察到铁钉表面有气泡产生,写出产生气泡的化学方程式:
______;
长时间反应后,溶液中有黑色颗粒沉淀,该物质是______,把该物质从溶液中分离出来的方法是______.
(5)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如下:

请写出第③步反应的化学方程式:______;
(6)金属矿物的储量有限,而且不能再生,所以废钢铁要______.
(7)一同学联想到家里铜制餐具上有一层绿色物质,认为铜在空气中也会生锈.他们上网查阅资料,知道这种绿色物质的化学成分为Cu2(OH)2CO3(铜绿).他们从铜绿组成和空气的成分大胆猜测,铜生锈除了与铁生锈条件相同外,还应该有CO2参加反应.
请写出铜在空气中生成铜绿的化学方程式______.
(8)将盛有等质量、等质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的铝和铁(提示:铝与盐酸反应生成氯化铝和氢气),待反应停止后,请判断:
若天平仍保持平衡,烧杯中一定没有剩余的物质是______;
若天平失去平衡,则指针一定偏向______的一侧.
查看习题详情和答案>>
(14分)钢铁是重要的金属材料,在生产、生活中有广泛的用途。
(1)钢铁属于______________(填“纯净物”或“混合物”)。
(2)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。在日常生活中,小明发现切过咸菜的菜刀更容易生锈.为了验证该现象,小明做了下列实验:
取两支试管,分别放上一个相同铁钉,在一支试管中加入___________,在另一支试管中加入等体积的___________,一周后小明观察实验现象,得到了与日常生活中相同的结果,他的结论是:水中溶有 。
(3)为了防止钢铁锈蚀,人们常采用在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法。这些方法都能防止锈蚀的共同原理是_________________________。
(4)铁螺丝放入足量的稀盐酸中,观察到铁锈逐渐消失,该反应的化学方程式为:
;
一段时间后,又观察到铁钉表面有气泡产生,写出产生气泡的化学方程式:
;
长时间反应后,溶液中有黑色颗粒沉淀,该物质是 ,把该物质从溶液中分离出来的方法是 。
(5)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如下:
请写出第③步反应的化学方程式:_________________________________________;
(6)金属矿物的储量有限,而且不能再生,所以废钢铁要_____________。
(7)一同学联想到家里铜制餐具上有一层绿色物质,认为铜在空气中也会生锈。他们上网查阅资料,知道这种绿色物质的化学成分为Cu2(OH)2CO3(铜绿)。他们从铜绿组成和空气的成分大胆猜测,铜生锈除了与铁生锈条件相同外,还应该有CO2参加反应。
请写出铜在空气中生成铜绿的化学方程式 。
(8)将盛有等质量、等质量分数的稀盐酸的两只烧杯,放在托盘天平左右两盘上,调节至平衡,再向两只烧杯中分别放入质量相等的铝和铁(提示:铝与盐酸反应生成氯化铝和氢气),待反应停止后,请判断:
若天平仍保持平衡,烧杯中一定没有剩余的物质是 ;
若天平失去平衡,则指针一定偏向 的一侧。