摘要:(9)C+SiO2 Si+2CO↑ (10)2H2O2 2H2O+O2↑ (11)2NaCl+2H2O 2NaOH+H2↑+Cl2↑ (12)4NH3+5O2 4NO+6H2O
网址:http://m.1010jiajiao.com/timu_id_437576[举报]
下列说法正确的是( )
| A、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | B、检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清夜于试管中,滴加KSCN溶液2-3滴即可 | C、在粗硅的制取中,C+SiO2═Si+2CO 硅被还原,所以碳的还原性大于硅的还原性 | D、用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通CO2 |
A、B两元素的原子最外层电子数相同,但相差一个电子层,且两单质在常温下所处的状态相同,A、C两元素位于同一周期,并能形成化合物AC2,AC2内共有22质子,试求:
(1)A、B、C的元素名称A
(2)A、B的最高价氧化物的水化物的按酸性由强到弱顺序为(填化学式)
(3)A、B、C的氢化物的按稳定性由强到弱顺序为(填化学式)
(4)B的氧化物与A的单质反应的化学方程式为
查看习题详情和答案>>
(1)A、B、C的元素名称A
碳
碳
;B硅
硅
;C氧
氧
(2)A、B的最高价氧化物的水化物的按酸性由强到弱顺序为(填化学式)
H2CO3>H2SiO3
H2CO3>H2SiO3
(3)A、B、C的氢化物的按稳定性由强到弱顺序为(填化学式)
H2O>CH4>SiH4
H2O>CH4>SiH4
(4)B的氧化物与A的单质反应的化学方程式为
C+SiO2
2CO↑+Si
| ||
C+SiO2
2CO↑+Si
.
| ||
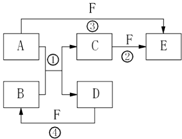 A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出).
A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出).(1)若A是常见金属单质,与B的水溶液反应生成C和D.D、F是气体单质,D在F中燃烧时发出苍白色火焰.则反应②(在水溶液中进行)的离子方程式为
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(2)若A、D为短周期元素组成的固体单质,一种为金属,另一种为非金属.且③④两个反应都有红棕色气体生成,则反应④的化学方程式为
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
| ||
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
.
| ||
(3)若A是黑色固体,D是有臭鸡蛋气味的气体,E溶液中滴加KSCN溶液呈血红色.则D的电子式是


4FeS2+11O2
2Fe2O3+8SO2
| ||
4FeS2+11O2
2Fe2O3+8SO2
,使用的设备是
| ||
沸腾炉
沸腾炉
.(4)若B是由地壳中含量最高的两种元素组成,A的一种同素异形体与B、D属同一种类型的晶体,则反应①的化学方程式是
2C+SiO2
Si+2CO↑
| ||
2C+SiO2
Si+2CO↑
,B与烧碱溶液反应的化学方程式是
| ||
SiO2+2NaOH=Na2SiO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
.