摘要:20种常见物质的俗名重晶石-BaSO4 明矾-KAl(SO4) 2?12H2O 蓝矾.胆矾-CuSO4?5H20 熟石膏-2CaSO4?H2O 石膏-CaSO4?2H2O 小苏打-NaHCO3 纯碱-Na2CO3 碳铵―NH4HCO3 干冰-CO2 水玻璃 -Na2SiO3 氯仿-CHCl3 甘油-CH2OH-CHOH- CH2OH 石炭酸-C6H5OH 福马林林-HCHO 冰醋酸.醋酸-CH3COOH 草酸-HOOC―COOH硬脂酸-C17H35COOH 软脂酸-C15H31COOH 油酸-C17H33COOH甘氨酸-H2N―CH2COOH
网址:http://m.1010jiajiao.com/timu_id_437570[举报]
中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出).

已知:A、B、C、D是单质,其余是化合物.其中B、D是常见金属.又知A在C中点燃有苍白色火焰.请回答下列问题:
(1)W的电子式是
 .
.
(2)写出N的化学式
(3)写出下列反应的离子方程式:
反应①
反应③
K溶液和过量氨水反应
查看习题详情和答案>>

已知:A、B、C、D是单质,其余是化合物.其中B、D是常见金属.又知A在C中点燃有苍白色火焰.请回答下列问题:
(1)W的电子式是


(2)写出N的化学式
FeCl3
FeCl3
,并任写一种N的主要用途可用作催化剂、净水剂、印刷电路铜板腐蚀剂和外伤止血剂等
可用作催化剂、净水剂、印刷电路铜板腐蚀剂和外伤止血剂等
.(3)写出下列反应的离子方程式:
反应①
2Cl-+2H2O
2OH-+H2↑+Cl2↑
| ||
2Cl-+2H2O
2OH-+H2↑+Cl2↑
,
| ||
反应③
Al3++3AlO2-+6H2O═4Al(OH)3↓
Al3++3AlO2-+6H2O═4Al(OH)3↓
,K溶液和过量氨水反应
Al3++3NH3?H2O═Al(OH)3↓+3NH4+
Al3++3NH3?H2O═Al(OH)3↓+3NH4+
. 中学化学中几种常见物质的转化关系如下图(部分产物未列出).A是一种金属单质,D是一种非金属固体单质.
中学化学中几种常见物质的转化关系如下图(部分产物未列出).A是一种金属单质,D是一种非金属固体单质.请回答下列问题:
(1)A、C的化学式分别为A
Fe
Fe
,CFe2(SO4)3
Fe2(SO4)3
.(2)F的浓溶液与A反应过程中,F体现的性质与下列反应中H2SO4体现的性质完全相同的是
C
C
.A.C+2H2SO4(浓)
| ||
B.Fe+H2SO4═FeSO4+H2↑
C.Cu+2H2SO4(浓)
| ||
D.FeO+H2SO4═FeSO4+H2O
(3)写出反应E+H2O2-→F的化学方程式:
SO2+H2O2═H2SO4
SO2+H2O2═H2SO4
.(4)若反应F+D-→E转移电子数为6.02×1023,则消耗D的质量为
8g
8g
. 中学化学中几种常见物质的转化关系如下所示(部分反应的生成物已略去),其中A、a、c是单质,a为黄绿色气体,E为红褐色沉淀.请回答下列问题:
中学化学中几种常见物质的转化关系如下所示(部分反应的生成物已略去),其中A、a、c是单质,a为黄绿色气体,E为红褐色沉淀.请回答下列问题:(1)写出下列物质的化学式:B
FeS
FeS
,bNaOH
NaOH
.(2)D的水溶液呈 (填“酸”、“碱”或“中”)性,将饱和的D溶液加入沸水中并继续煮沸一段时间后得到的液体(填序号).
①是溶液
②是胶体
③具有丁达尔现象
④可全部透过滤纸
(3)写出下列反应的离子方程式:
①电解F的水溶液:
2Cl-+2H2O
2OH-+Cl2↑+H2↑
| ||
2Cl-+2H2O
2OH-+Cl2↑+H2↑
;
| ||
②C与等物质的量的Na2O2在溶液中反应:
4Fe2++4Na2O2+6H2O=4Fe(OH)3↓+O2↑+8Na+
4Fe2++4Na2O2+6H2O=4Fe(OH)3↓+O2↑+8Na+
.无机框图下图为中学化学中几种常见物质的转化关系(部分产物已略去).已知:A、C、D是常见的气体单质,F气体极易溶于水,且液态常做致冷剂.
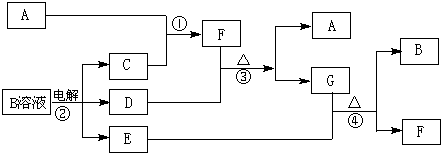
(1)写出化学式F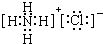
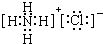 ;
;
(2)鉴定G中阳离子的实验方法和现象
(3)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶液反应的离子方程式和③的化学方程式
(4)工业上电解B溶液制得一系列化工原料,写出其电解的化学方程式,并标出电子转移的方向和数目
 .
.
查看习题详情和答案>>

(1)写出化学式F
NH3
NH3
,写出电子式G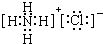
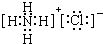
(2)鉴定G中阳离子的实验方法和现象
取少量氯化铵的溶液加入试管中,用胶头滴管加入少量NaOH浓溶液,加热用湿润的红色石蕊试纸在试管口检验放出的气体,试纸变蓝色
取少量氯化铵的溶液加入试管中,用胶头滴管加入少量NaOH浓溶液,加热用湿润的红色石蕊试纸在试管口检验放出的气体,试纸变蓝色
;(3)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶液反应的离子方程式和③的化学方程式
2OH-+Cl2=ClO-+Cl-+H2O
2OH-+Cl2=ClO-+Cl-+H2O
、8NH3+3Cl2
N2+6NH4Cl
| ||
8NH3+3Cl2
N2+6NH4Cl
.
| ||
(4)工业上电解B溶液制得一系列化工原料,写出其电解的化学方程式,并标出电子转移的方向和数目

