摘要:化学平衡典型实验:Cr2O72― + H2O == 2CrO42― +2H+ .2NO2 = N2O4 .Fe3+ + 3SCN― = Fe(SCN)3
网址:http://m.1010jiajiao.com/timu_id_437504[举报]
某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为零.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为零.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列问题:
(1)利用表中的相应的数字请分析在实验1、2中,实验
(2)实验1与实验4相比较实验
(3)在实验1中,求反应在10至20分钟时间内的平均反应速率?(请写出计算过程)
查看习题详情和答案>>
 B+D在四种不同条件下进行,B、D起始浓度为零.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为零.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:| 实验序号 | 时间/浓度/温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)利用表中的相应的数字请分析在实验1、2中,实验
2
2
使用了催化剂.(2)实验1与实验4相比较实验
4
4
先达到平衡,理由是实验4在进行了30min后达到化学平衡,因为30min后A的浓度不再随时间而变化,而实验1在进行了40min才达到化学平衡,所以实验4先达到化学平衡,
实验4在进行了30min后达到化学平衡,因为30min后A的浓度不再随时间而变化,而实验1在进行了40min才达到化学平衡,所以实验4先达到化学平衡,
.(3)在实验1中,求反应在10至20分钟时间内的平均反应速率?(请写出计算过程)
试述实验室证明浓度对化学平衡影响实验过程.
反应原理(用离子方程式表示):
操作步骤及现象:
查看习题详情和答案>>
反应原理(用离子方程式表示):
Fe3++SCN-?Fe(SCN)3
Fe3++SCN-?Fe(SCN)3
操作步骤及现象:
| 实验步骤 | 实验现象 | 解释和结论 |
| (1)在小烧杯中加入0.1mol/LFeCl3溶液2mL和0.1mol/LNH4SCN溶液2mL.加水10ml,混匀后分装于3支试管中. | 反应后形成红色溶液. | |
| (2) 往第一支试管加入少量三氯化铁溶液 往第一支试管加入少量三氯化铁溶液 |
试管中溶液 颜色加深 试管中溶液 颜色加深 |
增大反应物浓度促使 化学平衡向正反应的 方向移动 增大反应物浓度促使 化学平衡向正反应的 方向移动 |
| (3) 往第二支试管中加入少量硫氰化钾溶液 往第二支试管中加入少量硫氰化钾溶液 |
试管中溶液 颜色加深 试管中溶液 颜色加深 |
增大反应物浓度促使 化学平衡向正反应的 方向移动 增大反应物浓度促使 化学平衡向正反应的 方向移动 |
| (4)比较上述三支试管的颜色. | 加入铁离子或硫氰根离子都能使溶液 颜色加深 加入铁离子或硫氰根离子都能使溶液 颜色加深 |
增大任何一种反应物 的浓度促使化学平衡向正反应的方向移动 增大任何一种反应物 的浓度促使化学平衡向正反应的方向移动 |
试述实验室证明浓度对化学平衡影响实验过程.
反应原理(用离子方程式表示):______
操作步骤及现象:
查看习题详情和答案>>
反应原理(用离子方程式表示):______
操作步骤及现象:
| 实验步骤 | 实验现象 | 解释和结论 |
| (1)在小烧杯中加入0.1mol/LFeCl3溶液2mL和0.1mol/LNH4SCN溶液2mL.加水10ml,混匀后分装于3支试管中. | 反应后形成红色溶液. | |
| (2)______ | ______ | ______ |
| (3)______ | ______ | ______ |
| (4)比较上述三支试管的颜色. | ______ | ______ |
查看习题详情和答案>>
将CoCl2溶解于盐酸中可以形成CoCl42-,在溶液中存在下面的化学平衡:
Co2+ +4Cl- CoCl42- ; △H>0
CoCl42- ; △H>0
粉红色 蓝色
下列说法正确的是
Co2+ +4Cl-
 CoCl42- ; △H>0
CoCl42- ; △H>0 粉红色 蓝色
下列说法正确的是
[ ]
A.升高温度,正反应速率增大,逆反应速率减小
B.该反应的平衡常数K=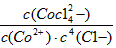
C.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
D.增大Cl-浓度,平衡向正反应方向移动,CO2、Cl-浓度都减小
查看习题详情和答案>>
B.该反应的平衡常数K=
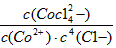
C.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色
D.增大Cl-浓度,平衡向正反应方向移动,CO2、Cl-浓度都减小
 通过实验测定反应速率的方法有多种,为证明化学反应速率与反应的浓度有关.有同学设计如下实验:
通过实验测定反应速率的方法有多种,为证明化学反应速率与反应的浓度有关.有同学设计如下实验:(1)比较锌粒与不同浓度硫酸反应时的速率,如图装置可通过测定收集等体积H2需要的
时间
时间
来实现;(2)在KMnO4与H2C2O4反应中,可通过测定
溶液褪色所需时间
溶液褪色所需时间
来测定该反应的速率;写出酸性条件下KMnO4与H2C2O4(弱酸)反应,产生二氧化碳气体、水和Mn2+的离子反应方程式:2MnO4-+5H2C2O4 +6H+=2Mn2++8H2O+10CO2↑
2MnO4-+5H2C2O4 +6H+=2Mn2++8H2O+10CO2↑
;此反应开始反应缓慢,随后反应迅速加快,其原因是C
C
(填字母)A.KMnO4溶液中的H+起催化作用
B.生成的CO2逸出,使生成物浓度降低
C. 反应中,生成的Mn2+起催化作用
D.在酸性条件下KMnO4的氧化性增强
(3)在Na2S2O3和H2SO4反应中,该反应速率可通过测定
出现浑浊所需的时间
出现浑浊所需的时间
来测定,分析下列实验数据记录,可推测出现混浊的时间由快到慢的顺序是t1=t4<t3<t2
t1=t4<t3<t2
;| 序号 | Na2S2O3溶液 | 稀H2SO4 | 出现混浊时间 | ||
| 浓度 | 用量 | 浓度 | 用量 | ||
| (1) | 0.1mol?L-1 | 10mL | 0.1mol?L-1 | 10mL | t1 |
| (2) | 0.1mol?L-1 | 10mL+5mL 水 | 0.1mol?L-1 | 10mL | t2 |
| (3) | 0.1mol?L-1 | 10mL | 0.1mol?L-1 | 5mL+5mL水 | t3 |
| (4) | 0.1mol?L-1 | 5mL | 0.1mol?L-1 | 5mL | t4 |
(已知:在水溶液中K2Cr2O7为橙红色,K2CrO4为黄色.)往上述溶液中加入氢氧化钠溶液呈
黄色
黄色
色;向已加入氢氧化钠的溶液中,再加入过量硫酸溶液呈橙红色
橙红色
色;此实验现象,符合勒夏特列原理:如果改变维持化学平衡的条件(浓度、压力和温度),平衡就会向着减弱
减弱
这种改变的方向移动.