摘要:25.某二氧化锰样品中含有杂质炭.为测定该样品中二氧化锰的质量分数.某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气.使杂质炭在加热条件下反应生成CO2来进行分析测定. (1)仪器①的名称是 .如果该实验选择图㈠装置来制取氧气.则所用药品为 .反应的化学方程式为 . (2)用图㈡装置可收集和干燥氧气:若烧瓶充满水来收集氧气.气体应从 端通入,若在烧瓶内装入浓硫酸进行干燥气体.气体应从 端通入. (3)图㈢是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置.装置③中装有碱石灰.其作用是 . (4)为验证图㈢中装置②已将CO2吸收完全.可在装置②与③之间加入图㈣装置进行证明.则图㈣装置中加入的试剂为 . A. NaOH溶液 B. 澄清石灰水 C. 浓硫酸 (5)称取5.0 g二氧化锰样品进行实验.图㈢中装置②反应前后的质量差为1.1 g.则样品中二氧化锰的质量分数为 .26.已知某合金粉末除铝外.还含有铁.铜中的一种或两种.某兴趣小组在老师的指导下.对合金粉末中铁.铜的存在情况进行了探究. [查阅资料]铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水),Fe.Cu不与氢氧化钠溶液反应. [猜 想]猜想1:该合金粉末中除铝外.还含有铁. 猜想2:该合金粉末中除铝外.还含有 . 猜想3:该合金粉末中除铝外.还含有铁.铜. [实验探究]下列实验仅供选择的试剂:10%盐酸.30%NaOH溶液. 实验方案 实现现象 结论 ①取一定量的合金粉末.加过量的 .充分反应后过滤.滤渣备用. 粉末部分溶解.并有气体放出. 合金中一定含有 . ②取步骤①所得滤渣.加过量的 .充分反应. 滤渣部分溶解.并有气体放出.溶液呈浅绿色. 合金中一定含有 . [探究结论]猜想3成立. [反思]一般来说.活泼金属能与盐酸等酸反应.而铝与酸.碱都能反应.说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式 .
网址:http://m.1010jiajiao.com/timu_id_4374742[举报]
某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:利用下图实验装置,在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定.

(1)仪器①的下端插在液面下是为了防止 ,如果该实验选择甲装置来制取氧气,则反应的化学方程式为 .
(2)用乙装置可用来收集和干燥气体.若在烧瓶内装入浓硫酸进行气体干燥,气体应从 端通入(选填“a”或“b”),下列气体中不能用浓硫酸干燥的是 .
A.H2B.NH3C.CO2D.O2
(3)丙是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,仪器③中装有碱石灰,其作用是 .
(4)为验证装置丙中②已将CO2吸收完全,可在②与③之间加入丁装置进行证明,则丁装置中加入的试剂为( )
A.浓盐酸 B.澄清石灰水 C.烧碱溶液 D.浓硫酸
(5)称取8 g二氧化锰样品进行实验,丙中装置②反应前后的质量差为1.1 g,计算样品中二氧化锰的质量分数为多少? 查看习题详情和答案>>

(1)仪器①的下端插在液面下是为了防止
(2)用乙装置可用来收集和干燥气体.若在烧瓶内装入浓硫酸进行气体干燥,气体应从
A.H2B.NH3C.CO2D.O2
(3)丙是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,仪器③中装有碱石灰,其作用是
(4)为验证装置丙中②已将CO2吸收完全,可在②与③之间加入丁装置进行证明,则丁装置中加入的试剂为(
A.浓盐酸 B.澄清石灰水 C.烧碱溶液 D.浓硫酸
(5)称取8 g二氧化锰样品进行实验,丙中装置②反应前后的质量差为1.1 g,计算样品中二氧化锰的质量分数为多少? 查看习题详情和答案>>
某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定.
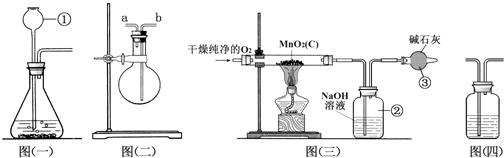
(1)仪器①的名称是 .如果该实验选择图㈠装置来制取氧气,则所用药品反应的化学方程式为 .如果该实验选择图㈠装置来制取氢气则反应的化学方程式为 .如果该实验选择图㈠装置来制取二氧化碳气体则反应的化学方程式为 .
(2)用图(二)装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从 (填“a”或“b”,下同)端通入;若在烧瓶内装入浓硫酸进行干燥气体,气体应从 端通入.
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰,其作用是 .
(4)为验证图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为 (填字母).
A.NaOH溶液 B.澄清石灰水 C.浓硫酸
(5)称取5.0g二氧化锰样品进行实验,图㈢中装置②反应前后的质量差为1.1g,则样品中二氧化锰的质量分数为 (填计算结果).
查看习题详情和答案>>

(1)仪器①的名称是
(2)用图(二)装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰,其作用是
(4)为验证图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为
A.NaOH溶液 B.澄清石灰水 C.浓硫酸
(5)称取5.0g二氧化锰样品进行实验,图㈢中装置②反应前后的质量差为1.1g,则样品中二氧化锰的质量分数为
某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定.

(1)如果该实验选择图(一)装置来制取氧气,则所用药品为 (填化学式),反应的化学方程式为 .
(2)用图(二)装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从 (填“a”或“b”,下同)端通入;若在烧瓶内装入浓硫酸进行干燥气体,气体应从 端通入.
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰,其作用是 .
(4)为验证图㈢中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图㈣装置中加入的试剂为 (填字母).
A. NaOH溶液;B.澄清石灰水;C.浓硫酸
(5)称取5.0 g二氧化锰样品进行实验,图㈢中装置②反应前后的质量差为1.1 g,则样品中二氧化锰的质量分数为 (填计算结果).
查看习题详情和答案>>

(1)如果该实验选择图(一)装置来制取氧气,则所用药品为
(2)用图(二)装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰,其作用是
(4)为验证图㈢中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图㈣装置中加入的试剂为
A. NaOH溶液;B.澄清石灰水;C.浓硫酸
(5)称取5.0 g二氧化锰样品进行实验,图㈢中装置②反应前后的质量差为1.1 g,则样品中二氧化锰的质量分数为
某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定.

(1)仪器①的名称是 .如果该实验选择图(一)装置来制取氧气,该反应的化学方程式为 .
(2)用图(二)装置可用于干燥氧气:应在烧瓶内装入 进行干燥气体,气体应从 端通入.
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰(生石灰与固体氢氧化钠的混合物),其作用是 .
(4)为验证图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为 (填字母).
A.NaOH溶液 B. 澄清石灰水 C. 浓硫酸
(5)称取5.0g二氧化锰样品进行实验,图(三)中装置②反应前后的质量差为1.1g,则样品中二氧化锰的质量分数为 (填计算结果).
查看习题详情和答案>>

(1)仪器①的名称是
(2)用图(二)装置可用于干燥氧气:应在烧瓶内装入
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰(生石灰与固体氢氧化钠的混合物),其作用是
(4)为验证图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为
A.NaOH溶液 B. 澄清石灰水 C. 浓硫酸
(5)称取5.0g二氧化锰样品进行实验,图(三)中装置②反应前后的质量差为1.1g,则样品中二氧化锰的质量分数为
某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定(测定均为安全范围内).

(1)仪器①的名称是 .如果该实验选择图㈠装置来制取氧气,则该装置中发生反应的方程式为 .
(2)用图㈡装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从 (填“a”或“b”,下同)端通入;若在烧瓶内装入浓硫酸进行干燥气体,气体应从 端通入.
(3)为验证图㈢中装置②己将CO2吸收完全,可在装置②与③之间加入图㈣装置进行证明,则图㈣装置中加入的试剂为 (填字母).
A.NaOH溶液 B.澄清石灰水 C.浓硫酸
(4)图㈢是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰(即氧化钙和氢氧化钠固体混合物),其作用是 .
(5)称取5.0g二氧化锰样品进行实验,图㈢中装置②反应前后的质量差为1.1g,则样品中二氧化锰的质量分数为 (填计算结果).
查看习题详情和答案>>

(1)仪器①的名称是
(2)用图㈡装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从
(3)为验证图㈢中装置②己将CO2吸收完全,可在装置②与③之间加入图㈣装置进行证明,则图㈣装置中加入的试剂为
A.NaOH溶液 B.澄清石灰水 C.浓硫酸
(4)图㈢是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰(即氧化钙和氢氧化钠固体混合物),其作用是
(5)称取5.0g二氧化锰样品进行实验,图㈢中装置②反应前后的质量差为1.1g,则样品中二氧化锰的质量分数为