网址:http://m.1010jiajiao.com/timu_id_437444[举报]
 (2009?广东)铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂.
(2009?广东)铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂.(1)Cu位于元素周期表第I B族.Cu2+的核外电子排布式为
(2)右图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为
(3)胆矾CuSO4?5H2O可写成[Cu(H2O4)]SO4?H2O,其结构示意图如下:

下列说法正确的是
A.在上述结构示意图中,所有氧原子都采用sp3杂化
B.在上述结构示意图中,存在配位键、共价键和离子键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子.已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
(5)Cu2O的熔点比Cu2S的
A.锗的第一电离能高于碳而电负性低于碳
B.四氯化锗与四氯化碳分子都是四面体构型
C.二氧化锗与二氧化碳都是非极性的气体化合物
D.锗和碳都存在具有原子晶体结构的单质
(2)铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域.回答下列问题:
①铜原子基态电子排布式为
②用晶体的x射线衍射法可以测得阿伏加德罗常数.对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361pm.又知铜的密度为9.00g?cm-3,则镉晶胞的体积是
(列式计算,己知Ar(Cu)=63.6);
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如图),a位置上Cl原子的杂化轨道类型为
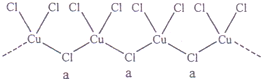
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是

用化学用语回答下列问题:
(1)写出元素f的基态原子核外电子排布式
(2)在c6a6分子中,元素c为
(3)ci2分子的电子式为


(4)第一电离能:h
(5)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是
A.j位于元素周期表中第四周期、ⅠB族,属于ds区元素
B.d的基态原子中,2p能级为半充满,属于p区元素
C.最外层电子排布式为4s1,一定属于ⅠA族
D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
(6)将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液,显深蓝色的离子是
(7)j的金属晶体的晶胞如图2所示,则一个晶胞中j原子的个数是
晶体的质点(分子、离子或原子等)在空间有规则地排列、具有整齐外形、以多面体出现的固体物质。在空间里无限地周期性的重复形成晶体的、具有代表性的最小单元,称为晶胞。一种A1―Fe合金的晶胞如下图所示。据此解答下列问题:

(1)确定该合金的化学式 。
(2)若晶体的密度为![]() ,则此合金中最近的两个Fe原子之间的距离(用含
,则此合金中最近的两个Fe原子之间的距离(用含![]() 的代数式表示,不必化简)为 cm。
的代数式表示,不必化简)为 cm。
(3)取该合金粉末2.78g溶于100mL某稀硝酸溶液中,待反应完全后得到1.12L(标准状况)NO气体(设两者恰发完全反应),则原硝酸溶液的物质的量浓度为 mol/L
查看习题详情和答案>>(选做题)(19分)图表法、模型法是常用的科学研究方法。
I.下图是研究部分元素的氢化物的沸点变化规律的图像。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b(其中A点对应的沸点是100℃),你认为正确的是 ,理由是 。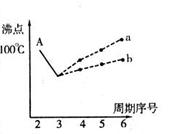
II.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属则被科学家预测为是钛(Ti)。钛被誉为“未来世纪的金属”。试回答下列问题:
(1)22Ti元素基态原子的价电子层排布式为 。
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,价电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如右图,则它的化学式是 。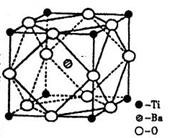
III.上世纪60年化,第一个稀有气体化合物Xe[PtF6]被合成出来后,打破了“绝对情性”的观念。在随后的几年内,科学家又相继后成了氙的氟化物、氧化物等。
(1)金属Pt内部原子的堆积方式与铜及干冰中的CO2相同,右图正方体是Pt晶胞的示意图,试说出Pt原子在晶胞中的位置 。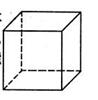
(2)稀有气体(氡除外)中,只有较重的氙能合成出多种化合物,
其可能原因是 (填字母代号)
| A.氙的含量比较丰富 | B.氙的相对原子质量大 |
| C.氙原子半径大,电离能小 | D.氙原子半径小,电负性大 |