摘要:判断反应能否进行 该类题目往往以提供陌生信息.然后让学生通过分析提取信息从而解答问题. 例2.已知反应Co2O3+6HCl=2CoCl2+Cl2↑+3H2O.3Cl2+2FeI2=2FeCl3+3I2.2FeCl3+2KI=I2+2FeCl2+2KCl均能进行.请判断下列反应在溶液中不可能发生的是( ) A.Cl2+FeI2=FeCl2+I2 B.3Cl2+6FeI2=2FeCl3+4FeI3 C.I2+2Fe2+=2Fe3++I― D.Co2O3+6H++2I―=I2+2Co2++3H2O E.Co2O3+6H++2Fe2+=2Fe3++2Co2++3H2O 解析:氧化还原反应是:强氧化剂+强还原剂 弱氧化剂+弱还原剂.或者说氧化性.还原性体现“以强制弱 的原则.故根据三个已知反应可知氧化性顺序为Co2O3>Cl2>FeCl3>I2.Cl2与FeI2反应时.首先是还原性更强的I―反应.因此A反应正确.B.C中由于氧化性Fe3+>I2.因此反应均错误.D.E根据Co2O3>I2.Co2O3>Fe3+.可以确定两反应均正确. 答案:B.C
网址:http://m.1010jiajiao.com/timu_id_4367368[举报]
(2011?咸阳模拟)如图是工业生产硝酸铵的流程示意图.
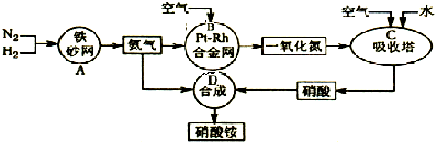
(1)吸收塔C中通入过量空气的目的是
(2)已知:4NH3(g)+3O2(g)═2N2(g)+6H2O(g),△H=-1266.8kJ/mol;
N2(g)+O2(g)═2NO(g),△H=+180.5kJ/mol
据此写出氨高温催化氧化的热化学方程式:
若上述催化氧化过程转移了5mol电子,则反应的能量变化为
(3)在化工研究中,经常要判断反应能否自发进行,若某反应的△H<0,则该反应是否一定能自发进行?
(4)已知:N2(g)+3H2(g)?2NH3(g),△H=-92kJ/mol.为提高氢气的转化率,宜采取的措施有
A.适当升高温度
B.使用更有效的催化剂
C.增大压强
D.循环利用和不断补充氮气
E.及时分离出氨气
(5)在一定温度和压强下,将H2和N2按3:1的体积比在密闭容器中混合,当反应达到平衡时,测得平衡混合气中NH3的体积分数为20.0%,此时H2的转化率为
查看习题详情和答案>>

(1)吸收塔C中通入过量空气的目的是
使NO充分氧化(或者“提高NO的转化率”)
使NO充分氧化(或者“提高NO的转化率”)
.A、B、C、D四个容器中的反应,属于氧化还原反应的是ABC
ABC
(填字母).(2)已知:4NH3(g)+3O2(g)═2N2(g)+6H2O(g),△H=-1266.8kJ/mol;
N2(g)+O2(g)═2NO(g),△H=+180.5kJ/mol
据此写出氨高温催化氧化的热化学方程式:
4NH3(g)+5O2(g)=4NO(g)+6H2O(g),△H=-905.8KJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g),△H=-905.8KJ/mol
.若上述催化氧化过程转移了5mol电子,则反应的能量变化为
226.45
226.45
kJ.(3)在化工研究中,经常要判断反应能否自发进行,若某反应的△H<0,则该反应是否一定能自发进行?
不一定
不一定
(填“一定”或“不一定”)(4)已知:N2(g)+3H2(g)?2NH3(g),△H=-92kJ/mol.为提高氢气的转化率,宜采取的措施有
CDE
CDE
(填字母).A.适当升高温度
B.使用更有效的催化剂
C.增大压强
D.循环利用和不断补充氮气
E.及时分离出氨气
(5)在一定温度和压强下,将H2和N2按3:1的体积比在密闭容器中混合,当反应达到平衡时,测得平衡混合气中NH3的体积分数为20.0%,此时H2的转化率为
33.3%
33.3%
(计算结果保留一位小数).利用相关数据作出的推理或判断一定正确的是
A.用弱酸的电离常数比较相同条件下强碱弱酸盐溶液的碱性强弱
B.用物质的熔沸点数据推断物质的晶体类型
C.根据溶液的pH判断该溶液的酸碱性
D.根据焓变数据判断反应能否自发进行
查看习题详情和答案>>
已知:(NH4)2CO3(s)====NH4HCO3(s)+NH3(g) ΔH="+74.9" kJ·mol-1,下列说法中正确的是( )
| A.该反应中熵变小于0,焓变大于0 |
| B.该反应是吸热反应,因此一定不能自发进行 |
| C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行 |
| D.判断反应能否自发进行需要根据ΔH与ΔS综合考虑 |