摘要:H2S通入H2SeO3.溶液中所得氧化产物是( ) A.S B.Se C.S和Se D.不能反应.无氧化产物
网址:http://m.1010jiajiao.com/timu_id_4364459[举报]
(2013?海淀区二模)硫化氢(H2S)是一种具有臭鸡蛋气味的无色气体,有剧毒;存在于多种生产过程以及自然界中.在人体的很多生理过程中也起着重要作用.
(1)某化学小组设计了制取H2S并验证其性质的实验,如下图所示.A中是CuSO4溶液,B中放有湿润的蓝色石蕊试纸,C中是FeCl3溶液.
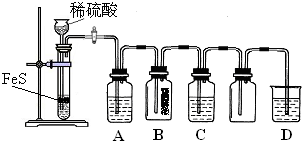
回答下列问题:
①A中有黑色沉淀(CuS)产生,A中发生反应的化学方程式为
②B中的现象是
③C中只有浅黄色沉淀产生,且溶液变浅绿色.则C中发生反应的离子方程式为
④D中盛放的试剂可以是
a.水 b.盐酸 c.NaCl溶液 d.NaOH溶液
(2)为进一步探究-2价硫的化合物与+4价硫的化合物反应条件,小组同学又设计了下列实验.
已知:电离平衡常数:H2S Ka1=1.3×10-7;Ka2=7.1×10-15
H2SO3 Ka1=1.7×10-2;Ka2=5.6×10-8
①根据上述实验,可以得出结论:在
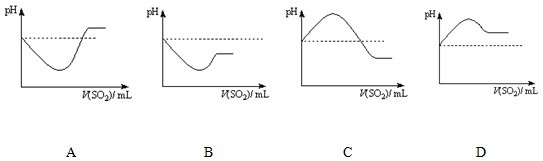
②将SO2气体通入H2S水溶液中直至过量,下列表示溶液pH随SO2气体体积变化关系示意图正确的是
(3)文献记载,常温下H2S可与Ag发生置换反应生成H2.现将H2S气体通过装有银粉的玻璃管,请设计简单实验,通过检验反应产物证明H2S与Ag发生了置换反应
查看习题详情和答案>>
| 资料:①H2S可溶于水(约1:2),其水溶液为二元弱酸. ②H2S可与许多金属离子反应生成沉淀. ③H2S在空气中燃烧,火焰呈淡蓝色. |

回答下列问题:
①A中有黑色沉淀(CuS)产生,A中发生反应的化学方程式为
H2S+CuSO4=CuS↓+H2SO4
H2S+CuSO4=CuS↓+H2SO4
.②B中的现象是
蓝色石蕊试纸变红
蓝色石蕊试纸变红
.③C中只有浅黄色沉淀产生,且溶液变浅绿色.则C中发生反应的离子方程式为
H2S+2Fe3+=S↓+2H++2Fe2+
H2S+2Fe3+=S↓+2H++2Fe2+
.④D中盛放的试剂可以是
d
d
(填标号).a.水 b.盐酸 c.NaCl溶液 d.NaOH溶液
(2)为进一步探究-2价硫的化合物与+4价硫的化合物反应条件,小组同学又设计了下列实验.
| 实验操作 | 实验现象 | |
| 实验1 | 将等浓度的Na2S和Na2SO3溶液按体积比2:1混合 | 无明显现象 |
| 实验2 | 将H2S通入Na2SO3溶液中 | 未见明显沉淀,再加入少量稀硫酸,立即产生大量浅黄色沉淀 |
| 实验3 | 将SO2通入Na2S溶液中 | 有浅黄色沉淀产生 |
H2SO3 Ka1=1.7×10-2;Ka2=5.6×10-8
①根据上述实验,可以得出结论:在
酸性(或酸性较强)
酸性(或酸性较强)
条件下,+4价硫的化合物可以氧化-2价硫的化合物.②将SO2气体通入H2S水溶液中直至过量,下列表示溶液pH随SO2气体体积变化关系示意图正确的是
C
C
(填序号).
(3)文献记载,常温下H2S可与Ag发生置换反应生成H2.现将H2S气体通过装有银粉的玻璃管,请设计简单实验,通过检验反应产物证明H2S与Ag发生了置换反应
将反应后的气体通入足量氢氧化钠溶液中(或硫酸铜溶液或氯化铁溶液等),除去未反应的H2S后,点燃,若观察到火焰呈淡蓝色,说明有H2生成,从而证明H2S与Ag发生了置换反应
将反应后的气体通入足量氢氧化钠溶液中(或硫酸铜溶液或氯化铁溶液等),除去未反应的H2S后,点燃,若观察到火焰呈淡蓝色,说明有H2生成,从而证明H2S与Ag发生了置换反应
.下述实验中,不能达到预期目的是( )
查看习题详情和答案>>
| 编号 | 实验内容 | 实验目的 |
| A | 将SO2通入酸性KMnO4溶液中 | 证明SO2具还原性 |
| B | 将H2S通入CuSO4溶液中生成黑色沉淀 | 比较H2S与H2SO4的酸性强弱 |
| C | 一定温度下,压缩一端封闭收集有NO2气体的注射器,使其体积减小 | 研究压强对气体反应化学平衡状态的影响 |
| D | 分别向2支试管中加入等体积等浓度的H2O2溶液,再向其中1支加入少量MnO2 | 研究催化剂对相同条件的H2O2分解速率的影响 |
水溶液是中学化学的重点研究对象.
(1)水是极弱的电解质,也是最重要的溶剂.常温下某电解质溶解在水中后,溶液中的c(H+)=10-9mol?L-1,则该电解质可能是
A. CuSO4 B. HCl C. Na2S D.NaOH E.K2SO4
(2)已知次氯酸是比碳酸还弱的酸,要使新制稀氯水中的c(HClO)增大,可以采取的措施为(至少回答两种)
(3)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性.
①浓度为1.0×10-3mol?L-1的氨水b L;②c(OH-)=1.0×10-3mol?L-1的氨水c L;③c(OH-)=1.0×10-3mol?L-1的氢氧化钡溶液d L.则a、b、c、d之间的关系是:
(4)强酸制弱酸是水溶液中的重要经验规律.
①已知HA、H2B是两种弱酸,存在以下关系:H2B(少量)+2A-=B2-+2HA,则A-、B2-、HB-三种阴离子结合H+的难易顺序为
②某同学将H2S通入CuSO4溶液中发现生成黑色沉淀,查阅资料并在老师的指导下写出了化学方程式:H2S+CuSO4=CuS↓+H2SO4,但这位同学陷入了困惑:这不成了弱酸制取强酸了吗?请你帮助解释
(5)已知:H2A═H++HA-、HA-?H++A2-,常温下,0.1mol?L-1的NaH A溶液其pH=2,则0.1mol?L-1的H2A溶液中氢离子浓度的大小范围是:
(6)己知:Ksp(AgCl)=1.8×10-10mol?L-1,向50mL 0.018mol?L-1的AgNO3溶液中加入相同体积0.020mol?L-1的盐酸,则c(Ag+)=
查看习题详情和答案>>
(1)水是极弱的电解质,也是最重要的溶剂.常温下某电解质溶解在水中后,溶液中的c(H+)=10-9mol?L-1,则该电解质可能是
CD
CD
(填序号).A. CuSO4 B. HCl C. Na2S D.NaOH E.K2SO4
(2)已知次氯酸是比碳酸还弱的酸,要使新制稀氯水中的c(HClO)增大,可以采取的措施为(至少回答两种)
再通入氯气、加入碳酸盐、加入次氯酸钠
再通入氯气、加入碳酸盐、加入次氯酸钠
.(3)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性.
①浓度为1.0×10-3mol?L-1的氨水b L;②c(OH-)=1.0×10-3mol?L-1的氨水c L;③c(OH-)=1.0×10-3mol?L-1的氢氧化钡溶液d L.则a、b、c、d之间的关系是:
b>a=d>c
b>a=d>c
.(4)强酸制弱酸是水溶液中的重要经验规律.
①已知HA、H2B是两种弱酸,存在以下关系:H2B(少量)+2A-=B2-+2HA,则A-、B2-、HB-三种阴离子结合H+的难易顺序为
A->B2->HB-
A->B2->HB-
.②某同学将H2S通入CuSO4溶液中发现生成黑色沉淀,查阅资料并在老师的指导下写出了化学方程式:H2S+CuSO4=CuS↓+H2SO4,但这位同学陷入了困惑:这不成了弱酸制取强酸了吗?请你帮助解释
铜离子和硫化氢只所以能生成硫化铜沉淀,是因为硫化铜既难溶于水又难溶于酸
铜离子和硫化氢只所以能生成硫化铜沉淀,是因为硫化铜既难溶于水又难溶于酸
.(5)已知:H2A═H++HA-、HA-?H++A2-,常温下,0.1mol?L-1的NaH A溶液其pH=2,则0.1mol?L-1的H2A溶液中氢离子浓度的大小范围是:
0.1mol/L<c(H+)<0.11mol/L
0.1mol/L<c(H+)<0.11mol/L
;NaHA溶液中各种离子浓度大小关系为c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
.(6)己知:Ksp(AgCl)=1.8×10-10mol?L-1,向50mL 0.018mol?L-1的AgNO3溶液中加入相同体积0.020mol?L-1的盐酸,则c(Ag+)=
1.8×10-7mol/L
1.8×10-7mol/L
,此时所得混合溶液的pH=2
2
.