摘要:记住溶质的质量分数的定义.熟练掌握有关溶质质量分数的计算.
网址:http://m.1010jiajiao.com/timu_id_4360325[举报]
小彬同学想测定黄铜(含Cu、Zn)和硬铝(含铝、铜、镁、锰)两种合金中铜的质量分数,实验室只提供了一瓶末标明溶质质量分数的稀盐酸和必要的仪器.
(1)请你判断出他能测出铜的质量分数的合金是 .
(2)小彬取该合金的粉末32.5g,与足量该盐酸充分反应后,经测定产生了0.4g气体,请你帮助他计算出该合金中铜的质量分数为多少?
(3)若盐酸恰好用完,则计算盐酸中溶质的质量分数时还需要提供和测出的数据是 (选填序号)
A.参加反应的金属质量;B.稀盐酸的质量
C.生成的气体质量;D.取用的合金质量. 查看习题详情和答案>>
(1)请你判断出他能测出铜的质量分数的合金是
(2)小彬取该合金的粉末32.5g,与足量该盐酸充分反应后,经测定产生了0.4g气体,请你帮助他计算出该合金中铜的质量分数为多少?
(3)若盐酸恰好用完,则计算盐酸中溶质的质量分数时还需要提供和测出的数据是
A.参加反应的金属质量;B.稀盐酸的质量
C.生成的气体质量;D.取用的合金质量. 查看习题详情和答案>>
某同学利用一黑色粉末(含氧化铜、碳粉、铁粉中的一种或多种)和未知溶质的质量分数的稀硫酸,做如下探究:将ag黑色粉末加入到盛有50g该稀硫酸的烧杯中,充分反应后称得烧杯内物质的质量为(49.8+a)g.他对实验的推理不正确的是( )
| A、反应后不可能得到红色固体 | B、若反应后黑色粉末无剩余,则黑色粉末一定不含有碳粉 | C、黑色粉末中含铁粉,加入黑色粉末质量一定为5.6g | D、该稀硫酸中溶质的质量分数不低于19.6% |
化学是一门以实验为基础的科学,通过实验可以学习科学探究的方法.现有一份由碳酸钠和氯化钠组成的固体样品,质量为m1g.小明设计了图中的装置,请你参与探究.
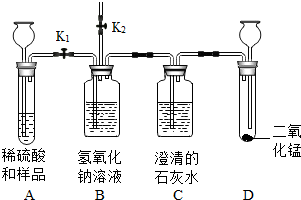
【实验目的】探究碳酸钠的化学性质并测定样品中碳酸钠的质量分数.
【查阅资料】碳酸钠能与稀硫酸发生反应,生成硫酸钠、二氧化碳和水.
【实验步骤】
①关闭止水夹K2,打开止水夹K1.向装有样品的A装置内加入适量的稀硫酸,充分反应后,B装置的质量增重m2g,C装置中的澄清石灰水不变浑浊.
②关闭止水夹K1,打开止水夹K2,使B装置与空气连通.向D装置内加入适量的过氧化氢溶液充分反应(确保溶液浸没长颈漏斗下端管口).请回答:
(1)实验前需检查装置的 .
(2)判断样品中含有碳酸钠的实验现象为 .
(3)样品中碳酸钠的质量分数的表达式为 .
(4)在整个反应过程中,B装置内发生反应的化学方程式为 .
【实验拓展】反应结束后,B装置溶液中溶质的组成有多种情况,其中的一种是只含有氢氧化钠,还有的情况是: .你怎样验证溶质只含有氢氧化钠的这种情况: .
查看习题详情和答案>>

【实验目的】探究碳酸钠的化学性质并测定样品中碳酸钠的质量分数.
【查阅资料】碳酸钠能与稀硫酸发生反应,生成硫酸钠、二氧化碳和水.
【实验步骤】
①关闭止水夹K2,打开止水夹K1.向装有样品的A装置内加入适量的稀硫酸,充分反应后,B装置的质量增重m2g,C装置中的澄清石灰水不变浑浊.
②关闭止水夹K1,打开止水夹K2,使B装置与空气连通.向D装置内加入适量的过氧化氢溶液充分反应(确保溶液浸没长颈漏斗下端管口).请回答:
(1)实验前需检查装置的
(2)判断样品中含有碳酸钠的实验现象为
(3)样品中碳酸钠的质量分数的表达式为
(4)在整个反应过程中,B装置内发生反应的化学方程式为
【实验拓展】反应结束后,B装置溶液中溶质的组成有多种情况,其中的一种是只含有氢氧化钠,还有的情况是:
 请根据图曲线回答:
请根据图曲线回答: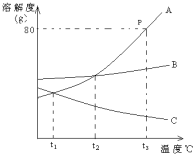 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: