摘要:已知随机变量服从正态分布..则( ) A. B. C. D.
网址:http://m.1010jiajiao.com/timu_id_4339018[举报]
常温下,将FeCl3溶液和KI溶液混合,发生如下反应:
2Fe3++2I-?2Fe2++I2
某研究小组为了证明FeCl3溶液和KI溶液的反应存在一定限度,设计了如下实验:取5mL 0.1mol?L-1 KI溶液,滴加0.1mol?L-1 FeCl3溶液5~6滴,充分反应后溶液呈黄褐色,加入2mL CCl4溶液,振荡后静置,取上层溶液,滴加KSCN试剂,观察实验现象.
已知:v(正)=k?cm(I-)?cn(Fe3+)(k为常数)
根据以上信息回答下列问题:
(1)能够证明反应存在限度的现象是 .加入四氯化碳的作用是 .
(2)甲同学按上述步骤进行实验,结果并未观察到预期现象,推测可能原因是反应后溶液中Fe3+浓度过低.为此,甲又做了下列对比实验,实验结果记录如下:
分析实验记录,甲认为导致Fe3+浓度过低的原因是 ;乙同学结合平衡移动的知识,认为还有一个原因是 .
(3)该反应的平衡常数表达式为 .
(4)已知改变I-、Fe3+的浓度,正反应速率对应数值如下表所示:
分析表中数据,I-浓度对反应速率的影响 Fe3+浓度对反应速率的影响(填“大于”、“小于”或“等于”),理由是(写出计算过程) .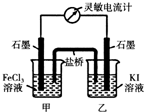
(5)现将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池
①能说明反应达到平衡的标志是 (填序号).
a.电流计读数为零 b.电流计指针不再偏转且不为零
c.电流计指针偏转角度最大 d.甲烧杯中溶液颜色不再改变
②反应达平衡后,向甲中加入适量FeCl2固体,此时 (填“甲“或“乙”)中石墨电极为负极,对应的电极反应方程式为 .
查看习题详情和答案>>
2Fe3++2I-?2Fe2++I2
某研究小组为了证明FeCl3溶液和KI溶液的反应存在一定限度,设计了如下实验:取5mL 0.1mol?L-1 KI溶液,滴加0.1mol?L-1 FeCl3溶液5~6滴,充分反应后溶液呈黄褐色,加入2mL CCl4溶液,振荡后静置,取上层溶液,滴加KSCN试剂,观察实验现象.
已知:v(正)=k?cm(I-)?cn(Fe3+)(k为常数)
根据以上信息回答下列问题:
(1)能够证明反应存在限度的现象是
(2)甲同学按上述步骤进行实验,结果并未观察到预期现象,推测可能原因是反应后溶液中Fe3+浓度过低.为此,甲又做了下列对比实验,实验结果记录如下:
| 氯化铁溶液用量 | 10滴 | 20滴 | 30滴 | 2mL | 3mL | 4mL |
| 萃取后上层溶液颜色 | 黄色 | 黄色 | 黄色 | 较深黄色 | 黄色略带红色 | 黄红色 |
| 加入KSCN溶液后颜色 | 不变红 | 不变红 | 略变红 | 偏血红色 | 血红色 | 血红色 |
(3)该反应的平衡常数表达式为
(4)已知改变I-、Fe3+的浓度,正反应速率对应数值如下表所示:
| c(I-)/mol?L-1 | c(Fe3+)/mol?L-1 | v/mol?L-1?s-1 | |
| ① | 0.20 | 0.80 | 0.032k |
| ② | 0.60 | 0.40 | 0.144k |
| ③ | 0.80 | 0.20 | 0.128k |

(5)现将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池
①能说明反应达到平衡的标志是
a.电流计读数为零 b.电流计指针不再偏转且不为零
c.电流计指针偏转角度最大 d.甲烧杯中溶液颜色不再改变
②反应达平衡后,向甲中加入适量FeCl2固体,此时
有体积相等的甲、乙两个密闭容器,如图1所示,甲的活塞可以随意推拉,乙为恒容.向甲容器中充入等物质的量的气体A和B,一定温度下发生反应,达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时问变化的曲线如图2所示.
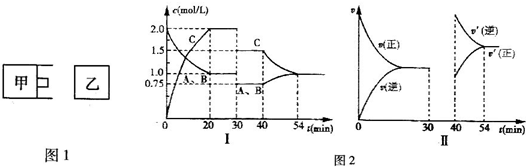
(1)0~20min A的平均反应速率为
(2)①30min时改变了一种反应条件,所改变的条件和判断的理由是
(3)请在图2的Ⅱ图中补画出30~40min正、逆反应速率关于时间变化的曲线.
(4)若向乙容器中充入一定量的A、B、C,使A、B起始浓度均为a mol/L,C为3.5mol/L,一定温度下达到平衡时,C的浓度为2.0mol/L,则a=
查看习题详情和答案>>

(1)0~20min A的平均反应速率为
0.05mol/(L?min)
0.05mol/(L?min)
.(2)①30min时改变了一种反应条件,所改变的条件和判断的理由是
增大体积为原来的
倍;30min时正、逆反应速率降低,A、C的浓度瞬时降低,反应仍处于平衡状态,A的浓度由1mol/L变为0.75mol/L
| 4 |
| 3 |
增大体积为原来的
倍;30min时正、逆反应速率降低,A、C的浓度瞬时降低,反应仍处于平衡状态,A的浓度由1mol/L变为0.75mol/L
;②已知该反应的正反应为放热反应,40min时改变了一种反应条件,所改变的条件和判断的理由是| 4 |
| 3 |
升高温度;40min时改变的条件,瞬间A、C的浓度不变,正、逆速率都增大,平衡向逆反应移动
升高温度;40min时改变的条件,瞬间A、C的浓度不变,正、逆速率都增大,平衡向逆反应移动
.(3)请在图2的Ⅱ图中补画出30~40min正、逆反应速率关于时间变化的曲线.
(4)若向乙容器中充入一定量的A、B、C,使A、B起始浓度均为a mol/L,C为3.5mol/L,一定温度下达到平衡时,C的浓度为2.0mol/L,则a=
0.25
0.25
.在25℃、101kPa下,白磷(化学式为P4)、红磷(化学式为P)燃烧的热化学方程式分别为:
P4(s)+5O2(g)=P4O10(s);△H=-3093.2kJ?mol-1
4P(s)+5O2(g)=P4O10(s);△H=-2954.0kJ?mol-1
由此判断下列说法正确的是( )
P4(s)+5O2(g)=P4O10(s);△H=-3093.2kJ?mol-1
4P(s)+5O2(g)=P4O10(s);△H=-2954.0kJ?mol-1
由此判断下列说法正确的是( )
查看习题详情和答案>>
 已知:在热力学标准态(298K、1.01×105Pa)下,由稳定的单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H).下图为氧族元素氢化物a、b、c、d的生成热数据示意图.试回答下列问题:
已知:在热力学标准态(298K、1.01×105Pa)下,由稳定的单质发生反应生成1mol化合物的反应热叫该化合物的生成热(△H).下图为氧族元素氢化物a、b、c、d的生成热数据示意图.试回答下列问题:(1)写出氧族元素中含有18e-的两种氢化物的电子式


(2)请你归纳:非金属元素氢化物的稳定性与氢化物的生成热△H的关系
非金属元素氢化物越稳定,△H越小,反之亦然
非金属元素氢化物越稳定,△H越小,反之亦然
(3)写出硫化氢在热力学标准态下,发生分解反应的热化学反应方程式:
H2S(g)=S(s)+H2(g);△H=+20kJ/mol
H2S(g)=S(s)+H2(g);△H=+20kJ/mol
.