摘要:10.在配制250ml 2.0mol/L NaCl溶液的实验中.必须使用的仪器是
网址:http://m.1010jiajiao.com/timu_id_433388[举报]
2009.05
一、选择题(本题包括30小题,每小题1分,共30分。)
题号
1
2
3
4
5
6
7
8
9
10
答案
A
C
B
A
B
B
D
B
A
A
题号
11
12
13
14
15
16
17
18
19
20
答案
C
D
C
C
D
C
D
C
B
D
题号
21
22
23
24
25
26
27
28
29
30
答案
C
C
B
C
B
A
B
A
B
D
二、选择题(本题包括25小题, 31~45题为必做题;46~55题为选做题,其中46~50题为“化学与生活”模块内容的试题,51~55为“化学与技术”模块内容的试题,每个考生只能选择一个模块的试题。每小题2分,共40分。)
题号
31
32
33
34
35
36
37
38
39
40
答案
C
C
D
D
C
A
A
D
B
A
题号
41
42
43
44
45
46
47
48
49
50
答案
D
C
C
B
A
D
B
C
B
B
三、选择题(本题包括10小题,每小题3分,共30分。每题至少有2个选项符合题意,全选对得3分,少选且正确得1分,未选、错选得0分.)
题号
56
57
58
59
60
61
62
63
64
65
答案
BC
CD
AD
ABC
BD
ACD
AD
AC
ABD
AC
过碳酸钠俗称固体双氧水,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,它的制备原理和路线如下:2Na2CO3+3H2O2=2Na2CO3?3H2O2△H<0
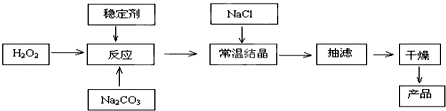
回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是
(2)下列物质可使过碳酸钠较快失效的是
a.MnO2 b.H2S c.稀硫酸 d.NaHCO3
(3)加入NaCl的实验操作名称是
(4)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与Fe3+生成稳定的配合物,Fe3+对反应的不良影响是
(5)反应的最佳温度控制在15℃~20℃,温度偏高时造成产率低可能是
(6)以上抽滤过程中遗漏了一步操作,造成所得产品纯度偏低,该步操作的名称是
(7)准确称取0.2000g 过碳酸钠样品于250mL 锥形瓶中,加50mL 蒸馏水溶解,再加50mL 2.0mol?L-1 H2SO4,用2.000×10-2 mol?L-1 KMnO4 标准溶液滴定至终点时消耗30.00mL,则产品中H2O2的质量分数为
查看习题详情和答案>>

回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是
强氧化性
强氧化性
.(2)下列物质可使过碳酸钠较快失效的是
abc
abc
.a.MnO2 b.H2S c.稀硫酸 d.NaHCO3
(3)加入NaCl的实验操作名称是
盐析
盐析
;作用是降低2Na2CO3?3H2O2溶解度,析出更多晶体
降低2Na2CO3?3H2O2溶解度,析出更多晶体
.(4)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与Fe3+生成稳定的配合物,Fe3+对反应的不良影响是
催化双氧水的分解
催化双氧水的分解
.(5)反应的最佳温度控制在15℃~20℃,温度偏高时造成产率低可能是
温度高时双氧水易分解
温度高时双氧水易分解
,温度偏低时造成产率低的可能是温度低时反应缓慢
温度低时反应缓慢
.(6)以上抽滤过程中遗漏了一步操作,造成所得产品纯度偏低,该步操作的名称是
洗涤
洗涤
;进行该操作的方法是:向置于过滤器上的沉淀加蒸馏水至刚好淹没沉淀,静置,待水自然流出后,再重复操作两到三次
向置于过滤器上的沉淀加蒸馏水至刚好淹没沉淀,静置,待水自然流出后,再重复操作两到三次
.(7)准确称取0.2000g 过碳酸钠样品于250mL 锥形瓶中,加50mL 蒸馏水溶解,再加50mL 2.0mol?L-1 H2SO4,用2.000×10-2 mol?L-1 KMnO4 标准溶液滴定至终点时消耗30.00mL,则产品中H2O2的质量分数为
25.50%
25.50%
.










