摘要:20. 第三周期IA族 .(2) H2O2 (3) H2S+ OH-==HS-+ H2O .(4)① H++HSO32-===SO2+H2O ② Na2SO3 . 亚硫酸 (5). NaH+H2O==H2+NaOH
网址:http://m.1010jiajiao.com/timu_id_428733[举报]
元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表是元素周期表的一部分,请依据该表回答问题.
(1)第三周期IA族元素的原子结构示意图是
 ,该元素与同周期VIIA族元素组成的化合物类型是
,该元素与同周期VIIA族元素组成的化合物类型是
(2)第三周期元素的最高价氧化物对应水化物中,酸性最强的是
(3)有人认为形成化合物最多的不是IVA的碳元素,而是另一种短周期元素,请你根据已学化学知识判断这一元素是
(4)由H、N、O三种元素组成的离子化合物X,在210℃时可分解生成N元素的一种气态氧化物Y和水.已知 40g X完全分解可生成11.2L(标准状况)Y,则Y的化学式为
查看习题详情和答案>>
| 族 周期 |
IA | 0 | ||||||
| 1 | H | IIA | IIIA | IVA | VA | VIA | VIIA | He |
| 2 | Li | Be | B | C | N | O | F | Ne |
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar |


离子化合物
离子化合物
;(2)第三周期元素的最高价氧化物对应水化物中,酸性最强的是
HClO4
HClO4
(填化学式,下同);碱性最强的是NaOH
NaOH
;具有两性的是Al(OH)3
Al(OH)3
,其与氢氧化钠溶液反应的化学方程式为A1(OH)3+NaOH=NaA1O2+2H2O
A1(OH)3+NaOH=NaA1O2+2H2O
;(3)有人认为形成化合物最多的不是IVA的碳元素,而是另一种短周期元素,请你根据已学化学知识判断这一元素是
H
H
(填元素符号);(4)由H、N、O三种元素组成的离子化合物X,在210℃时可分解生成N元素的一种气态氧化物Y和水.已知 40g X完全分解可生成11.2L(标准状况)Y,则Y的化学式为
N2O
N2O
.
元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表是元素周期表的一部分,请依据该表回答问题.
(1)第三周期IA族元素的原子结构示意图是______,该元素与同周期VIIA族元素组成的化合物类型是______;
(2)第三周期元素的最高价氧化物对应水化物中,酸性最强的是______(填化学式,下同);碱性最强的是______;具有两性的是______,其与氢氧化钠溶液反应的化学方程式为______;
(3)有人认为形成化合物最多的不是IVA的碳元素,而是另一种短周期元素,请你根据已学化学知识判断这一元素是______(填元素符号);
(4)由H、N、O三种元素组成的离子化合物X,在210℃时可分解生成N元素的一种气态氧化物Y和水.已知 40g X完全分解可生成11.2L(标准状况)Y,则Y的化学式为______.
查看习题详情和答案>>
| 族 周期 | IA | |||||||
| 1 | H | IIA | IIIA | IVA | VA | VIA | VIIA | He |
| 2 | Li | Be | B | C | N | O | F | Ne |
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar |
(2)第三周期元素的最高价氧化物对应水化物中,酸性最强的是______(填化学式,下同);碱性最强的是______;具有两性的是______,其与氢氧化钠溶液反应的化学方程式为______;
(3)有人认为形成化合物最多的不是IVA的碳元素,而是另一种短周期元素,请你根据已学化学知识判断这一元素是______(填元素符号);
(4)由H、N、O三种元素组成的离子化合物X,在210℃时可分解生成N元素的一种气态氧化物Y和水.已知 40g X完全分解可生成11.2L(标准状况)Y,则Y的化学式为______.
查看习题详情和答案>>
下表是部分短周期元素的原子半径及主要化合价:
试回答下列问题:(1)七种元素中原子半径最大的元素在周期表中位置是
(2)X可与R按1:1的原子个数比形成化合物甲,甲中存在的化学键有
 .
.
查看习题详情和答案>>
| 元素代号 | W | R | X | Y | Z | Q | M |
| 原子半径/nm | 0.037 | 0.186 | 0.074 | 0.075 | 0.077 | 0.110 | 0.160 |
| 主要化合价 | +1 | +1 | -2 | -3,+5 | +2、+4 | -3、+5 | +2 |
第三周期IA族
第三周期IA族
;M在Z的最高价氧化物中燃烧的化学方程式为2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
.
| ||
(2)X可与R按1:1的原子个数比形成化合物甲,甲中存在的化学键有
离子键和共价键
离子键和共价键
;X可与W组成含18电子的化合物乙,则乙的电子式为

某教师在上《元素周期表》复习课时,组织了一个“介绍自己”的活动: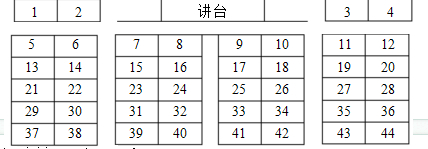
我们班级中共有44位同学,分为8个小组,按从左到右分别为IA、IIA…VIIA、0族,从上到下分别为第一、二…六周期.座位上的每一位同学对应一种元素,请在下列问题中符合要求的同学向大家介绍自己.
请你一起思考并回答下列问题:
(1)第三周期IVA族的元素对应座位号是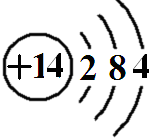
 .
.
(2)座位号为22的元素在元素周期表中的位置是
(3)比较座位号为18、19对应的元素的非金属性强弱,请用离子方程式表示
(4)课堂中有学生提出,这样的安排会导致他们没有对应的元素,则学生对应的座位号是
查看习题详情和答案>>

我们班级中共有44位同学,分为8个小组,按从左到右分别为IA、IIA…VIIA、0族,从上到下分别为第一、二…六周期.座位上的每一位同学对应一种元素,请在下列问题中符合要求的同学向大家介绍自己.
请你一起思考并回答下列问题:
(1)第三周期IVA族的元素对应座位号是
16
16
,原子结构示意图为

(2)座位号为22的元素在元素周期表中的位置是
第四周期第IIA族
第四周期第IIA族
.(3)比较座位号为18、19对应的元素的非金属性强弱,请用离子方程式表示
Cl2+S2-=S↓+2Cl-或Cl2+H2S=2H++S↓+2Cl-
Cl2+S2-=S↓+2Cl-或Cl2+H2S=2H++S↓+2Cl-
.(4)课堂中有学生提出,这样的安排会导致他们没有对应的元素,则学生对应的座位号是
2,3
2,3
.已知X、Y、Z、W四种元素分布在元素周期表中的三个不同短周期元素里,且原子序数依次增大.X、W同主族,Y、Z为同周期的相邻元素.W原子的质子数等于Y、Z原子最外层电子数之和.Y的氢化物分子中有3个共价键.Z原子最外层电子数是次外层电子数的3倍.试推断:
(1)写出X、Y的元素符号:X
(2)W在元素周期表中的位置是

(3)由X、Y、Z所形成的离子化合物的化学式是
(4)用电子式表示Y的氢化物的形成过程
 .
.
查看习题详情和答案>>
(1)写出X、Y的元素符号:X
H
H
、YN
N
;(2)W在元素周期表中的位置是
第三周期IA族
第三周期IA族
;Z的原子结构示意图

(3)由X、Y、Z所形成的离子化合物的化学式是
NH4NO3
NH4NO3
,它与W的最高价氧化物的水化物的溶液反应时的离子方程式是NH4-+OH-=NH3?H2O
NH4-+OH-=NH3?H2O
;(4)用电子式表示Y的氢化物的形成过程

