摘要:2Fe + 3Cl22FeCl3.S + Fe FeS .根据铁被氧化程度的不同(Fe3+.Fe2+).可判断氧化性:Cl2>S.同理.当不同的还原剂与同一氧化剂反应时.氧化剂被还原的程度越大.还原剂的还原性就越强.(4)根据反应方程式进行比较氧化剂+还原剂=还原产物+氧化产物氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物 简记:左>右(5)根据元素周期律进行比较一般地.氧化性:上>下.右>左,还原性:下>上.左>右.(6)某些氧化剂的氧化性或还原剂的还原性与下列因素有关:温度:如热的浓硫酸的氧化性比冷的浓硫酸的氧化性强.浓度:如浓硝酸的氧化性比稀硝酸的强.酸碱性:如中性环境中NO3-不显氧化性,酸性环境中NO3-显氧化性,又如KMnO4溶液的氧化性随溶液的酸性增强而增强.注意:物质的氧化性或还原性的强弱只决定于得到或失去电子的难易.与得失电子的多少无关.[注意]:中学化学中提及的“化 名目繁多.要判别它们分属何种变化.必须了解其过程.请你根据下列知识来指出每一种“化 发生的是物理变化还是化学变化.
网址:http://m.1010jiajiao.com/timu_id_427880[举报]
已知有以下反应:
①2Fe+3Cl2![]() 2FeCl3
2FeCl3
②Fe+S![]() FeS
FeS
③Na2S+I2====2NaI+S
则Cl2、S、I2的氧化性由强到弱的顺序为( )
A.Cl2、I2、S B.Cl2、S、I2 C.S、I2、Cl2 D.I2、Cl2、S
查看习题详情和答案>>
已知A、B、C、D两种短周期元素,分别属于不同的主族,其原子序数依次增大,其中A与D、B与C的原子的最外层电子数之和均为9,A原子的最外层与次外层电子数相等,A、B、C、D中只有两种金属元素.试回答下列问题:
(1)A的元素符号为______,C的氢化物的化学式为______.
(2)为比较C与D的单质的氧化性强弱,可设计实验以证实,则该实验所依据的反应的化学方程式为______ FeS,2Fe+3Cl2 2FeCl3(或H2S+Cl2═S↓+2HCl)
2FeCl3(或H2S+Cl2═S↓+2HCl)
 查看习题详情和答案>>
查看习题详情和答案>>
(1)A的元素符号为______,C的氢化物的化学式为______.
(2)为比较C与D的单质的氧化性强弱,可设计实验以证实,则该实验所依据的反应的化学方程式为______ FeS,2Fe+3Cl2
 2FeCl3(或H2S+Cl2═S↓+2HCl)
2FeCl3(或H2S+Cl2═S↓+2HCl) 查看习题详情和答案>>
查看习题详情和答案>>
已知A、B、C、D两种短周期元素,分别属于不同的主族,其原子序数依次增大,其中A与D、B与C的原子的最外层电子数之和均为9,A原子的最外层与次外层电子数相等,A、B、C、D中只有两种金属元素.试回答下列问题:
(1)A的元素符号为______,C的氢化物的化学式为______.
(2)为比较C与D的单质的氧化性强弱,可设计实验以证实,则该实验所依据的反应的化学方程式为______ FeS,2Fe+3Cl2 2FeCl3(或H2S+Cl2═S↓+2HCl)
2FeCl3(或H2S+Cl2═S↓+2HCl)
 查看习题详情和答案>>
查看习题详情和答案>>
(1)A的元素符号为______,C的氢化物的化学式为______.
(2)为比较C与D的单质的氧化性强弱,可设计实验以证实,则该实验所依据的反应的化学方程式为______ FeS,2Fe+3Cl2
 2FeCl3(或H2S+Cl2═S↓+2HCl)
2FeCl3(或H2S+Cl2═S↓+2HCl) 查看习题详情和答案>>
查看习题详情和答案>>
类推思维是化学解题中常用的一种思维方法,下列有关反应方程式(或离子方程式)的类推正确的是
| 已知 | 类推 | |
| A | 将Fe加入CuSO4溶液中:Fe+ =Cu+Fe2+ =Cu+Fe2+ | 将Na加入到CuSO4溶液中:2Na+ =Cu+2Na+ =Cu+2Na+ |
| B | 稀硫酸与Ba(OH)2溶液反应至溶液呈中性:2H++S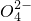 +Ba++2OH-=BaSO4↓+2H2O +Ba++2OH-=BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应呈中性:2H++S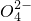 +Ba++2OH-=BaSO4↓+2H2O +Ba++2OH-=BaSO4↓+2H2O |
| C | 铁和氯气反应2Fe+3Cl2 2FeCl3 2FeCl3 | 铁和单质反应2Fe+3I2 2FeI3 2FeI3 |
| D | 向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
- A.A
- B.B
- C.C
- D.D