摘要:18.有关元素X.Y.Z.D.E的信息如下元 素有关信息X
网址:http://m.1010jiajiao.com/timu_id_426616[举报]
(8分)X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
若Z元素原子的最外层电子数是电子层数的2倍
(1)W在周期表中的位置为 。
(2)Y和Z元素形成的氢化物的沸点高低比较为 ,原因是 。
(3)含X元素的四核10电子微粒的电子式为 。
(4)写出铜和X的最高价氧化物水化物的稀溶液反应的离子方程式为 。
(5)W最高价氧化物水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol电子转移时,共产生9 mol气体,写出该反应的化学方程式 。
(8分)X、Y、Z、W四种短周期元素在周期表中的位置关系如图:

若Z元素原子的最外层电子数是电子层数的2倍
(1)W在周期表中的位置为 。
(2)Y和Z元素形成的氢化物的沸点高低比较为 ,原因是 。
(3)含X元素的四核10电子微粒的电子式为 。
(4)写出铜和X的最高价氧化物水化物的稀溶液反应的离子方程式为 。
(5)W最高价氧化物水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol电子转移时,共产生9 mol气体,写出该反应的化学方程式 。
查看习题详情和答案>>
(8分)X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
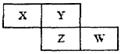
若Z元素原子的最外层电子数是电子层数的2倍
(1)W在周期表中的位置为 。
(2)Y和Z元素形成的氢化物的沸点高低比较为 ,原因是 。
(3)含X元素的四核10电子微粒的电子式为 。
(4)写出铜和X的最高价氧化物水化物的稀溶液反应的离子方程式为 。
(5)W最高价氧化物水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol电子转移时,共产生9 mol气体,写出该反应的化学方程式 。

若Z元素原子的最外层电子数是电子层数的2倍
(1)W在周期表中的位置为 。
(2)Y和Z元素形成的氢化物的沸点高低比较为 ,原因是 。
(3)含X元素的四核10电子微粒的电子式为 。
(4)写出铜和X的最高价氧化物水化物的稀溶液反应的离子方程式为 。
(5)W最高价氧化物水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol电子转移时,共产生9 mol气体,写出该反应的化学方程式 。
T、X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增,其相关信息如下表:
| 元素 | 相关信息 |
| T | T原子所处的周期数、族序数分别与其原子序数相等 |
| X | X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 |
| Z | Z的基态原子价电子排布为 |
| Q | 在该元素所在周期中,Q的基态原子的第一电离能最小 |
| R | 3p能级上有1个电子 |
| W | W的一种核素的质量数为65,中子数为36 |
(2)X与Y原子结合形成的X3Y4晶体,其硬度比金刚石大,则X3Y4晶体中含有 键(填“共价”、“离子”、“金属”),属于 晶体(填“分子”、“原子”、“离子”)。
(3)W的基态原子的核外电子排布式为 。利用电解可提纯W物质,在该电解反应中阳极物质是 ,阴极物质是 ,电解质溶液是 。
(4)T、X两种元素组成的一种化合物M是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则M分子中
 键和
键和 键的个数比为 。在T—Y、T—Z两种共价键中,键长较长的是 。
键的个数比为 。在T—Y、T—Z两种共价键中,键长较长的是 。(5)已知25℃、101 kPa条件下:
4R(s)+3Z2(
 g)
g)4R(s)+2Z3(g)
则16g Z2(g)完全转化为Z3(g)的△H= . 查看习题详情和答案>>
T、X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增,其相关信息如下表:
(1)X、Y、Q三种元素的电负性由大到小的顺序是 (用元素符号表示)。
(2)X与Y原子结合形成的X3Y4晶体,其硬度比金刚石大,则X3Y4晶体中含有 键(填“共价”、“离子”、“金属”),属于 晶体(填“分子”、“原子”、“离子”)。
(3)W的基态原子的核外电子排布式为 。利用电解可提纯W物质,在该电解反应中阳极物质是 ,阴极物质是 ,电解质溶液是 。
(4)T、X两种元素组成的一种化合物M是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则M分子中 键和
键和 键的个数比为 。在T—Y、T—Z两种共价键中,键长较长的是 。
键的个数比为 。在T—Y、T—Z两种共价键中,键长较长的是 。
(5)已知25℃、101 kPa条件下:
4R(s)+3Z2( g)
g) 2R2Z3(s) △H=-2834.9 kJ/mol
4R(s)+2Z3(g) 2R2Z3(s) △H=-3119.1 kJ/mol
则16g Z2(g)完全转化为Z3(g)的△H= .
| 元素 | 相关信息 |
| T | T原子所处的周期数、族序数分别与其原子序数相等 |
| X | X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 |
| Z | Z的基态原子价电子排布为 |
| Q | 在该元素所在周期中,Q的基态原子的第一电离能最小 |
| R | 3p能级上有1个电子 |
| W | W的一种核素的质量数为65,中子数为36 |
(2)X与Y原子结合形成的X3Y4晶体,其硬度比金刚石大,则X3Y4晶体中含有 键(填“共价”、“离子”、“金属”),属于 晶体(填“分子”、“原子”、“离子”)。
(3)W的基态原子的核外电子排布式为 。利用电解可提纯W物质,在该电解反应中阳极物质是 ,阴极物质是 ,电解质溶液是 。
(4)T、X两种元素组成的一种化合物M是重要的化工原料,常把它的产量作为衡量石油化工发展水平的标志,则M分子中
 键和
键和 键的个数比为 。在T—Y、T—Z两种共价键中,键长较长的是 。
键的个数比为 。在T—Y、T—Z两种共价键中,键长较长的是 。(5)已知25℃、101 kPa条件下:
4R(s)+3Z2(
 g)
g)4R(s)+2Z3(g)
则16g Z2(g)完全转化为Z3(g)的△H= .