摘要:(熟记课本中有关实验的现象和化学反应方程式)
网址:http://m.1010jiajiao.com/timu_id_4240813[举报]
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室从海藻中提取碘的流程如下:
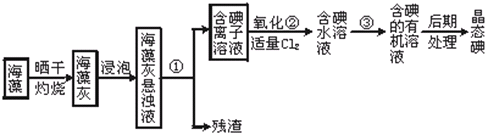
(1)指出提取碘的过程中有关实验操作名称 ① ③
(2)写出过程②中有关反应的离子方程式
(3)提取碘的过程中,可供选择的有机试剂是
A.乙酸 B.苯 C.四氯化碳 D.酒精
查看习题详情和答案>>

(1)指出提取碘的过程中有关实验操作名称 ①
(2)写出过程②中有关反应的离子方程式
(3)提取碘的过程中,可供选择的有机试剂是
A.乙酸 B.苯 C.四氯化碳 D.酒精
| 有机试剂 | 酒精 | 四氯化碳 | 苯 | 乙酸 |
| 毒性 | 无 | 无 | 有 | 无 |
| 水溶性 | 与水以任意比互溶 | 与水互不相溶 | 与水互不相溶 | 与水以任意比互溶 |
海洋植物如海带海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海洋中提取碘的流程如下:

(1)指出提取的过程中有关实验操作名称:①
(2)提取碘的过程中,可供选择的有机溶剂是
A.水、酒精 B.四氯化碳、苯 C.汽油、酒精.
查看习题详情和答案>>

(1)指出提取的过程中有关实验操作名称:①
过滤
过滤
;③萃取
萃取
.(2)提取碘的过程中,可供选择的有机溶剂是
B
B
.A.水、酒精 B.四氯化碳、苯 C.汽油、酒精.
海藻中提取碘的流程如图1:

(1)指出提取碘的过程中有关实验操作③的名称:
(2)在3mL碘水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出图3实验装置中的错误之处.(加热装置烧杯下已垫石棉网)
①
②
查看习题详情和答案>>

(1)指出提取碘的过程中有关实验操作③的名称:
萃取、分液
萃取、分液
;写出过程②中有关反应的离子方程式Cl2+2I-═2Cl-+I2
Cl2+2I-═2Cl-+I2
.(2)在3mL碘水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是
D
D
.(注:图2试管中深色区为紫红色溶液)(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出图3实验装置中的错误之处.(加热装置烧杯下已垫石棉网)
①
温度计下端的水银球不能插入溶液中,应放在支管口
温度计下端的水银球不能插入溶液中,应放在支管口
;②
冷凝管中水流方向相反了
冷凝管中水流方向相反了
. 海藻中提取碘的流程如图:
海藻中提取碘的流程如图:(1)指出提取碘的过程中有关实验操作名称:①
过滤
过滤
,③萃取
萃取
;写出过程②中有关反应的离子方程式Cl2+2I-═2Cl-+I2
Cl2+2I-═2Cl-+I2
(2)在提取碘的过程中,可供选择的有机试剂有下列四组,均可使用的是
B
B
.A.苯、酒精 B.四氯化碳、苯 C.汽油、醋酸 D.汽油、氨水
(3)在3mL碘水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是
溶液分层,上层颜色接近无色,下层呈紫红色
溶液分层,上层颜色接近无色,下层呈紫红色
(注:下图片中深色区为紫红色溶液)
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持器、物品,尚缺少的玻璃仪器是
分液漏斗
分液漏斗
.(5)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出上图实验装置中的错误之处.
①
缺石棉网
缺石棉网
;②温度计插到了液体中
温度计插到了液体中
;③冷凝管进出水的方向颠倒
冷凝管进出水的方向颠倒
.黄铁矿(主要成分为FeS2)是我国大多数硫酸厂制取的主要原料.某化学学习小组对黄铁矿石进行如下实验探究:
[实验一]为测定硫元素的含量
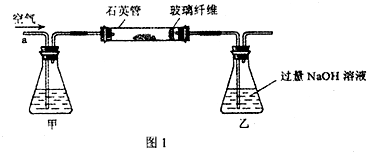
I.将m1g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全.
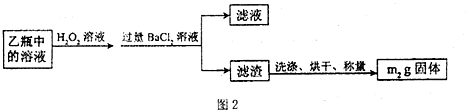
II.反应结束后,将乙瓶中的溶液进行如图2处理.
[实验二]测定铁元素的含量.III.测定铁元素含量的实验步骤如下:
①用足量稀硫酸溶解石英管中的固体残渣;
②加还原剂使溶液中的Fe3+完全转化为Fe2+后,过滤、洗涤;
③将滤液稀释至250mL;
④每次取稀释液25.00mL,用已知物质的量浓度为cmol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为VmL(该反应中还原产物为Mn2-)
请完成下列填空:
(1)已知12gFeS2完全燃烧放热85.3kJ,则FeS2燃烧热的化学方程式是
(2)I中,甲瓶内所盛试剂是
(3)II中的滤渣在称量前还应进行的操作是
(4)III的步骤③中,需要用到的仪器除烧杯、玻璃棒外,还有
(5)该黄铁矿中硫元素的质量分数
×100%
×100%(用I、II中有关实验数据表达);该黄铁矿中铁的元素的质量分数
×100%
×100%(用I、II中有关实验数据表达)
查看习题详情和答案>>
[实验一]为测定硫元素的含量
I.将m1g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全.

II.反应结束后,将乙瓶中的溶液进行如图2处理.

[实验二]测定铁元素的含量.III.测定铁元素含量的实验步骤如下:
①用足量稀硫酸溶解石英管中的固体残渣;
②加还原剂使溶液中的Fe3+完全转化为Fe2+后,过滤、洗涤;
③将滤液稀释至250mL;
④每次取稀释液25.00mL,用已知物质的量浓度为cmol/L的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为VmL(该反应中还原产物为Mn2-)
请完成下列填空:
(1)已知12gFeS2完全燃烧放热85.3kJ,则FeS2燃烧热的化学方程式是
FeS2(s)+
O2(g)═
Fe2O3(s)+2SO2(g)△H=-853kJ/mol
| 11 |
| 4 |
| 1 |
| 2 |
FeS2(s)+
O2(g)═
Fe2O3(s)+2SO2(g)△H=-853kJ/mol
.| 11 |
| 4 |
| 1 |
| 2 |
(2)I中,甲瓶内所盛试剂是
NaOH
NaOH
溶液;乙瓶内发生反应的离子方程式有2OH-+SO2═SO32-+H2O
2OH-+SO2═SO32-+H2O
;I中玻璃纤维的作用是防止粉尘进入导管和乙装置
防止粉尘进入导管和乙装置
.(3)II中的滤渣在称量前还应进行的操作是
洗涤、干燥
洗涤、干燥
;II中,所加H2O2溶液需足量的理由是使SO32- 完全转化成SO42-
使SO32- 完全转化成SO42-
.(4)III的步骤③中,需要用到的仪器除烧杯、玻璃棒外,还有
250ml容量瓶
250ml容量瓶
;④中取稀释液25.00mL需用的仪器是酸式滴定管
酸式滴定管
.(5)该黄铁矿中硫元素的质量分数
| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |
| 2.8CV |
| m1 |
| 2.8CV |
| m1 |