摘要:85gPbxOy粉末.. ⑵打开活塞K.通入H2.排尽装置内的空气后.点燃A处酒精灯. 进行反应.C装置的作用是: . ⑶待A中反应完全后.停止加热.仍要继续通入H2一段时间. 其目的是: ⑷卸下装置B.称量.发现增重0.72g.则该铅的氧化物化学式为: .
网址:http://m.1010jiajiao.com/timu_id_4235705[举报]
下列实验方法或操作正确的是( )
| A、测定某溶液的pH时,用pH试纸蘸取待测液,然后和标准比色卡对比得出pH | B、锌与稀硫酸反应制取氢气,加入少量硫酸铜粉末会使产生氢气的速率加快 | C、测定硫酸铜晶体中结晶水含量时,加热后的硫酸铜粉末要放在空气中冷却再称量 | D、用标准盐酸滴定未知浓度的氢氧化钠溶液,用待测液润洗锥形瓶 |
控制变量法是化学实验的一种常用方法,下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据(计算结果精确到小数点后一位):
分析以下数据,回答下列问题:
(1)实验1和实验2表明, 对反应速率有影响,对同一规律进行研究的实验还有一组是 (填实验序号).
(2)下列说法正确的是
A.t1<70 B.m1<m2 C.m6=19.3 D.t1>t4
(3)本实验还可以研究 对化学反应速率的影响.
(4)硫酸的物质的量浓度是 mol/L,实验6生成的硫酸锌的质量m5= g.
查看习题详情和答案>>
分析以下数据,回答下列问题:
| 序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
| 1 | 50.0 | 2.0 | 薄片 | 15 | 200 | m1 |
| 2 | 50.0 | 2.0 | 薄片 | 25 | 100 | m2 |
| 3 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m3 |
| 4 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m4 |
| 5 | 50.0 | 2.0 | 粉末 | 25 | t1 | 5.0 |
| 6 | 50.0 | 4.0 | 粉末 | 25 | t2 | m5 |
| 7 | 50.0 | 6.0 | 粉末 | 25 | t3 | 14.9 |
| 8 | 50.0 | 8.0 | 粉末 | 25 | t4 | 19.3 |
| 9 | 50.0 | 10.0 | 粉末 | 25 | t5 | m6 |
| 10 | 50.0 | 12.0 | 粉末 | 25 | t6 | 19.3 |
(2)下列说法正确的是
A.t1<70 B.m1<m2 C.m6=19.3 D.t1>t4
(3)本实验还可以研究
(4)硫酸的物质的量浓度是
一瓶无色液体A,含有NaCl、NaOH和Na2CO3中的两种;一包白色粉末B,含有CaO、Ca(OH)2和CaCO3中的两种.化学小组的同学为了探究A和B的成分,设计了如图所示的实验方案,请根据图示过程回答问题.

(1)固体C难溶于水,是一种常见的补钙产品,则固体C是 (填写化学式和名称均可,下同),与盐酸反应的化学方程式为 ;
(2)液体A中一定含有 ,白色粉末B中一定含有 .写出滤液1与液体A之间发生反应的化学方程式为 .
(3)小组同学们分析发现:假设溶液A滴加适量,若滤液2中只含有一种溶质,则原无色溶液A中含有的另外一种溶质是 ;若滤液2中含有两种溶质,则原无色溶液A中含有的另外一种溶质是 .
查看习题详情和答案>>

(1)固体C难溶于水,是一种常见的补钙产品,则固体C是
(2)液体A中一定含有
(3)小组同学们分析发现:假设溶液A滴加适量,若滤液2中只含有一种溶质,则原无色溶液A中含有的另外一种溶质是
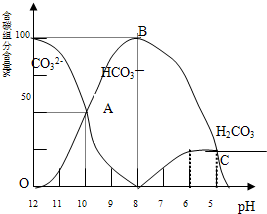 常温下在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示:回答下列问题:
常温下在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示:回答下列问题:(1)20mL 0.1mol/LNa2CO3溶液呈碱性的原因是(用离子方程式表示)
(2)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO32-离子不超过其总量的10%.请你设计简单实验证明该同学的观点是否正确
(3)若向20mL 0.1mol/LNa2CO3溶液中加入BaCl2粉末3.328×10-7g时开始产生沉淀X,则Ksp(X)=
(4)请写出OAB段的离子方程式
目前加碘食盐的添加剂是碘酸钾,碘酸钾是一种白色结晶粉末,无臭无味,酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、二氧化硫等还原性物质作用,被还原为单质碘,在碱性介质中,碘酸钾能被氯气、次氯酸盐等氧化为高碘酸钾.碘酸钾在常温下稳定,加热至560℃开始分解.工业生产碘酸钾的流程如下,在反应器中发生的反应方程式为:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑.试回答下列问题:
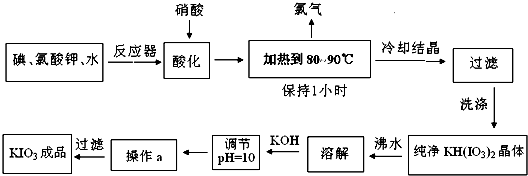
(1)对反应产物酸化时,用硝酸而不用HI,其原因可能是
(2)要保持溶液微沸(加热到80~90℃)1小时,以完全排出氯气.检验氯气完全排出简单实验方法是 .
(3)合成实验中涉及两次过滤,在实验室进行过滤实验时,用到的玻璃仪器有 .
(4)在过滤器上洗涤沉淀的操作是: .
(5)参照碘酸钾与氢氧化钾溶解度表格,操作a得到碘酸钾晶体,你建议的方法是
查看习题详情和答案>>

(1)对反应产物酸化时,用硝酸而不用HI,其原因可能是
(2)要保持溶液微沸(加热到80~90℃)1小时,以完全排出氯气.检验氯气完全排出简单实验方法是
(3)合成实验中涉及两次过滤,在实验室进行过滤实验时,用到的玻璃仪器有
(4)在过滤器上洗涤沉淀的操作是:
(5)参照碘酸钾与氢氧化钾溶解度表格,操作a得到碘酸钾晶体,你建议的方法是
| 温度 | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
| KOH g/100g水 | 49.2 | 50.8 | 52.8 | 59.8 | 62.4 | 78.6 |