摘要:交流卡片: NO:2006-SY-518 主题:Zn.Cu与浓盐酸 A.将锌放入浓盐酸中.反应较快 B.将锌片与铜片贴在一起.一同投入浓盐酸中.反应快速放出气体! C.当B中锌片完全溶解后.将溶液加热.又产生气体.得到无色溶液 D.将上述反应后的溶液.隔绝空气.加入适量水.出现白色沉淀
网址:http://m.1010jiajiao.com/timu_id_4235699[举报]
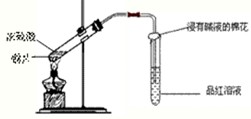 研究性学习小组为探究Cu与浓H2SO4反应及其产物SO2的性质,设计如下实验装置:
研究性学习小组为探究Cu与浓H2SO4反应及其产物SO2的性质,设计如下实验装置:
(1)写出铜与浓硫酸反应的化学方程式:______;浸有碱液的棉花的作用是:______.
(2)该小组同学在实验中发现以上实验装置有相当多不足之处,如实验不够安全和易造成环境污染等.为改进实验和更多地了解SO2的性质,经过同学间的讨论和与老师的交流,设计了如图实验装置.
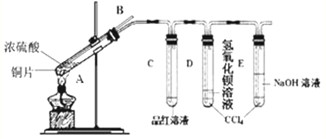
①对试管A中的浓H2SO4和铜丝进行加热,发现E试管中有气泡逸出,品红溶液 很快褪色,但最终 未见D试管中氢氧化钡溶液出现浑浊.为探究D试管中未出现浑浊的原因,该小组同学在化学手册中只查阅到下列物质常温下的溶解度数据:
| 物质 | 溶解度(g/100水) | 物质 | 溶解度(g/100水) |
| Ca(OH)2 | 0.173 | Ba(OH)2 | 3.89 |
| CaCO3 | 0.0013 | BaSO3 | 0.016 |
| Ca(HCO3)2 | 16.60 |
②为验证D试管中溶液的组成,进行了下列实验,请你帮他们完成实验报告.
| 实验方案 | 现象 |
| 1取少量溶液于试管中,加入氢氧化钠溶液 | |
| 2取少量溶液于试管中,加入稀盐酸,加热,用湿润的蓝色石蕊试纸检验生成的气体. |
A.铝粉 B.氯化钡溶液 C.银粉 D.碳酸氢钠溶液
(4)请写出长导管B的作用______(只写一点就可). 查看习题详情和答案>>
|
金属元素铊的相关信息如下图所示.下列有关卡片信息解读错误的是
| |
| [ ] | |
A. |
Tl是铊的元素符号 |
B. |
铊元素的中子数=204-81=123 |
C. |
铊位于第六周期ⅢA族 |
D. |
铊的金属性比铝的金属性强 |
按下表所列项目,对自己家里的灶具等进行调查分析,如实填写并与家长及同学交流。
|
所用的灶具 |
|
|
使用的燃料 |
|
|
使燃料充分燃烧的方法 |
|
|
防止燃烧废气污染的措施 |
|
|
存在的问题 |
|
|
改进的措施与方向 |
(2012?泉州二模)已知甲和乙在溶液中的转化关系如图1所示:

请回答下列问题:
(1)若甲是10电子的单核微粒,乙是两性氢氧化物,则微粒甲的结构示意图为
 .
.
(2)若甲是10电子的阳离子,乙是碱性气体.1mol乙通入足量强酸溶液中与H+反应,反应过程中能量变化如图2:写出乙的一种用途:
(3)若甲是CrO42-(黄色)和Cr2O72-(橙色)的混合溶液,在该溶液中存在如下平衡:CrO42-(黄色)+2H+? Cr2O72-(橙色)+H2O若测得甲溶液的pH=1,该溶液显
(4)若甲仅含有NO3-、SO42-和X三种离子,则X离子可能是
A.Fe2+ B.HCO3- C.Ba2+ D.Fe3+
(5)若甲是CO2,乙中HCO3-和CO32-的物质的量浓度相等,此时溶液的pH=10,则HCO3-的电离平衡常数Ka=
查看习题详情和答案>>

请回答下列问题:
(1)若甲是10电子的单核微粒,乙是两性氢氧化物,则微粒甲的结构示意图为


(2)若甲是10电子的阳离子,乙是碱性气体.1mol乙通入足量强酸溶液中与H+反应,反应过程中能量变化如图2:写出乙的一种用途:
制氮肥
制氮肥
;该反应的热化学方程式是NH3(g)+H+(aq)═NH4+(aq)△H=-(b-c)kJ?mol-1
NH3(g)+H+(aq)═NH4+(aq)△H=-(b-c)kJ?mol-1
.(3)若甲是CrO42-(黄色)和Cr2O72-(橙色)的混合溶液,在该溶液中存在如下平衡:CrO42-(黄色)+2H+? Cr2O72-(橙色)+H2O若测得甲溶液的pH=1,该溶液显
橙
橙
色.(4)若甲仅含有NO3-、SO42-和X三种离子,则X离子可能是
D
D
(填序号).A.Fe2+ B.HCO3- C.Ba2+ D.Fe3+
(5)若甲是CO2,乙中HCO3-和CO32-的物质的量浓度相等,此时溶液的pH=10,则HCO3-的电离平衡常数Ka=
10-10
10-10
.
