摘要:把由NaOH.AlCl3.MgCl2三种固体组成的混合物.溶于足量水中后有0.58克白色沉淀.在所得浊液中.逐滴加入0.5mol/L的盐酸.加入盐酸的体积与生成沉淀的质量关系如图所示: ⑴ 混合物中NaOH的质量为 . ⑵ 混合物中AlCl3质量为 . ⑶ 混合物中MgCl2质量为 . ⑷ P点表示盐酸的体积是 . ★13.有甲.乙两瓶无色溶液.已知它们只可能是A1Cl3溶液和 NaOH溶液.现做如下实验:①取440 mL甲溶液与120 mL乙溶液反应产生1.56 g沉淀,②若取120 mL甲溶液与440 mL乙溶液反应.也产生1.56 g沉淀,③若取120 mL甲溶液与400 mL乙溶液反应.则产生3.12 g沉淀.试通过计算和推理判断:甲溶液为 溶液.甲溶液的物质的量浓度为 .乙溶液的物质的量浓度为 . 第二讲 铝的化合物
网址:http://m.1010jiajiao.com/timu_id_4226104[举报]
 Ⅰ把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中,有0.58g白色沉淀析出,向所得浊液中,逐滴加入1mol/L盐酸,加入盐酸的体积和生成沉淀的质量如图所示.
Ⅰ把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中,有0.58g白色沉淀析出,向所得浊液中,逐滴加入1mol/L盐酸,加入盐酸的体积和生成沉淀的质量如图所示.(1)混合物中NaOH的质量是
4.4g
4.4g
(2)P点所表示盐酸的体积为
110ml
110ml
.Ⅱ某待测液可能含有Ag+、Fe3+、K+、Ba2+、NH4+、SO42-、NO3-等离子,
进行如下实验:
①加入过量的稀盐酸,有白色沉淀生成.
②过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成.
③过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现.
④另取少量步骤③中的滤液,加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体.
根据实验现象回答:待测液中一定含有
Ag+ Ba2+ NH4+ NO3-
Ag+ Ba2+ NH4+ NO3-
离子,一定不含有SO42-Fe3+
SO42-Fe3+
离子.
把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量的水中,有0.58 g白色沉淀析出,向所得的浊液里,逐滴加入0.5 mol·L-1的盐酸,加入盐酸的体积和生成沉淀的质量如图4-7所示。(提示:Na[Al(OH)4]+HCl Al(OH)3↓+NaCl+H2O)
Al(OH)3↓+NaCl+H2O)
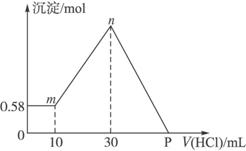
图4-7
(1)混合物中NaOH的质量是_________g;AlCl3的质量是_________g;MgCl2的质量是_________g。
(2)P点所表示盐酸加入体积是_________ mL。
查看习题详情和答案>>把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58 g白色难溶物析出,向所得溶液中逐滴加入0.5 mol·L-1的盐酸,加入盐酸的体积和生成沉淀的质量如右图所示:

(1)混合物中NaOH的质量是___________g,AlCl3的质量是___________g,MgCl2的质量为___________g。
(2)P点表示盐酸加入的体积为___________mL。
查看习题详情和答案>>