摘要:2.[广东梅州五华县横陂中学2009届高考模拟测试.2月]分类方法在化学学科的发展中起到了非常重要的作用.下列分类标准合理的是 ①根据酸分子中含有的氢原子数将酸分为一元酸.二元酸等②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应③根据分散系是否具有丁达尔现象将分散系分为溶液.胶体和浊液④根据反应中的热效应将化学反应分为放热反应和吸热反应 A.①③ B.②④ C.①②④ D.②③④
网址:http://m.1010jiajiao.com/timu_id_4224124[举报]
(2007广东梅州)(1)肼(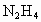 )又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0g
)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0g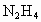 在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),
在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),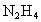 完全燃烧反应的热化学方程式是________.
完全燃烧反应的热化学方程式是________.
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时:
正极的电极反应式是________;
负极的电极反应式是________.
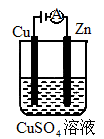
(3)图是一个电化学过程示意图.
①锌片上发生的电极反应是________.
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼-空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积含量为20%).
(4)传统制备肼的方法,是以NaClO氧化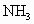 制得肼的稀溶液,该反应的离子方程式为________.
制得肼的稀溶液,该反应的离子方程式为________.
(2012?广东)难溶性杂卤石(K2SO4?MgSO4?2CaSO4?2H2O)属于“呆矿”,在水中存在如下平衡
K2SO4?MgSO4?2CaSO4?2H2O(s)?2Ca2++2K++Mg2++4
+2H2O
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如图1: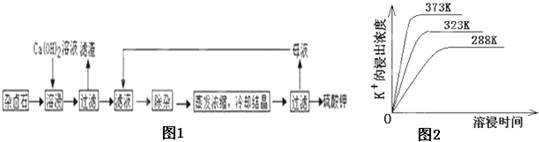
(1)滤渣主要成分有
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:
(3)“除杂”环节中,先加入
(4)不同温度下,K+的浸出浓度与溶浸时间的关系是图2,由图可得,随着温度升高,①
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+
?CaCO3(s)+
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K
查看习题详情和答案>>
K2SO4?MgSO4?2CaSO4?2H2O(s)?2Ca2++2K++Mg2++4
| SO | 2- 4 |
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如图1:

(1)滤渣主要成分有
CaSO4
CaSO4
和Mg(OH)2
Mg(OH)2
以及未溶杂卤石.(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:
氢氧根与镁离子结合使平衡向右移动,钾离子变多
氢氧根与镁离子结合使平衡向右移动,钾离子变多
.(3)“除杂”环节中,先加入
K2CO3
K2CO3
溶液,经搅拌等操作后,过滤,再加入H2SO4
H2SO4
溶液调滤液PH至中性.(4)不同温度下,K+的浸出浓度与溶浸时间的关系是图2,由图可得,随着温度升高,①
在同一时间K+的浸出浓度大
在同一时间K+的浸出浓度大
②反应速率加快,平衡时溶浸时间短
反应速率加快,平衡时溶浸时间短
;(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+
| CO | 2- 3 |
| SO | 2- 4 |
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K
1.75×104
1.75×104
(计算结果保留三位有效数字).