摘要:6.[河南运城市2008-2009学年高三第一学期期末调研测试]下列有关反应热的叙述正确的是 ( B ) A.已知. 则氢气的燃烧热为241.8Kj/mol B.C,△H=1.9kJ﹒mol-1说明石墨比金刚石稳定 C.X Z,△H>0恒温恒容条件下达到平衡后加入X. 上述反应的△H增大 D.已知.则△H1>△H2 7[河南运城市2008-2009学年高三第一学期期末调研测试] 把氯气通入稀氨水中.NH3分子上的一个H被Cl取代生成氯氨.然后加入过量的氨和氯氨作用.得到联氨(N2H4).写出上述反应的化学方程式: (1) 联氨是一种可燃性液体.可用作火箭燃料.已知32.0g N2H4和H2O2反应生成氮气和水.放出热量642kJ.该反应的热化学方程式是: (2) 联氨的水溶液显弱碱性.用离子方程式表示其显弱碱性的原因: (3) 联氨-空气燃料电池是一种碱性燃料电池.电解质溶液是20%-30%的KOH溶液.联氨-空气燃料电池放电生成N2和H2O.其电极反应式是: 正极 负极
网址:http://m.1010jiajiao.com/timu_id_4224118[举报]
2008年9月14日凌晨2时许,一辆载重为35吨的液苯槽车与一辆摩托车发生相撞,车辆翻入河沟,造成大量液苯泄漏,情况万分危急。河南焦作消防官兵和公安交警展开紧急大排险,经过13个小时艰苦奋战,将事故成功处理。以下报道中有科学性错误的是
[ ]
A.由于大量苯渗入土壤,会对周边农田、水源造成严重污染
B.由于苯是一种易挥发、易燃的物质,周围地区如果遇火星 就可能引起爆炸
C.可以采取抽吸水渠中下层液体的办法,达到清除泄漏物的目的
D.处理事故时,由于事故发生的周围比较空旷,有人提出用点火焚烧的办法来清除泄漏物,但由于苯燃烧会产生大量的黑烟扩大污染,所以该办法未被采纳
查看习题详情和答案>>
B.由于苯是一种易挥发、易燃的物质,周围地区如果遇火星 就可能引起爆炸
C.可以采取抽吸水渠中下层液体的办法,达到清除泄漏物的目的
D.处理事故时,由于事故发生的周围比较空旷,有人提出用点火焚烧的办法来清除泄漏物,但由于苯燃烧会产生大量的黑烟扩大污染,所以该办法未被采纳
2008年9月14日凌晨2时许,一辆载重量为35吨的液苯槽车与一辆摩托车发生相撞,车辆翻入河沟,造成大量液苯泄漏,情况万分危急。河南焦作消防官兵和公安交警展开紧急大排险,经过13个小时艰苦奋战,将事故成功处置。以下报道中有科学性错误的是
[ ]
A.由于大量苯渗入土壤,会对周边农田、水源造成严重污染
B.由于苯是一种易挥发、易燃的物质,周围地区如果遇火星就可能引起爆炸
C.可以采取抽吸水渠中下层液体的办法,达到清除泄漏物的目的
D.处理事故时,由于事故发生的周围比较空旷,有人提出用点火焚烧的办法来清除泄漏物,但由于苯燃烧会 产生大量的黑烟扩大污染,所以该办法未被采纳
查看习题详情和答案>>
B.由于苯是一种易挥发、易燃的物质,周围地区如果遇火星就可能引起爆炸
C.可以采取抽吸水渠中下层液体的办法,达到清除泄漏物的目的
D.处理事故时,由于事故发生的周围比较空旷,有人提出用点火焚烧的办法来清除泄漏物,但由于苯燃烧会 产生大量的黑烟扩大污染,所以该办法未被采纳
(2008?天津)Ⅰ.化学实验室制取气体的方法之一是将浓硫酸滴入浓盐酸中.请从下图中挑选所需仪器,在方框内画出用该方法制备、收集干燥氯化氢气体的装置简图,并在图中标明所用试剂.(仪器可重复使用,固定装置不必画出)
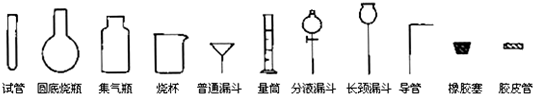
Ⅱ.实验室制备少量硫酸亚铁品体的实验步骤如下:取过量洁净的铁屑,加入20%~30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡.将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口.静置、冷却一段时间后收集产品.
(1)写出该实验制备硫酸亚铁的化学方程式:
(2)硫酸溶液过稀会导致
(3)采用水浴加热的原因是
(4)反应时铁屑过量的目的是(用离子方程式表示)
(5)溶液趁热过滤的原因是
(6)静置冷却一段时间后,在试管中观察到的现象是
查看习题详情和答案>>

Ⅱ.实验室制备少量硫酸亚铁品体的实验步骤如下:取过量洁净的铁屑,加入20%~30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡.将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口.静置、冷却一段时间后收集产品.
(1)写出该实验制备硫酸亚铁的化学方程式:
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
.(2)硫酸溶液过稀会导致
反应速率慢 不利于晶体析出
反应速率慢 不利于晶体析出
.(3)采用水浴加热的原因是
容易控制温度
容易控制温度
.(4)反应时铁屑过量的目的是(用离子方程式表示)
Fe+2Fe3+═3Fe2+
Fe+2Fe3+═3Fe2+
.(5)溶液趁热过滤的原因是
减小FeSO4的损失
减小FeSO4的损失
.塞紧试管口的目的是防止空气进入试管将Fe2+氧化为Fe3+
防止空气进入试管将Fe2+氧化为Fe3+
.(6)静置冷却一段时间后,在试管中观察到的现象是
有浅绿色晶体析出
有浅绿色晶体析出
.(2008?石家庄模拟)下列离子方程式中,只能表示一个化学反应的是( )
①CO32-+2H+═CO2↑+H2O
②Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
③Ag++Cl-=AgCl↓
④Fe+Cu2+═Fe2++Cu
⑤Cl2+H2O═H++Cl-+HClO.
①CO32-+2H+═CO2↑+H2O
②Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
③Ag++Cl-=AgCl↓
④Fe+Cu2+═Fe2++Cu
⑤Cl2+H2O═H++Cl-+HClO.
查看习题详情和答案>>
(2008?淮南一模)甲图是元素周期表的框架
(1)请在上面元素周期表中画出金属元素与非金属元素的分界线.
(2)依据元素周期表回答下列问题:
A.周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是
B.周期中表的元素④和元素⑦的氢化物的熔、沸点高低顺序是
C.①-⑦元素的某单质在常温下化学性质稳定,通常可以做保护气的是
D.在上面元素周期表中全部是金属元素的主族是
a.IA族 b.ⅡA族 c.ⅣA族 d.VIIA族
(3)已知甲元素位于第三周期,且其原子半径为同周期金属元素中的原子最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式
①、③两种元素的单质已被应用于宇宙飞船的燃料电池中,如图乙所示,两个电极均由多孔性碳构成,通入的两种单质由孔隙逸出并在电极表面放电.请回答:
b是电池的
查看习题详情和答案>>
(1)请在上面元素周期表中画出金属元素与非金属元素的分界线.
(2)依据元素周期表回答下列问题:
A.周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是
NaOH>Mg(OH)2
NaOH>Mg(OH)2
(用化学式表示).B.周期中表的元素④和元素⑦的氢化物的熔、沸点高低顺序是
HF>HCl
HF>HCl
(用化学式表示).C.①-⑦元素的某单质在常温下化学性质稳定,通常可以做保护气的是
N2
N2
(用化学式表示).D.在上面元素周期表中全部是金属元素的主族是
b
b
;全部是非金属元素的主族是d
d
(填写a、b、c、d).a.IA族 b.ⅡA族 c.ⅣA族 d.VIIA族
(3)已知甲元素位于第三周期,且其原子半径为同周期金属元素中的原子最小的,请写出甲的氧化物与NaOH溶液反应的离子方程式
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
;在一定条件下1g①的单质在足量③的单质中完全燃烧生成液态物质时,放出的热量为akJ,请写出此条件下表示①的单质燃烧热的热化学方程式H2(g)+
O2(g)=H2O(l)△H=-2akJ/mol
| 1 |
| 2 |
H2(g)+
O2(g)=H2O(l)△H=-2akJ/mol
;| 1 |
| 2 |
①、③两种元素的单质已被应用于宇宙飞船的燃料电池中,如图乙所示,两个电极均由多孔性碳构成,通入的两种单质由孔隙逸出并在电极表面放电.请回答:
b是电池的
正
正
极; a电极上的电极反应式是2H2+4OH--4e-=4H2O或H2+2OH--2e-=2H2O
2H2+4OH--4e-=4H2O或H2+2OH--2e-=2H2O
.