摘要: [湘西南名校联盟2009年2月高三联合考试试卷]食盐是日常生活的必需品.也是重要的化工原料. (1)粗食盐常含有少量Ca2+.Mg2+.SO42-等杂质离子. 欲除去食盐中的Ca2+.Mg2+.SO42-离子.滴加试剂顺序正确的是 . A. Na2CO3 BaCl2 NaOH HCl B. NaOH HCl BaCl2 Na2CO3 C. NaOH BaCl2 Na2CO3 HCl D. BaCl2 Na2CO3 NaOH HCl (2) 工业盐中含有NaNO2.外观和食盐相似.有咸味.人若误食会引起中毒,致死量为0.3g~0.5g.已知NaNO2能发生如下反应: 2NO2-+xI-+yH+=2NO↑+I2+zH2O.请回答 根据上述反应.可用化学试纸和生活中常见物质进行实验来鉴别工业盐和食盐.现有碘化钾淀粉试纸.则还需选用的生活中常见物质的名称为 . (3)用提纯的NaCl配制500 mL4.00 mol·L-1NaCl溶液.所用 仪器除药匙.玻璃棒外还有 . 电解饱和食盐水的装置如图所示.若收集的H2为2 L. 则同样条件下收集的Cl2<2 L.原因是 (4)实验室制备H2和Cl2通常采用下列反应: Zn+H2SO4 ZnSO4+H2↑,MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O 据此.从下列所给仪器装置中选择制备并收集H2的装置 和制备并收集干燥.纯净Cl2的装置 . 可选用制备气体的装置: 答案CD 食用醋,天平.烧杯.500 mL容量瓶.胶头滴管. 电解生成的氯气与电解生成的NaOH发生了反应. e,d.
网址:http://m.1010jiajiao.com/timu_id_4224076[举报]
用氯气对饮用水消毒已有百年历史.这种消毒方法会使饮用水中的有机物发生氯代反应,生成有机含氯化合物,对人体有害,且氯气本身也是一种有毒气体.世界环保联盟即将全面禁止用氯气对饮用水消毒,建议推广采用广谱性高效消毒剂二氧化氯(ClO2).目前欧洲一些国家用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,反应的化学方程式为:
(1)配平上述化学方程式.
(2)此反应中氧化剂是:
(3)在标准状况下有4.48L氯气生成时,转移的电子数为
(4)我国研制成功用氯气氧化亚氯酸钠(在氮气保护下)制得ClO2,表示这一反应的化学方程式是2NaClO2+Cl2═2ClO2↑+2A.已知A物质是一种盐,它的化学式为
查看习题详情和答案>>
2
2
NaClO3+4
4
HCl═2
2
NaCl+2
2
ClO2↑+1
1
Cl2↑+2
2
H2O.(1)配平上述化学方程式.
(2)此反应中氧化剂是:
NaClO3
NaClO3
,在反应中盐酸体现的性质是还原性
还原性
和酸性
酸性
;(3)在标准状况下有4.48L氯气生成时,转移的电子数为
0.4
0.4
mol,被氧化的盐酸的物质的量为0.4
0.4
mol.(4)我国研制成功用氯气氧化亚氯酸钠(在氮气保护下)制得ClO2,表示这一反应的化学方程式是2NaClO2+Cl2═2ClO2↑+2A.已知A物质是一种盐,它的化学式为
NaCl
NaCl
.这一方法的优点是不产生有毒的氯气,减小对环境的污染
不产生有毒的氯气,减小对环境的污染
.世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯.二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热.实验室以电解法制备ClO2的流程如图:
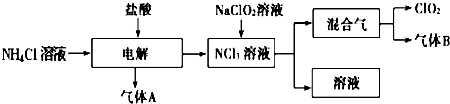
(1)ClO2中所有原子 (填“是”或“不是”)都满足8电子结构.上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用 .
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是 .
A.二氧化氯可广泛用于工业和饮用水处理
B.应用在食品工业中能有效地延长食品贮藏期
C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
D.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备.化学反应方程式为 .缺点主要是产率低、产品难以分离,还可能污染环境.
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是 ,此法相比欧洲方法的优点是 .
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为 .此法提高了生产及储存、运输的安全性,原因是 .
查看习题详情和答案>>

(1)ClO2中所有原子
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是
A.二氧化氯可广泛用于工业和饮用水处理
B.应用在食品工业中能有效地延长食品贮藏期
C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
D.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备.化学反应方程式为
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为
三国时代,诸葛亮领兵南征孟获,遇到了“哑泉”,士兵饮后致哑,腹痛,甚至死亡.又有一“安乐泉”饮后可解“哑泉”毒.1995年10月国内某报刊报道,经科研人员研究,“哑泉”水中溶有CuSO4,“安乐泉”水质偏碱性.下列有关说法可能符合题意的是( )
查看习题详情和答案>>
世界环保联盟即将全面禁止在自来水中加氯气(Cl2,黄绿色气体),推广采用光谱高效消毒剂二氧化氯,目前欧州和我国主采用Kesting法[原料为氯酸钠(NaClO3)与盐酸]制取ClO2,该法的缺点是同时会产生Cl2.该法制ClO2的化学方程式为:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
(1)该反应中,氧化剂为
(2)若反应生成0.1mol Cl2,则转移的电子的物质的量为
(3)盐酸在反应中显示出来的性质是:(填写编号)
①还原性 ②还原性、酸性 ③氧化性 ④氧化性、酸性.
查看习题详情和答案>>
(1)该反应中,氧化剂为
NaClO3
NaClO3
,氧化产物为Cl2
Cl2
.(2)若反应生成0.1mol Cl2,则转移的电子的物质的量为
0.2mol
0.2mol
.(3)盐酸在反应中显示出来的性质是:(填写编号)
②
②
.①还原性 ②还原性、酸性 ③氧化性 ④氧化性、酸性.
A~H以及X、Y的转化关系如右图所示:

请回答下列问题:
(1)电解上述滤液时产生G的电极是
(2)取上述滤液进行焰色反应实验显紫色(透过钴玻璃片),图中焰色反应显紫色的还有
(3)写出黑色固体A与X的浓溶液共热时反应的离子方程式:
(4)写出G与B溶液反应的化学方程式:
(5)ClO2是一种广谱型的消毒剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2,成为自来水的消毒剂.工业上ClO2常用NaClO3和Na2SO3溶液混合并加硫酸酸化制得,在该反应中NaClO3和Na2SO3的物质的量之比为
查看习题详情和答案>>

请回答下列问题:
(1)电解上述滤液时产生G的电极是
阳极
阳极
,其电极反应式为2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
.(2)取上述滤液进行焰色反应实验显紫色(透过钴玻璃片),图中焰色反应显紫色的还有
D、F、Y
D、F、Y
.(3)写出黑色固体A与X的浓溶液共热时反应的离子方程式:
MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O
MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O
.(4)写出G与B溶液反应的化学方程式:
Cl2+H2O2=O2↑+2HCl
Cl2+H2O2=O2↑+2HCl
.(5)ClO2是一种广谱型的消毒剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2,成为自来水的消毒剂.工业上ClO2常用NaClO3和Na2SO3溶液混合并加硫酸酸化制得,在该反应中NaClO3和Na2SO3的物质的量之比为
2:1
2:1
.