摘要:[广东梅州五华县横陂中学2009届高考模拟测试.2月]某中学化学教材上有如下介绍:“在氢氧化钠浓溶液中加入氧化钙.加热.制得白色固体就是碱石灰.它是水和二氧化碳的吸收剂 .有两个实验小组决定通过实验来探究碱石灰的组成. (1)第一小组设计的实验方案如下: 下列关于溶液中n(OH-).n(Ca2+).n(Na+)之间的关系式正确的是 A. n(Na+)+ 2n(Ca2+)= n(OH-) B. 2n(Na+) + 2n(Ca2+)= n(OH-) C. n(Na+)+ n(Ca2+)= 2n(OH-) 现有4.0g碱石灰,设其中n(Na+)= xmol, n(Ca2+)= ymol,请填写下列空格: 碱石灰的可能组成 NaOH, CaO NaOH, CaO, Ca(OH)2 NaOH, Ca(OH)2 NaOH, Ca(OH)2 H2O x,y之间关系式 A 40x+56y﹤4.0﹤ 40x+74y B C 把表中A.C的关系式填在下面空格上: A: C: . (2)第二小组查得如下资料:氢氧化钙在250℃时不分解.高于250℃时才分解,氢氧化钠在580℃时不分解.他们设计了如下方案并得出相应相关数据:取市售碱石灰4.0g.在250℃时加热至恒重.测得固体质量减少了0.6g,剩余固体在580℃时继续加热至恒重.测得固体质量又减少了0.7g.请通过计算确定该碱石灰各成分的质量分数? 答案 A A:40x+56y=4.0 C:40x+74y﹤4.0 NaOH%=13% Ca(OH)2%=72% H2O%=15% 7 [广东梅州五华县横陂中学2009届高考模拟测试.2月]某化学小组以苯甲酸为原料.制取苯甲酸甲酯.已知有关物质的沸点如下 物质 甲醇 苯甲酸 苯甲酸甲酯 沸点/℃ 65 249 199.6 I.合成苯甲酸甲酯粗产品 在圆底烧瓶中加入12.4 g苯甲酸和20ml甲醇(密度约为0.79g/cm3.).再小心加入3ml浓硫酸.混匀后.投入几粒碎瓷片.小心加热使反应完全.得苯甲酸甲酯粗产品. (1) 简述液体混合时.最后加入浓硫酸的理由是 . (2) 若反应产物水分子中有18O.写出能表示反应前后18O位置的化学方程式: . (3) 甲.乙.丙三位同学分别设计了如图三套实验室制取苯甲酸甲酯的装置(夹持仪器和 加热仪器均己略去).根据有机物的特点.最好采用 装置(填“甲 .“乙 . “丙 ). (4)计算可知.反应物甲醇过量.而反应物甲醇应过量.其理由是 . Ⅱ.粗产品的精制 (5)苯甲酸甲酯粗产品中往往含有少量甲醇.硫酸.苯甲酸和水等.现拟用下列流程图进 行精制.请根据流程图填入恰当操作方法的名称:操作l为 .操作2为 . (6)通过计算.苯甲酸甲酯的产率为 . 答案:浓硫酸密度较大.且与苯甲酸.甲醇混合时会放出大量热.先放入浓硫酸会导致甲醇 挥发.乙 , 该合成 反应是可逆反应.甲醇比苯甲酸价廉.且甲醇沸点低.易损失.增加甲醇的量.可提高苯甲酸的转化率.分液.蒸馏 65% .
网址:http://m.1010jiajiao.com/timu_id_4224075[举报]
(2007广东梅州)(1)肼(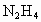 )又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0g
)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0g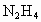 在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),
在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),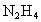 完全燃烧反应的热化学方程式是________.
完全燃烧反应的热化学方程式是________.
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时:
正极的电极反应式是________;
负极的电极反应式是________.
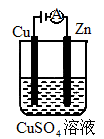
(3)图是一个电化学过程示意图.
①锌片上发生的电极反应是________.
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼-空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积含量为20%).
(4)传统制备肼的方法,是以NaClO氧化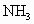 制得肼的稀溶液,该反应的离子方程式为________.
制得肼的稀溶液,该反应的离子方程式为________.
(2012?广东)难溶性杂卤石(K2SO4?MgSO4?2CaSO4?2H2O)属于“呆矿”,在水中存在如下平衡
K2SO4?MgSO4?2CaSO4?2H2O(s)?2Ca2++2K++Mg2++4
+2H2O
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如图1: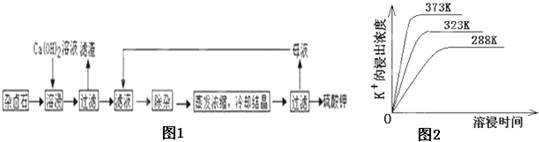
(1)滤渣主要成分有
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:
(3)“除杂”环节中,先加入
(4)不同温度下,K+的浸出浓度与溶浸时间的关系是图2,由图可得,随着温度升高,①
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+
?CaCO3(s)+
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K
查看习题详情和答案>>
K2SO4?MgSO4?2CaSO4?2H2O(s)?2Ca2++2K++Mg2++4
| SO | 2- 4 |
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如图1:

(1)滤渣主要成分有
CaSO4
CaSO4
和Mg(OH)2
Mg(OH)2
以及未溶杂卤石.(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:
氢氧根与镁离子结合使平衡向右移动,钾离子变多
氢氧根与镁离子结合使平衡向右移动,钾离子变多
.(3)“除杂”环节中,先加入
K2CO3
K2CO3
溶液,经搅拌等操作后,过滤,再加入H2SO4
H2SO4
溶液调滤液PH至中性.(4)不同温度下,K+的浸出浓度与溶浸时间的关系是图2,由图可得,随着温度升高,①
在同一时间K+的浸出浓度大
在同一时间K+的浸出浓度大
②反应速率加快,平衡时溶浸时间短
反应速率加快,平衡时溶浸时间短
;(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+
| CO | 2- 3 |
| SO | 2- 4 |
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,求此温度下该反应的平衡常数K
1.75×104
1.75×104
(计算结果保留三位有效数字).