网址:http://m.1010jiajiao.com/timu_id_4224025[举报]
(福建省漳州市芗城中学2009届高三一轮复习单元测试,化学,25)实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液。 应量取盐酸体积_______mL ,应选用容量瓶的规格_________mL。 除容量瓶外还需要的其它仪器_________________________________。
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)____________________
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(3) 操作A中,将洗涤液都移入容量瓶,其目的是
。溶液注入容量瓶前需恢复到室温,这是因为
。
(4)若出现如下情况,对所配溶液浓度将有何影响(偏高、偏低或无影响)?
a.没有进行A操作__________ ;b.加蒸馏水时不慎超过了刻度________ ;c.定容时俯视____________。
(5)若实验过程中出现如下情况如何处理?
加蒸馏水时不慎超过了刻度 ? __________________。
向容量瓶中转移溶液时(实验步骤B) 不慎有液滴掉在容量瓶外? _______ _______。
查看习题详情和答案>>(宁夏银川市实验中学2009届高三年级第三次月考,化学,5)离子检验的常用方法有三种:
| 检验方法 | 沉淀法 | 显色法 | 气体法 |
| 含义 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应中有气体产生 |
下列离子检验的方法不合理的是
A.NH4+-气体法 B.I--沉淀法
C.Fe3+-显色法 D.Ca2+-气体法
查看习题详情和答案>>(浙江舟山中学2009届度第一学期高三期中考试,化学,24)某课外小组利用H2还原黄色的WO3粉末测定W的相对原子质量,下图是测定装置的示意图,A中的试剂是盐酸。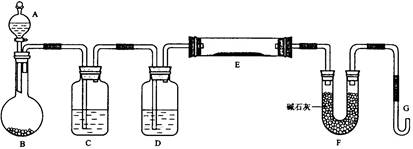
请回答下列问题。
(1)仪器中装入的试剂:B_________ 、C________、D___________;
(2)连接好装置后应首先_________________________;
(3)“加热反应管E”和“从A瓶逐滴滴加液体”这两步操作应该先进行的是:
____________________。在这两步之间还应进行的操作是_____________________;
(4)反应过程中G管逸出的气体是________________,其处理方法是:
______________________________________________________________________。
(5)从实验中测得了下列数据
①空E管的质量a
②E管和WO3的总质量b
③反应后E管和W粉的总质量c(冷却到室温称量)
④反应前F管及内盛物的总质量d
⑤反应后F管及内盛物的总质量e
由以上数据可以列出计算W的相对原子质量的两个不同计算式(除W外,其他涉及的元素的相对原子质量均为已知):
计算式1:Ar(W)=____________;计算式2:Ar(W)=____________。