摘要:14.[湖北省黄冈市2008年秋季高三年级期末考试化学]Ba2+是一种重金属离子.有一环境监测小组欲利用Na2S2O3.KI.K2Cr2O7.等试剂测定某工厂废水中Ba2+的浓度. (1)现需配制250mL 0.100mol·L-1标准Na2S2O3溶液.所需要的玻璃仪器除量筒.250rnL 容量瓶.玻璃棒外.还需要 . (2)需准确称取Na2S4O3固体的质量为 g. (3)另取废水50.00mL.控制适当的酸度加人足量的K2Cr2O7溶液.得BaCrO4沉淀,沉淀经洗涤.过滤后.用适量的稀盐酸溶解.此时CrO42-全部转化为Cr2O72-,再加过量KI溶液反应.反应液中再滴加上述Na2S2O3溶液.反应完全时.消耗Na2S2O2溶液36.00mL.已知有关的离子方程式为: ①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O, ②I2+2S2O32-=2I-+S4O62-. 试计算该工厂废水中Ba2+的物质的量浓度. 答案..(1)设Ba2+为x mol.则有 Ba2+~BaCrO2~Cr2O72-~I2~3S2O32- 1mol 3mol x mol 36.00×0.100×10-3mol mol 所以c(Ba2+)mol·L-1
网址:http://m.1010jiajiao.com/timu_id_4223950[举报]
|
背景材料:①2005年10月12日,“神舟六号”发射升空;②2005年10月,河南省鹤壁市发生煤矿“瓦斯”爆炸;③近期,黄冈市举行“液氯泄漏”预警演习;④据湖北省环境质量监测所抽查显示,新装修住房甲醛含量7成超标.据此判断,下列说法正确的是 | |
| [ ] | |
A. |
“神六”遨游太空时,在其轨道舱中无法完成“粗盐的提纯”实验 |
B. |
“瓦斯”爆炸最猛烈时,煤矿坑道中甲烷的体积分数为33.3% |
C. |
发生“液氯泄漏”时,应疏导群众就近向地下商场转移 |
D. |
为降低甲醛含量,新装修住房应紧闭门窗,并放置一盆水 |
|
背景材料:①“神舟六号”的防护层由聚四氟乙烯和玻璃纤维布组合而成;②光化学烟雾是导致珠三角地区空气质量下降的重要原因;③近期,黄冈市举行“液氯泄漏”预警演习;④据湖北省环境质量监测所抽查显示,新装修住房甲醛含量7成超标.⑤在广东、香港海域,渤海湾均出现过大面积的赤潮.据此判断,下列说法正确的是 (1)“神舟六号”的防护层是复合材料,四氟乙烯属于不饱和烃. (2)光化学污染主要是由氮氧化物和碳氢化物引起的. (3)发生“液氯泄漏”时,应疏导群众立即逆风向高处远离出事地点 (4)为降低甲醛含量,新装修住房应紧闭门窗,并放置一盆水 (5)赤潮是指在一定条件下海洋中某些生物短时间内大量繁殖或聚集,使海水变红色、褐色的现象 | |
| [ ] | |
A. |
(1)(2)(3) |
B. |
(1)(2)(5) |
C. |
(2)(3)(5) |
D. |
(2)(4)(5) |
1808年,英国化学家戴维用钾还原氧化镁,最早制得少量的镁.镁是航空工业的重要材料,镁合金用于制造飞机机身、发动机零件等,一架超音速飞机约有5%的镁合金构件,一枚导弹一般消耗100~200公斤镁合金;镁作为一种强还原剂,还用于钛、锆、铍和铀等的生产中;镁是燃烧弹和照明弹不能缺少的组成物;镁粉是节日烟花必需的原料.镁及其合金是一种用途很广泛的金属材料,目前世界上60%的镁是从海水中提取的.从海水(主要含NaCl和MgSO4)中提取金属镁的主要步骤如图:
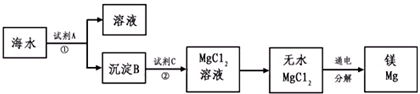
回答下列问题:
(1)Mg在周期表中的位置 ,试剂A可以选用 ,试剂C可选用 ;
(2)步骤①的离子方程式 ;
(3)用电子式表示氯化镁的形成过程 ;
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为: ;
(5)戴维制镁的化学方程式为 ;
(6)配平下列反应的方程式.
①UF4+Mg--U+MgF2
②Mg+HNO3--Mg(NO3)2+N2O↑+H2O. 查看习题详情和答案>>

回答下列问题:
(1)Mg在周期表中的位置
(2)步骤①的离子方程式
(3)用电子式表示氯化镁的形成过程
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为:
(5)戴维制镁的化学方程式为
(6)配平下列反应的方程式.
①UF4+Mg--U+MgF2
②Mg+HNO3--Mg(NO3)2+N2O↑+H2O. 查看习题详情和答案>>
 将8.34g FeSO4?7H2O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)如图所示.则下列说法正确的是( )
将8.34g FeSO4?7H2O样品隔绝空气加热脱水,其热重曲线(样品质量随温度变化的曲线)如图所示.则下列说法正确的是( )| A、FeSO4?7H2O晶体中有4种不同结合力的水分子 | ||||
| B、在100℃时,M的化学式为FeSO4?6H2O | ||||
| C、在200℃时,N的化学式为FeSO4?3H2O | ||||
D、380℃的P加热至650℃时的化学方程式为:2FeSO4
|
某铜矿石含氧化铜、氧化亚铜、三氧化二铁和大量脉石(SiO2),现采用酸浸法从矿石中提取铜,其流程图如下:

已知:①当矿石中三氧化二铁含量太低时,可用硫酸和硫酸铁的混合液浸出铜;②反萃取后的水层是硫酸铜溶液,Cu2+浓度约为50g/L.回答下列问题:
(1)矿石用稀硫酸浸出过程中氧化亚铜发生的反应为:Cu2O+2H+═Cu2++Cu+H2O;请写出该过程中发生的另一个氧化还原反应的离子方程式:
(2)萃取剂A是一类称作为肟类的有机化合物,如N-510、N-530等.某肟类化合物A的分子结构中仅含n1个-CH3、n2个-OH 和n3个 三种基团,无环状结构,三种基团的数目关系为n3=
三种基团,无环状结构,三种基团的数目关系为n3=
(3)写出电解过程中阳极(惰性电极)发生反应的电极反应式:
(4)循环中反萃取剂B的主要成分是
(5)某铜矿石样品中,若仅含氧化亚铜、三氧化二铁和脉石三种物质.取该矿石样品200.0g,用100mL1.0mol?L-1H2SO4溶液浸取后,还需加入10mL 1.0mol?L-1 Fe2(SO4)3溶液才能使铜全部浸出,浸取液经充分电解后可得到 6.4gCu.求铜矿石样品中氧化亚铜和氧化铁的质量分数?
查看习题详情和答案>>

已知:①当矿石中三氧化二铁含量太低时,可用硫酸和硫酸铁的混合液浸出铜;②反萃取后的水层是硫酸铜溶液,Cu2+浓度约为50g/L.回答下列问题:
(1)矿石用稀硫酸浸出过程中氧化亚铜发生的反应为:Cu2O+2H+═Cu2++Cu+H2O;请写出该过程中发生的另一个氧化还原反应的离子方程式:
Cu+2Fe3+═2Fe2++Cu2+
Cu+2Fe3+═2Fe2++Cu2+
.(2)萃取剂A是一类称作为肟类的有机化合物,如N-510、N-530等.某肟类化合物A的分子结构中仅含n1个-CH3、n2个-OH 和n3个
 三种基团,无环状结构,三种基团的数目关系为n3=
三种基团,无环状结构,三种基团的数目关系为n3=n1+n2-2
n1+n2-2
.若A的相对分子质量为116,分子结构中碳原子跟碳原子相连接,则A的结构简式是CH3-C(=N-OH)-C(=N-OH)-CH3
CH3-C(=N-OH)-C(=N-OH)-CH3
.(3)写出电解过程中阳极(惰性电极)发生反应的电极反应式:
4OH--4e-═O2↑+2H2O
4OH--4e-═O2↑+2H2O
.(4)循环中反萃取剂B的主要成分是
H2SO4
H2SO4
.(5)某铜矿石样品中,若仅含氧化亚铜、三氧化二铁和脉石三种物质.取该矿石样品200.0g,用100mL1.0mol?L-1H2SO4溶液浸取后,还需加入10mL 1.0mol?L-1 Fe2(SO4)3溶液才能使铜全部浸出,浸取液经充分电解后可得到 6.4gCu.求铜矿石样品中氧化亚铜和氧化铁的质量分数?