摘要: [河北正定中学2009届高三第四次月考]若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性.则可能的原因是[ BD ] A.生成了一种强酸弱碱盐 B.弱酸和强碱的反应 C.强酸和弱碱的反应 D.弱酸和弱碱的反应
网址:http://m.1010jiajiao.com/timu_id_4223948[举报]
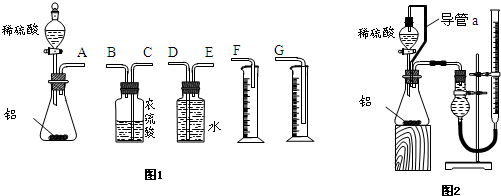
某中学有甲、乙两个探究性学习小组,他们拟用一定质量的纯铝片与足量稀硫酸的反应测定通常状况(约20℃,101kPa)下气体摩尔体积的方法.
(1)甲组同学拟选用下列实验装置完成实验(如图1):
①该组同学必须选用的装置的连接顺序是A接 接 接 (填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因. .
③实验结束时,该组同学应怎样测量实验中生成氢气的体积? .
(2)乙组同学仔细分析甲组同学的实验装置后,认为:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了如图2所示的实验装置.装置中导管a的作用是 , .
 查看习题详情和答案>>
查看习题详情和答案>>
(1)甲组同学拟选用下列实验装置完成实验(如图1):
①该组同学必须选用的装置的连接顺序是A接
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因.
③实验结束时,该组同学应怎样测量实验中生成氢气的体积?
(2)乙组同学仔细分析甲组同学的实验装置后,认为:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了如图2所示的实验装置.装置中导管a的作用是
 查看习题详情和答案>>
查看习题详情和答案>>
某化学兴趣小组需100mL某物质的量浓度的FeSO4溶液作标准试剂,现有外观颜色发黄的硫酸亚铁晶体、浓硫酸、稀盐酸、KMnO4溶液、溴水、KSCN溶液、石蕊、酚酞及中学化学常用化学仪器,实验过程如下:
Ⅰ.配制FeSO4溶液
(1)下列关于FeSO4溶液配制操作步骤的合理顺序为
A.在盛适量水的烧杯中滴加少量浓H2SO4后搅拌均匀并冷却到室温
B.称取一定质量的FeSO4晶体样品
C.将样品溶于已配制的稀H2SO4中,用玻璃棒搅拌至样品充分溶解
D.过滤后,将滤液转移到容量瓶中,加水稀释至指定刻度
E.往硫酸亚铁溶液中加入稍过量的铁粉,充分搅拌,静置一段时间至不再有气体冒出为止
(2)回答下列问题:
①将样品溶于稀H2SO4,而不直接溶于水的理由是
②在配制硫酸亚铁溶液时,需加入铁粉的理由是
Ⅱ.标定FeSO4溶液的浓度
(1)用移液管量取20.00mL FeSO4溶液放入锥形瓶中,用0.10mol?L-1的酸性KMnO4溶液滴至终点,耗去KMnO4溶液20.00mL,若生成物中Mn元素全部呈+2价,滴定反应的离子方程式为
(2)滴定时选用
查看习题详情和答案>>
Ⅰ.配制FeSO4溶液
(1)下列关于FeSO4溶液配制操作步骤的合理顺序为
A→B→C→E→D
A→B→C→E→D
(填字母).A.在盛适量水的烧杯中滴加少量浓H2SO4后搅拌均匀并冷却到室温
B.称取一定质量的FeSO4晶体样品
C.将样品溶于已配制的稀H2SO4中,用玻璃棒搅拌至样品充分溶解
D.过滤后,将滤液转移到容量瓶中,加水稀释至指定刻度
E.往硫酸亚铁溶液中加入稍过量的铁粉,充分搅拌,静置一段时间至不再有气体冒出为止
(2)回答下列问题:
①将样品溶于稀H2SO4,而不直接溶于水的理由是
防止Fe2+、Fe3+水解
防止Fe2+、Fe3+水解
.②在配制硫酸亚铁溶液时,需加入铁粉的理由是
将药品中Fe3+还原并防止Fe2+被氧化
将药品中Fe3+还原并防止Fe2+被氧化
.Ⅱ.标定FeSO4溶液的浓度
(1)用移液管量取20.00mL FeSO4溶液放入锥形瓶中,用0.10mol?L-1的酸性KMnO4溶液滴至终点,耗去KMnO4溶液20.00mL,若生成物中Mn元素全部呈+2价,滴定反应的离子方程式为
5Fe2++8H++MnO4-═5Fe3++Mn2++4H2O
5Fe2++8H++MnO4-═5Fe3++Mn2++4H2O
,据此可测得FeSO4溶液的物质的量浓度为0.5
0.5
mol?L-1.(2)滴定时选用
C
C
(A.石蕊 B.酚酞 C.不用指示剂,填字母)为指示剂,理由是可利用KMnO4溶液紫色不再褪去判断滴定终点
可利用KMnO4溶液紫色不再褪去判断滴定终点
.平衡指的是两个相反方向的变化最后所处的运动状态;在平衡时,两种变化仍在继续进行,但是它们的速率相等;根据变化的性质可分为物理平衡和化学平衡,中学阶段涉及的平衡有气体可逆反应的平衡、酸碱电离平衡、水解平衡及沉淀-溶解平衡等等.
(1)现有容积为1L的恒温恒容密闭容器,向其中加入2mol A气体和2mol B气体后发生如下反应:
A(g)+B(g)?C(g)△H=-a kJ?mol-1
20s后,反应达到平衡状态,生成1mol C气体,放出热量Q1kJ.回答下列问题.
①计算20s内B气体的平均化学反应速率为
②保持容器温度和容积不变,若改为向其中加入1mol C气体,反应达到平衡时,吸收热量Q2 kJ,则Q1与Q2的相互关系正确的是
(A)Q1+Q2=a (B) Q1+2Q2<2a (C)Q1+2Q2>2a (D)Q1+Q2<a
③在原平衡基础上,保持容器温度和容积不变,向容器中再通入b mol A气体(b>0)时,v(正)
,则b=
(2)常温下,将V mL、0.1000mol?L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol?L-1醋酸溶液中,充分反应.回答下列问题(忽略溶液体积的变化).
①如果溶液pH=7,此时V的取值
②如果V=40.00,则此时溶液中c(OH-)-c(H+)-c(CH3COOH)=
或0.033
或0.033mol?L-1.
查看习题详情和答案>>
(1)现有容积为1L的恒温恒容密闭容器,向其中加入2mol A气体和2mol B气体后发生如下反应:
A(g)+B(g)?C(g)△H=-a kJ?mol-1
20s后,反应达到平衡状态,生成1mol C气体,放出热量Q1kJ.回答下列问题.
①计算20s内B气体的平均化学反应速率为
0.05mol/(L?s)
0.05mol/(L?s)
,写出该反应的平衡常数表达式K=
| c(C) |
| c(A)?c(B) |
K=
.| c(C) |
| c(A)?c(B) |
②保持容器温度和容积不变,若改为向其中加入1mol C气体,反应达到平衡时,吸收热量Q2 kJ,则Q1与Q2的相互关系正确的是
C
C
(填字母).(A)Q1+Q2=a (B) Q1+2Q2<2a (C)Q1+2Q2>2a (D)Q1+Q2<a
③在原平衡基础上,保持容器温度和容积不变,向容器中再通入b mol A气体(b>0)时,v(正)
>
>
v(逆)(填“>”、“<”或“=”),重新达平衡后,C气体的平衡体积分数?(C)=| 1 |
| 3 |
1.33
1.33
.(2)常温下,将V mL、0.1000mol?L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol?L-1醋酸溶液中,充分反应.回答下列问题(忽略溶液体积的变化).
①如果溶液pH=7,此时V的取值
<
<
20.00(填“>”、“<”或“=”),而溶液中c(Na+)、c(CH3COO-)、c(H+)、c(OH-)的大小关系为c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
.②如果V=40.00,则此时溶液中c(OH-)-c(H+)-c(CH3COOH)=
| 1 |
| 30 |
| 1 |
| 30 |
盐酸、硫酸和硝酸是中学阶段常见的三种强酸.请就三者与金属铜的反应情况,回答下列问题:
(1)①在100mL 18mol?L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为
查看习题详情和答案>>
(1)①在100mL 18mol?L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
B
B
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
NO2、NO
NO2、NO
,反应中所消耗的硝酸的物质的量可能为C
C
.A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为
Cu+H2O2+2HCl=CuCl2+2H2O
Cu+H2O2+2HCl=CuCl2+2H2O
.