摘要:7.[广西南宁武鸣高中09届高中化学2月调研试卷]时.水的Kw=1×10-12.则该温度(填“> .“< 或“= ) 25℃.其理由是 . ⑴将此温度下pH=11的NaOH与pH=1 HCl等体积混合.混合后溶液pH= , ⑵将此温度下pH=9的Ba(OH)2溶液取出1mL.加水稀释至10000mL.则稀释后溶液 c(Ba2+)﹕c(OH-)= , ⑶将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合: ①若所得混合液为中性.则a﹕b= , ②若所得混合液的pH=2.则a﹕b= . 答案.> , 水的电离过程是吸热过程, 升高温度, 能促进水的电离, 水的离子积常数增大, 温度大于25℃ 1:20 ②9:11 8.[2009年阳泉市十五中学高三第二次理综考试化学部分]常温下.向0.1mol/L的H2SO4溶液中逐滴加入0.1mol/L的Ba(OH)2溶液.生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示.下列说法中正确的是 A.a~d溶液的pH:a<b<c<d B.a~d溶液的导电能力:a<b<c<d C.b处溶液的c(H+)与d处溶液的c(OH-)相等 D.c处溶液和d处溶液均呈碱性
网址:http://m.1010jiajiao.com/timu_id_4223945[举报]
(08广西南宁二中模拟)设NA代表阿伏加德罗常数,下列说法正确的是 ( )
A.1.8g重水(D2O)中含NA个中子
B.在铜与足量硫蒸汽的反应中,1 mol铜失去的电子数为2NA
C.在常温常压下,11.2L氧气所含的原子数为NA
D.0.5mol铝与足量烧碱溶液反应,转移的电子数为1.5NA
查看习题详情和答案>>硝苯吡啶(心痛定)是治疗心血管疾病的一种重要药物,其合成路线如下:
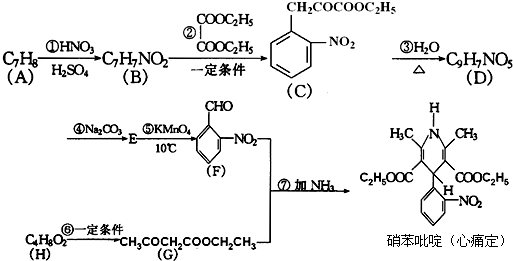
请回答下列问题:
(1)硝苯吡啶(心痛定)的化学式为
(2)指出反应②的反应类型:
(3)写出反应③的化学方程式: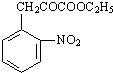 +H2O
+H2O
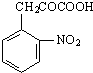 +C2H5OH
+C2H5OH +H2O
+H2O
 +C2H5OH.
+C2H5OH.
(4)方程式②和方程式⑥有一定的相似性,且含同一种产物,请写出(H)的结构简式
(5)H的同分异构体在一定条件下能与氢氧化钠溶液反应,则符合该条件的H的同分异构体有
(6)反应②是一种重要的酰基化反应,高中阶段也有一种酰基化反应----阿司匹林的制备,阿司匹林产品中通常含有一定的杂质(杂质不与酸反应),通常采用返滴定法测定阿司匹林片剂中乙酰水杨酸的含量.现称取10片该产品(设总质量为w总g),研细混匀后,准确称取一定量(Gg)药粉于锥形瓶中,加入V1mL(过量)的NaOH标准溶液[浓度c(NaOH) mol?L-1],于水浴上加热使乙酰基水解完全后,再用HCl标准溶液[浓度c(HCl) mol?L-1]回滴,以酚酞为指示剂,耗去HCl溶液V2 mL.请列出求算每片药中含有乙酰水杨酸的质量(g/片)的计算式:
×
×
.
已知:①乙酰水杨酸溶于过量NaOH溶液的离子方程式可表示为:
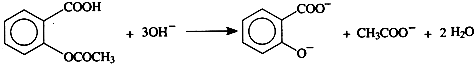
②乙酰水杨酸的摩尔质量为180.2g?mol-1,水杨酸的pKal=3.0,pKa2=13.1,乙酸的pKa=4.75 pKa=-lgKa.
查看习题详情和答案>>

请回答下列问题:
(1)硝苯吡啶(心痛定)的化学式为
C19H22N2O6
C19H22N2O6
.(2)指出反应②的反应类型:
取代反应
取代反应
.(3)写出反应③的化学方程式:
 +H2O
+H2O
| ||
| △ |
 +C2H5OH
+C2H5OH +H2O
+H2O
| ||
| △ |
 +C2H5OH
+C2H5OH(4)方程式②和方程式⑥有一定的相似性,且含同一种产物,请写出(H)的结构简式
CH3COOC2H5
CH3COOC2H5
.写出反应⑥的方程式:2CH3COOC2H5
CH3COCH2COOC2H5+C2H5OH
| 一定条件下 |
2CH3COOC2H5
CH3COCH2COOC2H5+C2H5OH
| 一定条件下 |
(5)H的同分异构体在一定条件下能与氢氧化钠溶液反应,则符合该条件的H的同分异构体有
5
5
种(不包含H本身).G的一种链状结构的同分异构体的核磁共振氢谱中只有2个吸收峰,其结构简式为CH3CH2-CO-O-CO-CH2CH3或CH3-CO-CH2-O-CH2-CO-CH3
CH3CH2-CO-O-CO-CH2CH3或CH3-CO-CH2-O-CH2-CO-CH3
(任写一种).(6)反应②是一种重要的酰基化反应,高中阶段也有一种酰基化反应----阿司匹林的制备,阿司匹林产品中通常含有一定的杂质(杂质不与酸反应),通常采用返滴定法测定阿司匹林片剂中乙酰水杨酸的含量.现称取10片该产品(设总质量为w总g),研细混匀后,准确称取一定量(Gg)药粉于锥形瓶中,加入V1mL(过量)的NaOH标准溶液[浓度c(NaOH) mol?L-1],于水浴上加热使乙酰基水解完全后,再用HCl标准溶液[浓度c(HCl) mol?L-1]回滴,以酚酞为指示剂,耗去HCl溶液V2 mL.请列出求算每片药中含有乙酰水杨酸的质量(g/片)的计算式:
| ||
| 1000G |
| W总 |
| 10 |
| ||
| 1000G |
| W总 |
| 10 |
已知:①乙酰水杨酸溶于过量NaOH溶液的离子方程式可表示为:

②乙酰水杨酸的摩尔质量为180.2g?mol-1,水杨酸的pKal=3.0,pKa2=13.1,乙酸的pKa=4.75 pKa=-lgKa.
(2010?南宁一模)已知A、B、C、D为四种单质,常温时,A、B是气体,C、D是固体且D显淡黄色.E、F、G、H、I为五种化合物,E为气体且极易溶于水成为无色溶液,F不溶于水,G溶于水得黄棕色溶液.这九种物质间反应的转化关系如图所示:

(I)写出四种单质的化学式
A
(2)用电子式表示E的形成过程
 ;化台物I的晶体类型为
;化台物I的晶体类型为
(3)写出G+I→H+D+E的化学方程式
(4)某工厂用B制漂白粉.为测定该工厂制得的漂白粉中有效成分的含量,兴趣小组的同学进行了如下实验:称取漂白粉样品2.0g,研磨后溶解,配置成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为:
查看习题详情和答案>>

(I)写出四种单质的化学式
A
H2
H2
,BCl2
Cl2
,CFe
Fe
,DS
S
.(2)用电子式表示E的形成过程


分子晶体
分子晶体
其空间构型为V型
V型
.(3)写出G+I→H+D+E的化学方程式
2FeCl3+H2S═2FeCl2+S↓+2HCl
2FeCl3+H2S═2FeCl2+S↓+2HCl
.(4)某工厂用B制漂白粉.为测定该工厂制得的漂白粉中有效成分的含量,兴趣小组的同学进行了如下实验:称取漂白粉样品2.0g,研磨后溶解,配置成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为:
2I-+ClO-+2H+=I2+Cl-+H2O
2I-+ClO-+2H+=I2+Cl-+H2O
.静置,待完全反应后,用0.1mol?L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去Na2S2O3溶液20.00ml.则该漂白粉样品中有效成分的质量分数为35.75%
35.75%
(保留到小数点后两位).(2010?南宁一模)Ⅰ、下面a~e是中学化学实验中常见的几种定量仪器:
A、量筒b、容量瓶c、滴定管d、托平天平e、温度计
(1)上述仪器中标有0刻度的玻璃仪器是
(2)若用上述仪器测定中和热,则缺少的玻璃仪器为烧杯、
Ⅱ、某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c表示止水夹).
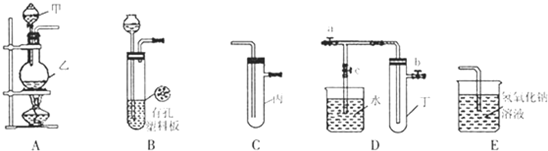
请按要求填空:
(1)利用B装置可制取的气体有
(2)A、B、E相连后的装置可用于制取Cl2并进行相关的性质实验.
若在丙中加入适量水,即可制得氯水.将所得氯水分成两份,进行如下①、②两个实验,实验操作、现象、结论如下:
请你评价实验①、②的结论是否合理?
(3)将B、D、E装置相连后,在B中盛装浓硝酸和铜片(铜片放在有孔塑料板上),制得NO2后,进行以下实验.
①欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹
②试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满溶液,则原NO2与通入O2的物质的量之比为
③尾气吸收的装置是
查看习题详情和答案>>
A、量筒b、容量瓶c、滴定管d、托平天平e、温度计
(1)上述仪器中标有0刻度的玻璃仪器是
cd
cd
(填序号).(2)若用上述仪器测定中和热,则缺少的玻璃仪器为烧杯、
环形玻璃搅拌棒
环形玻璃搅拌棒
.Ⅱ、某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c表示止水夹).

请按要求填空:
(1)利用B装置可制取的气体有
氢气、二氧化碳(硫化氢、一氧化氮、二氧化氮)
氢气、二氧化碳(硫化氢、一氧化氮、二氧化氮)
(写出两种即可).(2)A、B、E相连后的装置可用于制取Cl2并进行相关的性质实验.
若在丙中加入适量水,即可制得氯水.将所得氯水分成两份,进行如下①、②两个实验,实验操作、现象、结论如下:
| 实验序号 | 实验操作 | 现象 | 结论 |
| ① | 将氯水滴入品红溶液 | 溶液褪色 | 氯水有漂泊作用 |
| ② | 氯水中加入NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
实验①结论合理、实验②结论不合理
实验①结论合理、实验②结论不合理
;若不合理,请说明理由:制取的氯气中含有氯化氢气体,氯化氢溶于水后能与碳酸氢钠粉末反应产生气泡
制取的氯气中含有氯化氢气体,氯化氢溶于水后能与碳酸氢钠粉末反应产生气泡
.(3)将B、D、E装置相连后,在B中盛装浓硝酸和铜片(铜片放在有孔塑料板上),制得NO2后,进行以下实验.
①欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹
ab
ab
,再打开止水夹c
c
,使烧杯中的水进入试管丁的操作是双手紧握试管丁使试管中气体溢出,二氧化氮与水接触后即可引发烧杯中的水倒流入试管丁
双手紧握试管丁使试管中气体溢出,二氧化氮与水接触后即可引发烧杯中的水倒流入试管丁
.②试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满溶液,则原NO2与通入O2的物质的量之比为
4:1
4:1
.③尾气吸收的装置是
E
E
(填序号).