摘要:①在 实验室中要想把明矾中的铝离子全部沉淀出来应选择的试剂是 ②在盛有2mLFeCl3溶液的试管中加入过量铁粉.充分反应后.溶液由 色变为 色,反应方程式为 .反应中氧化剂是 ,还原剂是 .再滴入2滴KSCN溶液.溶液颜色 ,再加入几滴氯水.观察溶液颜色变为 .说明 ,反应方程式为 .还原剂是 .
网址:http://m.1010jiajiao.com/timu_id_4223755[举报]
 (1)阅读、分析下列两个材料:材料一:
(1)阅读、分析下列两个材料:材料一:材料二:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g?cm3 | 溶解性 |
| 乙二醇(C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意以互溶 |
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤”的方法 D.分液法
①将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用
C
C
;②将乙二醇和丙三醇相互分离的最佳方法是
A
A
.(2)阅读材料三:在溶解性方面,Br2(溴)与I2很相似,其稀的水溶液显黄色.在实验室里从溴水(Br2的水溶液)中提取Br2和提取I2的方法相似.回答下列问题:
①常用的提取方法是
萃取
萃取
,化学试剂是CCl4
CCl4
,最主要的仪器是分液漏斗
分液漏斗
.②若观察发现提取Br2以后的水还有颜色,解决该问题的方法是
再进行萃取,直到水为无色,将各次分离出来的含溴的四氯化碳溶液合并起来
再进行萃取,直到水为无色,将各次分离出来的含溴的四氯化碳溶液合并起来
. 1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18g?cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用如图所示装置制备1,2-二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).
1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18g?cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用如图所示装置制备1,2-二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.
(2)瓶b的两个作用是
(3)容器c中NaOH溶液的作用是:
(4)瓶e的作用是
1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18g?cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2-二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).

填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象.
(3)容器c中NaOH溶液的作用是:
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因.
查看习题详情和答案>>

填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.
CH3CH2OH
CH2=CH2↑+H2O,CH2=CH2+Br2→CH2BrCH2Br
| 浓硫酸 |
| 170℃ |
CH3CH2OH
CH2=CH2↑+H2O,CH2=CH2+Br2→CH2BrCH2Br
| 浓硫酸 |
| 170℃ |
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象.
b中水面会下降,玻璃管中的水柱会上升,甚至溢出
b中水面会下降,玻璃管中的水柱会上升,甚至溢出
.(3)容器c中NaOH溶液的作用是:
除去乙烯中带出的酸性气体.或答除去CO2、SO2
除去乙烯中带出的酸性气体.或答除去CO2、SO2
.(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因.
①乙烯发生(或通过液溴)速度过快
②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃(答“控温不当“亦可)
②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃(答“控温不当“亦可)
①乙烯发生(或通过液溴)速度过快
②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃(答“控温不当“亦可)
.②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃(答“控温不当“亦可)
已知下列数据:
学生在实验室制取乙酸乙酯的主要步骤如下:
①在30mL的大试管A中按体积比2:3:2的比例配制浓硫酸、乙醇和乙酸的混合溶液;
②按图1连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5-10min;
③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层、洗涤、干燥.
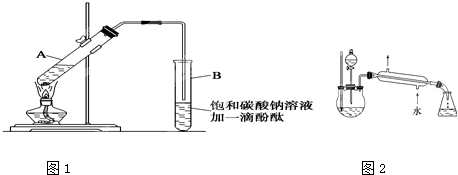
请根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热操作,其主要理由是
(4)指出步骤③所观察到的现象:
A.P2O5B.无水Na2SO4 C.碱石灰 D.NaOH固体
(5)某化学课外小组设计了如图2所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),与上图装置相比,此装置的主要优点有
查看习题详情和答案>>
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g/cm3) |
| 乙醇 | -117.0 | 78.0 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸(98%) | - | 338.0 | 1.84 |
①在30mL的大试管A中按体积比2:3:2的比例配制浓硫酸、乙醇和乙酸的混合溶液;
②按图1连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5-10min;
③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层、洗涤、干燥.

请根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为
应先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,最后加入冰醋酸
应先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,最后加入冰醋酸
.写出制取乙酸乙酯的化学反应方程式CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
| 浓硫酸 |
| 加热 |
CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O
.| 浓硫酸 |
| 加热 |
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)
BC
BC
.A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热操作,其主要理由是
减少乙酸乙醇的挥发,减少副反应的发生
减少乙酸乙醇的挥发,减少副反应的发生
.(4)指出步骤③所观察到的现象:
试管B中的液体分成上下两层,上层无色,下层为红色液体,振荡后下层液体的红色变浅
试管B中的液体分成上下两层,上层无色,下层为红色液体,振荡后下层液体的红色变浅
,分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为(填字母)B
B
.A.P2O5B.无水Na2SO4 C.碱石灰 D.NaOH固体
(5)某化学课外小组设计了如图2所示的制取乙酸乙酯的装置(图中的铁架台、铁夹、加热装置已略去),与上图装置相比,此装置的主要优点有
①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的发生;②增加了分液漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加了冷凝装置,有利于收集产物乙酸乙酯.
①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的发生;②增加了分液漏斗,有利于及时补充反应混合液,以提高乙酸乙酯的产量;③增加了冷凝装置,有利于收集产物乙酸乙酯.
. 溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:
溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:NaBr+H2SO4→NaHSO4+HBr
CH3CH2OH+HBr
| 硫酸 |
某课外小组欲在实验室制备溴乙烷的装置如图.数据如表.
| 物质 数据 |
乙醇 | 溴乙烷 | 1,2-二溴乙烷 | 乙醚 | 浓硫酸 |
| 密度/g?cm-3 | 0.79 | 1.46 | 2.2 | 0.71 | 1.84 |
| 熔点(℃) | -130 | -119 | 9 | -116 | 10 |
| 沸点(℃) | 78.5 | 38.4 | 132 | 34.6 | 338 |
| 在水中的溶解度(g/100g水) | 互溶 | 0.914 | 1 | 7.5 | 互溶 |
(1)加入药品之前须做的操作是:
(2)装置B的作用是除了使溴乙烷馏出,还有一个目的是
(3)反应时有可能生成SO2和一种红棕色气体,可选择氢氧化钠溶液除去该气体,有关的离子方程式是
(4)实验中采用80%硫酸,而不能用98%浓硫酸,一方面是为了减少副反应,另一方面是为了
(5)粗产品中含有的主要有机液体杂质是