摘要:22.X.Y.Z.Q.E五种元素中.X原子核外的M层中只有两对成对电子.Y原子核外的L层电子数是K层的两倍.Z是地壳内含量最高的元素.Q的核电荷数是X与Z的核电荷数之和.E在元素周期表的各元素中电负性最大.请回答下列问题: (1)X.Y的元素符号依次为 . , (2)XZ2与YZ2分子的立体结构分别是 和 .相同条件下两者在水中的溶解度较大的是 (写分子式).理由是 , (3)Q的元素符号是 .它属于第 周期.它的核外电子排布式为 .在形成化合物时它的最高化合价为 , (4)用氢键表示式写出E的氢化物溶液中存在的所有氢键 .
网址:http://m.1010jiajiao.com/timu_id_4223259[举报]
 (1)(2011?江苏高考,节选)Ag2O2是银锌碱性电池的正极活性物质,其电解质溶液为 KOH 溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池反应方程式:
(1)(2011?江苏高考,节选)Ag2O2是银锌碱性电池的正极活性物质,其电解质溶液为 KOH 溶液,电池放电时正极的Ag2O2转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池反应方程式:Ag2O2+2Zn+4KOH+2H2O═2K2Zn(OH)4+2Ag
Ag2O2+2Zn+4KOH+2H2O═2K2Zn(OH)4+2Ag
.(2)(2011?山东高考,节选)如图为钠高能电池的结构示意图,该电池的工作温度为320℃左右,电池反应为2Na+xS═Na2Sx,正极的电极反应式为
xS+2e-═Sx2-
xS+2e-═Sx2-
.M(由Na2O和Al2O3制得)的两个作用是导电和隔离钠与硫
导电和隔离钠与硫
.与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的4.5
4.5
倍.(3)(2011?新课标高考,节选)以甲醇为燃料的电池中,电解质溶液为酸性,负极的反应式为
CH3OH+H2O-6e-═CO2+6H+
CH3OH+H2O-6e-═CO2+6H+
,正极的反应式为| 3 |
| 2 |
| 3 |
| 2 |
96.6%
96.6%
(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比,甲醇的燃烧热为△H=-726.5kJ/mol).低碳经济是以低能耗、低污染、低排放为基础的经济模式,低碳循环正成为科学家研究的主要课题.
Ⅰ.最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇.该构想技术流程如下:
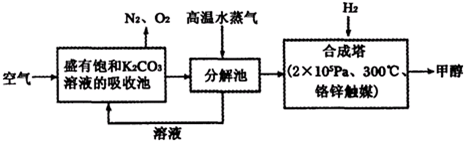
(1)向分解池中通入高温水蒸气的作用是 .
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)=H2O(1)△H=-44.0kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 .
Ⅱ.一氧化碳与氢气也可以合成甲醇,反应为CO(g)+2H2(g)?CH3OH(g)△H<0.
(1)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应达到平衡,测得c(H2)=2.2mol?L-1,则CO的转化率为 .
(2)T1℃时,此反应的平衡常数为K(T1)=50.此温度下,在一个2L的密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v正 v逆值(填“>”、“<”或“=”).
②若其他条件不变时,只改变反应的某一个条件,下列说法正确的是 .
A.若达到新平衡时c(CO)=0.3mol/L,平衡一定逆向移动
B.若将容器体积缩小到原来的一半,达到新平衡时,0.2mol/L<c(CO)<0.4mol/L
C.若向容器中同时加入0.4mol CO和0.8mol CH3OH(g),平衡不移动
D.若升高温度,平衡常数将增大
Ⅲ.CO2和SO2的处理是许多科学家都在着力研究的重点.有学者想以如图所示装置用燃料电池原理将CO2、SO2转化为重要的化工原料.
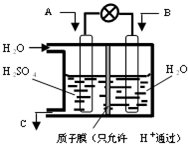
(1)若A为CO2,B为H2,C为CH3OH,电池总反应式为CO2+3H2=CH3OH+H2O,则正极反应式为 .
(2)若A为SO2,B为O2,C为H2SO4,则负极反应式为 .
查看习题详情和答案>>
Ⅰ.最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇.该构想技术流程如下:

(1)向分解池中通入高温水蒸气的作用是
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)=H2O(1)△H=-44.0kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
Ⅱ.一氧化碳与氢气也可以合成甲醇,反应为CO(g)+2H2(g)?CH3OH(g)△H<0.
(1)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应达到平衡,测得c(H2)=2.2mol?L-1,则CO的转化率为
(2)T1℃时,此反应的平衡常数为K(T1)=50.此温度下,在一个2L的密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol?L-1) | 0.2 | 0.2 | 0.4 |
②若其他条件不变时,只改变反应的某一个条件,下列说法正确的是
A.若达到新平衡时c(CO)=0.3mol/L,平衡一定逆向移动
B.若将容器体积缩小到原来的一半,达到新平衡时,0.2mol/L<c(CO)<0.4mol/L
C.若向容器中同时加入0.4mol CO和0.8mol CH3OH(g),平衡不移动
D.若升高温度,平衡常数将增大
Ⅲ.CO2和SO2的处理是许多科学家都在着力研究的重点.有学者想以如图所示装置用燃料电池原理将CO2、SO2转化为重要的化工原料.

(1)若A为CO2,B为H2,C为CH3OH,电池总反应式为CO2+3H2=CH3OH+H2O,则正极反应式为
(2)若A为SO2,B为O2,C为H2SO4,则负极反应式为
(2011?中山三模)实验室用浓盐酸和二氧化锰制备氯气并用所制氯气制备少量氯水的装置图如下,回答有关问题.
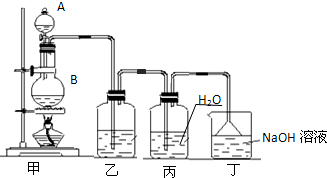
(1)从仪器A向仪器B中加入浓盐酸的操作方法是
(2)装置乙中盛放的试剂是
(3)写出氯气与水反应的化学方程式
(4)某同学设计了一个实验方案以证明新制氯水中含有次氯酸.他所用的试剂如下:
新制氯水 0.5mol.L-1CaCl2溶液 品红溶液 CaCO3粉末
请你协助完成实验方案.
步骤一:取5mL0.5mol.L-1CaCl2溶液于试管中,滴入3滴品红溶液,振荡,溶液不褪色.
步骤二:取5mL新制氯水于试管中,
步骤三:
说明新制氯水中存在次氯酸的实验现象是
(5)设计步骤一的理由是
查看习题详情和答案>>

(1)从仪器A向仪器B中加入浓盐酸的操作方法是
取下分液漏斗上口玻璃塞,旋动活塞,即可放下液体
取下分液漏斗上口玻璃塞,旋动活塞,即可放下液体
.反应中控制氯气产生速率大小的方法是通过控制浓盐酸的加入速度来控制氯气的产生速率
通过控制浓盐酸的加入速度来控制氯气的产生速率
.(2)装置乙中盛放的试剂是
饱和食盐水
饱和食盐水
,其作用是除去氯气中的氯化氢
除去氯气中的氯化氢
.(3)写出氯气与水反应的化学方程式
Cl2+H2O=HCl+HClO
Cl2+H2O=HCl+HClO
.(4)某同学设计了一个实验方案以证明新制氯水中含有次氯酸.他所用的试剂如下:
新制氯水 0.5mol.L-1CaCl2溶液 品红溶液 CaCO3粉末
请你协助完成实验方案.
步骤一:取5mL0.5mol.L-1CaCl2溶液于试管中,滴入3滴品红溶液,振荡,溶液不褪色.
步骤二:取5mL新制氯水于试管中,
加入碳酸钙粉末充分反应至溶液无色
加入碳酸钙粉末充分反应至溶液无色
.步骤三:
取上层清液于另一试管中加入3滴品红溶液,振荡
取上层清液于另一试管中加入3滴品红溶液,振荡
.说明新制氯水中存在次氯酸的实验现象是
品红溶液褪色
品红溶液褪色
.(5)设计步骤一的理由是
氯水与碳酸钙反应后生成氯化钙溶液,为证明品红溶液褪色是次氯酸的作用,须实验证明氯化钙溶液不具漂白性(或“排除氯化钙溶液的干扰”)
氯水与碳酸钙反应后生成氯化钙溶液,为证明品红溶液褪色是次氯酸的作用,须实验证明氯化钙溶液不具漂白性(或“排除氯化钙溶液的干扰”)
.温度为T时,向2.0L恒容密闭容器中充入2.0mol NO2,反应2NO2(g)?N2O4(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:
|
查看习题详情和答案>>