摘要:(3)B C: ,
网址:http://m.1010jiajiao.com/timu_id_42228[举报]
I卷 选择题(74分)
1
2
3
4
5
6
7
8
9
10
B
C
C
C
A
B
B
D
C
C
11
12
13
14
15
16
17
18
C
A
D
B
D
C
C
A
19
20
21
22
23
B
BD
C
BD
AB
II卷 非选择题(76分)
三、填空题(26分)
24.(8分)⑴⑥;⑧ ⑵①;②;④ ⑶③;⑤;⑦
25.(18分)(1)Ne、F、F2、Na (2)NaOH、HClO4、Al(OH)3 (3)HF (4)Na

 四、推断题(18分)
四、推断题(18分)
26.(9分)(1)Na SO3 Na2SO4 (2)Na+

 2SO3
2SO3 

 CO2↑+2SO2↑+2H2O?(2)④②①③
CO2↑+2SO2↑+2H2O?(2)④②①③ Ⅰ:如图表示800℃时,A、B、C三种气体物质的浓度随时间的变化情况,t1是达到平衡状态的时间.试回答:
Ⅰ:如图表示800℃时,A、B、C三种气体物质的浓度随时间的变化情况,t1是达到平衡状态的时间.试回答:
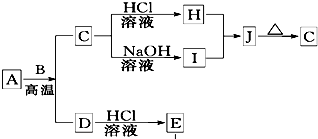 B、D是常见金属单质,A是一种红棕色金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体.
B、D是常见金属单质,A是一种红棕色金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体.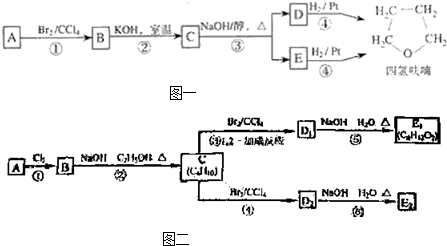
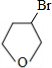


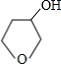 +NaBr
+NaBr