摘要:.能正确表示下列反应的离子方程式是 A 甲酸钠溶液和盐酸反应:HCOO-+H+=HCOOH B 硫化钠的第一步水解:S2-+2H2OH2S+2OH- C 醋酸钡溶液和硫酸反应:Ba2++SO42-=BaSO4↓ D 氢氧化钙溶液和碳酸氢镁反应:Ca2++OH-+HCO3-=CaCO3↓+H2O
网址:http://m.1010jiajiao.com/timu_id_4220573[举报]
(2005·广东,13)铊(Tl)是某超导体材料的组成元素之一,与铝同族,位于第六周期. 与Ag在酸性介质中发生反应:
与Ag在酸性介质中发生反应: .下列推断正确的是
.下列推断正确的是
[ ]
A. 的最外层有1个电子
的最外层有1个电子
B. 的氧化性比
的氧化性比 弱
弱
C.Tl能形成+3价和+1价的化合物
D. 的还原性比Ag强
的还原性比Ag强
(2005·江苏,13)A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3∶4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z.下列叙述正确的是
[ ]
A.X、Y、Z的稳定性逐渐减弱
B.A、B、C、D只能形成5种单质
C.X、Y、Z三种化合物的熔沸点逐渐升高
D.自然界中存在多种由A、B、C、D四种元素组成的化合物
查看习题详情和答案>>2005年11月13日,地处吉林市的中石油吉林石化公司101厂一化工车间连续发生爆炸,造成6死70伤的严重后果.爆炸导致1个硝基苯储罐、2个苯储罐报废,导致苯酚、苯胺停产.爆炸过程还产生了大量的浓烟和强烈的刺激性气味,造成了空气污染.
(1)上述材料中提到了四种有机物,请你写出其中两种有机物的结构简式:
①
 ;②
;②
 .
.
(2)爆炸过程中,产生了大量黑烟,其原因是:
(3)上述有苦杏仁味的有机物是
A.溶解在江水中 B.浮在水面上 C.沉降到水底
(4)硝基苯是制造染料的重要原料,但是硝基苯进入人体,严重危害人体健康,写出实验室由苯制取硝基苯反应的化学方程式: +HO-NO3
+HO-NO3
 +H2O
+H2O +HO-NO3
+HO-NO3
 +H2O.
+H2O.
查看习题详情和答案>>
(1)上述材料中提到了四种有机物,请你写出其中两种有机物的结构简式:
①




(2)爆炸过程中,产生了大量黑烟,其原因是:
有机物不完全燃烧
有机物不完全燃烧
;上述爆炸事故带来的危害并没有结束,11月14日,吉化公司东10号线入江口处水样有强烈苦杏仁气味,苯、硝基苯、二甲苯等主要污染物指标均超过国家标准.硝基苯的浓度更是超过了国家标准的33.4倍.11月23日被污染的江水流经哈尔滨,造成哈尔滨停止供水4天的严重后果.(3)上述有苦杏仁味的有机物是
硝基苯
硝基苯
,它在江水中的主要存在形式是C
C
.(填序号)A.溶解在江水中 B.浮在水面上 C.沉降到水底
(4)硝基苯是制造染料的重要原料,但是硝基苯进入人体,严重危害人体健康,写出实验室由苯制取硝基苯反应的化学方程式:
 +HO-NO3
+HO-NO3| 浓H2SO4 |
| △ |
 +H2O
+H2O +HO-NO3
+HO-NO3| 浓H2SO4 |
| △ |
 +H2O
+H2O中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是
A.电解水制氢:2H2O
2H2↑+O2↑
B.高温使水分解制氢:2H2O
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O
2H2↑+O2↑
D.天然气制氢:CH4+H2O
CO+3H2
(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示.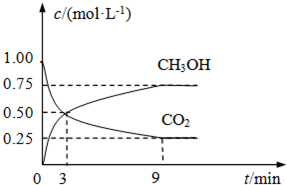
①从3min到9min,v(H2)=
②能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平衡常数:
下列说法正确的是
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高.
查看习题详情和答案>>
(1)有效“减碳”的手段之一是节能,下列制氢方法最节能的是
C
C
A.电解水制氢:2H2O
| ||
B.高温使水分解制氢:2H2O
| ||
C.太阳光催化分解水制氢:2H2O
| ||
| 太阳光 |
D.天然气制氢:CH4+H2O
| 高温 |
(2)CO2可转化成有机物实现碳循环.在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示.

①从3min到9min,v(H2)=
0.125
0.125
mol?L-1?min-1.②能说明上述反应达到平衡状态的是
D
D
(填编号).A.反应中CO2与CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成.参考合成反应CO(g)+2H2(g)?CH3OH(g)的平衡常数:
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
AC
AC
.A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行,说明该反应△S<0
C.在T℃时,1L密闭容器中,投入0.1mol CO和0.2mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5Mpa)和250℃,是因为此条件下,原料气转化率最高.