摘要:8.答案:.NO2 .N2O4 ,(3).As2S5 ,(4).①.NH3>AsH3>PH3 .NH3分子间存在氢键.使得分子间结合力增大.沸点反常地高.AsH3和PH3 是结构相似的分子晶体.相对分子质量越大.分子间作用力越大.沸点越高.AsH3>PH3.总顺序为:NH3>AsH3>PH3 ,②.SiH4 .正四面体结构.PH3 .三角锥形.H2S.角形或V形.(5).SiCl4+4NH3Si(NH2)4+4HCl 3Si(NH2)48NH3+Si3N4 解析:元素Q.R.W.Y与元素X相邻.相互间的位置关系如右: ,Y的最高化合价氧化物的水化 物是强酸.Y是N .S .Cl三种元素之一.W的氯化物分子呈正四面体结构.W位于元素周期表的IVA, Q的具有相同化合价且可以相互转变的氧化物中学阶段只有NO2 .N2O4 .Q是N元素.C和N元素不可能形成高温结构陶瓷.根据教材中新型材料的介绍有Si3N4高温结构陶瓷.确定W是硅元素.根据位置关系.X是P元素,X的下方元素是As元素.X的右方元素是S元素,P 和As元素的最高价氧化物对应的水化物都不是强酸.Y是S 元素.所以R是As元素. 要点1:IVA~VIIA元素最低价氢化物的空间结构类型.氧化物类型是高考时的热点. 要点2:NH3 .H2O .HF的沸点比同族非金属氢化物的沸点反常的高.是因为它们分子间能形成氢键分子键作用力明显增大的缘故.
网址:http://m.1010jiajiao.com/timu_id_4210243[举报]
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.(以下答案的W、X、Y、Z必须用相应的元素符号代替)
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.(以下答案的W、X、Y、Z必须用相应的元素符号代替)(1)X的原子结构示意图为


2
2
个未成对电子.(2)XZ与X2W都属于
离子
离子
晶体(写晶体类型);其熔点较高的是Na2O
Na2O
(写化学式),原因是氯离子的半径大于氧离子半径,氧化钠中核间距小且氧离子所带电荷多,氧化钠的晶格能大
氯离子的半径大于氧离子半径,氧化钠中核间距小且氧离子所带电荷多,氧化钠的晶格能大
.(3)YZ4和足量的水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
SiCl4+4H2O=H4SiO4↓+4HCl
SiCl4+4H2O=H4SiO4↓+4HCl
.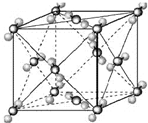 (2009?宿迁模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中B、D、E原子最外电子层的p能级(轨道)上的电子处于半满状态.通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如右下图所示.原子序数为31的元素镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一代半导体材料和GaE为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料.
(2009?宿迁模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中B、D、E原子最外电子层的p能级(轨道)上的电子处于半满状态.通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如右下图所示.原子序数为31的元素镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一代半导体材料和GaE为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料.试回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)基态Ga原子的核外电子排布式为
1s22s22p63s23p63d104s24p1
1s22s22p63s23p63d104s24p1
.(2)A、B、C的第一电离能由大到小的顺序为
N>C>Si
N>C>Si
.(3)B元素的单质分子中有
2
2
个π键,与其互为等电子体的物质的化学式可能为CO(或其他合理答案)
CO(或其他合理答案)
(任写一种).(4)上述A的氧化物分子的中心原子采取
sp
sp
杂化,其晶胞中微粒间的作用力为范德华力
范德华力
.(5)EH3分子的空间构型为
三角锥形
三角锥形
,其沸点与BH3相比低
低
(填“高”或“低”),原因是NH3分子间能形成氢键,AsH3分子间不能形成氢键
NH3分子间能形成氢键,AsH3分子间不能形成氢键
.(6)向CuSO4溶液中逐滴加入BH3的水溶液,得到深蓝色的透明溶液.请写出该反应的离子方程式
Cu2++2NH3?H2O=Cu(OH)2+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-
Cu2++2NH3?H2O=Cu(OH)2+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-
.I.下列说法正确的是 (填字母编号,每小题只有一个正确答案,下同)
A.离子晶体中一定存在离子键,分子晶体中一定存在共价键
B.主族元素形成的单质,从上到下熔沸点逐渐升高
C.N2分子中的共价键是由两个σ键和一个π键组成的
D.以极性键结合的分子不一定是极性分子
II.下列叙述正确的是 .
A.用VSERP理论预测PCl3的立体构型为平面三角形
B.SO2和CO2都是含有极性键的非极性分子
C.在NH+4和[Cu(NH3)4]2+中都存在配位键
D.铝元素的原子核外共有5种不同运动状态的电子
III.Q、R、X、Y、Z五种元素的原子序数逐渐增大.已知Z的原子序数为29,其余均为短周期主族元素.Y原子的价电子排布为msnmpn.R原子核外L层的电子数为奇数,Q、X原子p轨道的电子数分别为2和4.请回答下列问题: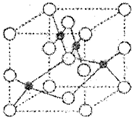
(1)Z2+的核外电子排布式是 .如图是Z和X形成晶体的晶胞结构示意图(O代表X),可确定该晶胞中阴离子的个数为 .
(2)Q与Y形成的最简单气态氢化物分别为A、B,试比较它们的热稳定性并说明理由:
.
(3)Q和X形成的一种化合物甲的相对分子质量为44,则甲的空间构型是 ,中心原子采取的杂化轨道类型是 ,该分子中含有 个π键.
(4)R有多种氧化物,其中乙的相对分子质量最小.在一定条件下,2L的乙气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是 .
(5)这五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于 晶体;Q、R、X三种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)
查看习题详情和答案>>
A.离子晶体中一定存在离子键,分子晶体中一定存在共价键
B.主族元素形成的单质,从上到下熔沸点逐渐升高
C.N2分子中的共价键是由两个σ键和一个π键组成的
D.以极性键结合的分子不一定是极性分子
II.下列叙述正确的是
A.用VSERP理论预测PCl3的立体构型为平面三角形
B.SO2和CO2都是含有极性键的非极性分子
C.在NH+4和[Cu(NH3)4]2+中都存在配位键
D.铝元素的原子核外共有5种不同运动状态的电子
III.Q、R、X、Y、Z五种元素的原子序数逐渐增大.已知Z的原子序数为29,其余均为短周期主族元素.Y原子的价电子排布为msnmpn.R原子核外L层的电子数为奇数,Q、X原子p轨道的电子数分别为2和4.请回答下列问题:

(1)Z2+的核外电子排布式是
(2)Q与Y形成的最简单气态氢化物分别为A、B,试比较它们的热稳定性并说明理由:
(3)Q和X形成的一种化合物甲的相对分子质量为44,则甲的空间构型是
(4)R有多种氧化物,其中乙的相对分子质量最小.在一定条件下,2L的乙气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是
(5)这五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于
已知X,Y,Z,Q为短周期非金属元素,R是长周期元素,X原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍;Y的基态原子有7种不同运动状态的电子;Z元素在地壳中含量最多;Q是电负性最大的元素;R+离子只有三个电子层且完全充满电子。
回答下列问题:(答题时,X、Y、Z、Q、R用所对应的元素符号表示)
(1)X元素为???????? ,X、Y、Z中第一电离能最大的是???????? 。
(2)已知Y2Q2分子存在如图所示的两种结构(球棍模型,短线不一定代表单键):
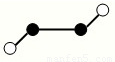
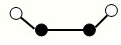
该分子中Y原子的杂化方式是???????? 。
(3)X与Y元素可以形成一种超硬新材料,其晶体部分结构如图所示,有关该晶体的说法正确的是???? (填正确答案编号)。

A.该晶体属于分子晶体
B.此晶体的硬度比金刚石还大
C.晶体的化学式是X3Y4
D.晶体熔化时破坏共价键
(4)有一种AB型分子与Y单质分子互为等电子体,它是一种常用的还原剂,其化学式为????????????? 。
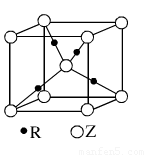
(5)R的基态原子的电子排布式为????????? ,R与Z形成的某离子晶体的晶胞结构如图,则该晶体的化学式为????????? ,该晶体的密度为a g·cm-3,则晶胞的体积是????????? cm3。
查看习题详情和答案>>
(1)下列说法正确的是____(每小题只有一个正确答案,下同)。
A. 离子晶体中一定存在离子键,分子晶体中一定存在共价键
B. 主族元素形成的单质,从上到下熔沸点逐渐升高
C. N2分子中的共价键是由两个σ键和一个π键组成的
D. 以极性键结合的分子不一定是极性分子
(2)下列叙述正确的是____。
A. 用VSEPR理论预测PCl3的立体构型为平面三角形
B. SO2和CO2都是含有极性键的非极性分子
C. 在NH4+和[Cu(NH3)2]2+中都存在配位键
D. 铝元素的原子核外共有5种不同运动状态的电子
Q、R、X、Y、Z五种元素的原子序数逐渐增大。已知Z的原子序数为29,其余均为短周期主族元素。Y 原子的价电子排布为msnmpn,R原子核外L层的电子数为奇数,Q、X原子p轨道的电子数分别为2和4。 请回答下列问题:
(3)Z2+的核外电子排布式是______________。如图是Z和X形成晶体的晶胞结构示意图(○代表X),可确定该品胞中阴离子的个数为___________。
A. 离子晶体中一定存在离子键,分子晶体中一定存在共价键
B. 主族元素形成的单质,从上到下熔沸点逐渐升高
C. N2分子中的共价键是由两个σ键和一个π键组成的
D. 以极性键结合的分子不一定是极性分子
(2)下列叙述正确的是____。
A. 用VSEPR理论预测PCl3的立体构型为平面三角形
B. SO2和CO2都是含有极性键的非极性分子
C. 在NH4+和[Cu(NH3)2]2+中都存在配位键
D. 铝元素的原子核外共有5种不同运动状态的电子
Q、R、X、Y、Z五种元素的原子序数逐渐增大。已知Z的原子序数为29,其余均为短周期主族元素。Y 原子的价电子排布为msnmpn,R原子核外L层的电子数为奇数,Q、X原子p轨道的电子数分别为2和4。 请回答下列问题:
(3)Z2+的核外电子排布式是______________。如图是Z和X形成晶体的晶胞结构示意图(○代表X),可确定该品胞中阴离子的个数为___________。

(4)Q与Y形成的最简单气态氢化物分别为A、B,试比较它们的热稳定性并说明理由:_______________。
(5)Q和X形成的一种化合物甲的相对分子质量为44,则甲的空间构型是_____________。中心原子采取的杂化轨道类型是____,该分子中含有____个π键。
(6)R有多种氧化物,其中乙的相对分子质量最小。在一定条件下,2L的乙气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是_________。
(7)这五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于____ 晶体;Q、R、X三种元素的第一电离能数值由小到大的顺序为____(用元素符号作答)。
查看习题详情和答案>>
(5)Q和X形成的一种化合物甲的相对分子质量为44,则甲的空间构型是_____________。中心原子采取的杂化轨道类型是____,该分子中含有____个π键。
(6)R有多种氧化物,其中乙的相对分子质量最小。在一定条件下,2L的乙气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是_________。
(7)这五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于____ 晶体;Q、R、X三种元素的第一电离能数值由小到大的顺序为____(用元素符号作答)。