摘要:平衡时A.B.C的物质的量之比为l∶3∶4.C的物质的量为y mol. (1)根据题中数据计算.x= .Y= , (2)如图Ⅱ.在体积为V L的恒容密闭容器N中发生上述反应.测得反应过程中气体的平均相对分子质量随时间的变化如图Ⅲ(t0时达平衡).平衡时容器中C的物质的量为z mol.由于反应物A.B的状态未知.则z和y的大小也不确定.请在下表中填入A.B的状态与z.y的大小之间的关系:可能的 情形 A.B是否为气态 z与y的大小关系 M的大小关系 AB ① 是 不是 z=Y 无法确定 ② ③ 2008学年浙江省五校第一次联考化学答案题号123456789101112答案CDDCDDBCAACC题号1314151617181920212223 答案BCDBCDACCCC
网址:http://m.1010jiajiao.com/timu_id_417828[举报]
A、B、C、D、E、F、G是原子序数依次增大的短周期元素,其中A与E、D与G同主族,且D与G核内质子数之和是A与E核内质子数之和的2倍,A与B、C、D可分别形成10电子分子,E、F、G元素最高价氧化物对应水化物之间可相互发生反应,请回答下列问题
(1)E、G两种元素的符号:E
(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是
(3)E在D2中燃烧生成化合物X中阴阳离子个数比为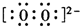
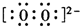 .
.
(4)能够说明可逆反应2CD2(g) C2D4(g)达到平衡状态的标志是
C2D4(g)达到平衡状态的标志是
①单位时间消耗2mol CD2的同时,生成1mol C2D4
②恒温恒压下,混合气体的密度不变
③CD2和C2D4的浓度之比为2:1
④混合气体的颜色不变
⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为
查看习题详情和答案>>
(1)E、G两种元素的符号:E
Na
Na
、GS
S
;F在元素周期表中的位置是第三周期第ⅢA族
第三周期第ⅢA族
.(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是
发生反应Zn+CuSO4═ZnSO4+Cu,形成铜锌-硫酸原电池,反应速率加快
发生反应Zn+CuSO4═ZnSO4+Cu,形成铜锌-硫酸原电池,反应速率加快
.(3)E在D2中燃烧生成化合物X中阴阳离子个数比为
1:2
1:2
;X中的阴离子电子式为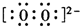
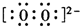
(4)能够说明可逆反应2CD2(g)
 C2D4(g)达到平衡状态的标志是
C2D4(g)达到平衡状态的标志是②④⑤
②④⑤
;①单位时间消耗2mol CD2的同时,生成1mol C2D4
②恒温恒压下,混合气体的密度不变
③CD2和C2D4的浓度之比为2:1
④混合气体的颜色不变
⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为
NaOH+CO2=NaHCO3
NaOH+CO2=NaHCO3
.A、B、C、D、E五种短周期元素的原子序数依次增大,且已知:①其原子半径的大小关系是:D>E>B>C>A;②A、D同主族,可形成离子化合物;③B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;④B、E两元素原子的最外层电子数之和等于A、C、D三种元素原子的最外层电子数之和.请填写下列空白:
(1)常温下,浓度均为0.lmol/L的B、D的最高价氧化物对应的水化物溶液中,水电离出的c(H+)的相对大小关系为X______Y(填写“大于”“于”或“等于”),化合物BA5所属晶体类型为离子晶体,其电子式为______.
(2)在合成BA3的实际生产过程中,常采取______的方法,使气态BA3变成液态后从混合气体中分离出去,以促使化学平衡向生成BA3的方向移动.
(3)E单质与足量的D的最高价氧化物的水化物溶液反应的离子方程式为______;BC2与水反应被氧化与被还原的物质的量之比是______.
(4)已知在298K时,lg B2A4气体燃烧生成B2和A2C气体,放出16.7kJ的热量.该燃烧反应的热化学方程式______.
(5)X、Y分别是B、C与A形成的10电子微粒,请你提供一个能验证X结合H+能力较Y强的离子方程式______.
查看习题详情和答案>>
(1)常温下,浓度均为0.lmol/L的B、D的最高价氧化物对应的水化物溶液中,水电离出的c(H+)的相对大小关系为X______Y(填写“大于”“于”或“等于”),化合物BA5所属晶体类型为离子晶体,其电子式为______.
(2)在合成BA3的实际生产过程中,常采取______的方法,使气态BA3变成液态后从混合气体中分离出去,以促使化学平衡向生成BA3的方向移动.
(3)E单质与足量的D的最高价氧化物的水化物溶液反应的离子方程式为______;BC2与水反应被氧化与被还原的物质的量之比是______.
(4)已知在298K时,lg B2A4气体燃烧生成B2和A2C气体,放出16.7kJ的热量.该燃烧反应的热化学方程式______.
(5)X、Y分别是B、C与A形成的10电子微粒,请你提供一个能验证X结合H+能力较Y强的离子方程式______.
A、B、C、D、E、F、G、H 八种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B、C、D在同一周期,A与E、B与G、D与H分别在同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F的2倍,C和D的最外层电子数之和为11。请回答下列问题:
(1)以上八种元素中非金属所形成的最简单气态氢化物中稳定性最弱的是____________(填化学式),E、F、H所形成的简单离子的半径由大到小的顺序为____________ (用离子符号表示)。
(2)一定条件下,A的单质与C的单质充分反应可生成气体W,W的结构式为___________。由A、D两元素可以组成X、Y两种化台物,X在一定条件下可以分解生成Y,X的电子式为___________。固体化合物
E2D2与化合物E2H的水溶液按物质的量之比1:1反应生成单质H的离子方程式为__________________。
(3)G是非金属元素,其单质在电子工业中有重要应用,请写出G的最高价氧化物与B的单质在高温下发生置换反应的化学反应方程式__________________。
(4)在10 L的密闭容器中,通入2molHD2气体和l mol D2气体,一定温度下反应后生成HD2气体,当反应达到平衡时,D2的浓度为0.01 mol/L,同时放出约177 kJ的热量,则平衡时HD2的转化率为________;该反应的热化学方程式为__________________;此时该反应的平衡常数K=_________。
查看习题详情和答案>>
(1)以上八种元素中非金属所形成的最简单气态氢化物中稳定性最弱的是____________(填化学式),E、F、H所形成的简单离子的半径由大到小的顺序为____________ (用离子符号表示)。
(2)一定条件下,A的单质与C的单质充分反应可生成气体W,W的结构式为___________。由A、D两元素可以组成X、Y两种化台物,X在一定条件下可以分解生成Y,X的电子式为___________。固体化合物
E2D2与化合物E2H的水溶液按物质的量之比1:1反应生成单质H的离子方程式为__________________。
(3)G是非金属元素,其单质在电子工业中有重要应用,请写出G的最高价氧化物与B的单质在高温下发生置换反应的化学反应方程式__________________。
(4)在10 L的密闭容器中,通入2molHD2气体和l mol D2气体,一定温度下反应后生成HD2气体,当反应达到平衡时,D2的浓度为0.01 mol/L,同时放出约177 kJ的热量,则平衡时HD2的转化率为________;该反应的热化学方程式为__________________;此时该反应的平衡常数K=_________。
A、B、C、D、E五种短周期元素的原子序数依次增大,且已知:①其原子半径的大小关系是:D>E>B>C>A;②A、D同主族,可形成离子化合物;③B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;④B、E两元素原子的最外层电子数之和等于A、C、D三种元素原子的最外层电子数之和.请填写下列空白:
(1)常温下,浓度均为0.lmol/L的B、D的最高价氧化物对应的水化物溶液中,水电离出的c(H+)的相对大小关系为X______Y(填写“大于”“于”或“等于”),化合物BA5所属晶体类型为离子晶体,其电子式为______.
(2)在合成BA3的实际生产过程中,常采取______的方法,使气态BA3变成液态后从混合气体中分离出去,以促使化学平衡向生成BA3的方向移动.
(3)E单质与足量的D的最高价氧化物的水化物溶液反应的离子方程式为______;BC2与水反应被氧化与被还原的物质的量之比是______.
(4)已知在298K时,lg B2A4气体燃烧生成B2和A2C气体,放出16.7kJ的热量.该燃烧反应的热化学方程式______.
(5)X、Y分别是B、C与A形成的10电子微粒,请你提供一个能验证X结合H+能力较Y强的离子方程式______.
查看习题详情和答案>>
(1)常温下,浓度均为0.lmol/L的B、D的最高价氧化物对应的水化物溶液中,水电离出的c(H+)的相对大小关系为X______Y(填写“大于”“于”或“等于”),化合物BA5所属晶体类型为离子晶体,其电子式为______.
(2)在合成BA3的实际生产过程中,常采取______的方法,使气态BA3变成液态后从混合气体中分离出去,以促使化学平衡向生成BA3的方向移动.
(3)E单质与足量的D的最高价氧化物的水化物溶液反应的离子方程式为______;BC2与水反应被氧化与被还原的物质的量之比是______.
(4)已知在298K时,lg B2A4气体燃烧生成B2和A2C气体,放出16.7kJ的热量.该燃烧反应的热化学方程式______.
(5)X、Y分别是B、C与A形成的10电子微粒,请你提供一个能验证X结合H+能力较Y强的离子方程式______.
查看习题详情和答案>>
已知A、B、C、D、E、F、G七种物质有如下转化关系,A、B、C、E都是由两种元素组成的化合物,D、F、G在常温下分别是固、液、气态单质,D、F的组成元素在周期表中位于同一主族。E溶液为浅绿色,与NaOH溶液反应生成的白色沉淀极易被氧化。

试回答下列问题
(1)写出A与B反应的化学方程式__________________________
(2)写出E与Cl2以物质的量之比按1∶1反应的离子方程式________
(3)检验A中阳离子最常用的试剂可用一种钾盐,其化学式为______
(4)实验室制得的B气体,不能用浓硫酸作干燥剂,其原因是______
(5)用惰性电极电解C溶液,其阳极反应为____________________,当转移1 mol e-时在阴极可收集到气体的体积为____L(标况下)。
(6)将2 mol 气体B放入1 L固定容积的某密闭容器中,在一定温度下反应达到平衡,测得D蒸气的体积分数为40%。若其它条件不变,再向该容器中充入2 mol 气体B,则平衡向_________(填“正反应方向”、“逆反应方向”、“不”)移动,当体系的颜色不再变化时D的体积分数_______(填“大于”、“小于”、“等于”)40%。
查看习题详情和答案>>
(1)写出A与B反应的化学方程式__________________________
(2)写出E与Cl2以物质的量之比按1∶1反应的离子方程式________
(3)检验A中阳离子最常用的试剂可用一种钾盐,其化学式为______
(4)实验室制得的B气体,不能用浓硫酸作干燥剂,其原因是______
(5)用惰性电极电解C溶液,其阳极反应为____________________,当转移1 mol e-时在阴极可收集到气体的体积为____L(标况下)。
(6)将2 mol 气体B放入1 L固定容积的某密闭容器中,在一定温度下反应达到平衡,测得D蒸气的体积分数为40%。若其它条件不变,再向该容器中充入2 mol 气体B,则平衡向_________(填“正反应方向”、“逆反应方向”、“不”)移动,当体系的颜色不再变化时D的体积分数_______(填“大于”、“小于”、“等于”)40%。